
-

生物通官微
陪你抓住生命科技
跳动的脉搏
抗生物膜肽Pom-1衍生物拯救氟康唑和两性霉素B对白色念珠菌的耐药性疗效
【字体: 大 中 小 】 时间:2025年07月10日 来源:Scientific Reports 3.8
编辑推荐:
推荐编辑:为解决白色念珠菌(Candida albicans)耐药性及抗真菌药物氟康唑(fluconazole)和两性霉素B(amphotericin B)的严重副作用问题,德国乌尔姆大学等机构研究人员开展抗生物膜肽Pom-1及其衍生物(nAMPs)的中和作用机制研究。结果显示,Pom-1肽通过抑制细胞聚集而非传统孔形成,结合传统药物可将剂量降至10-50%,恢复96%临床耐药株的完全杀灭效果,为减轻药物毒性及开发新型联合疗法提供突破性策略。
德国乌尔姆大学(Ulm University)的研究团队从古巴淡水螺Pomacea poeyana中分离出一种独特肽类Pom-1,其衍生物Pom-1A-F此前已被证明能高效抑制白色念珠菌生物膜且无显著细胞毒性。研究人员提出核心假说:Pom-1可能通过非孔形成机制中和细胞表面互作,从而瓦解聚集过程并恢复传统药物敏感性。为验证这一创新思路,团队首先通过分子动力学模拟和荧光透化实验分析肽-膜互作机制;其次结合临床分离株队列(来自侵袭性感染的27株耐药白色念珠菌),开展生物膜形成抑制实验和细胞活力测试;最后评估肽-药物联用对细胞毒性的影响。
通过CHARMM-GUI和NAMD 2.14软件模拟Pom-1及衍生物与白色念珠菌模型膜(含POPC/POPE/POPS/POPI/Erg脂质)的互作。结果显示:


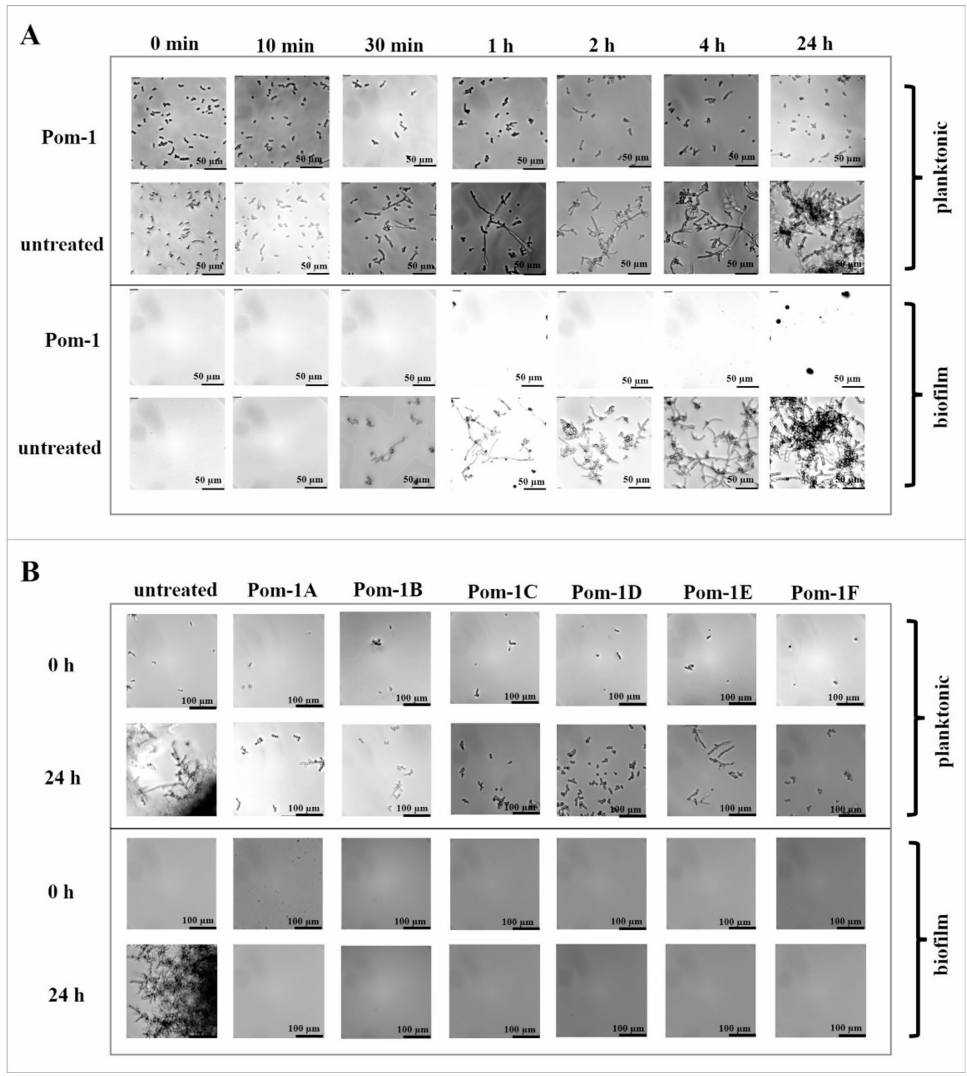
在聚苯乙烯微孔板中培养白色念珠菌参考株(ATCC 90028),添加Pom-1(最小生物膜抑制浓度MBIC=2.5μg/mL)后动态监测:
 生物通微信公众号
生物通微信公众号
知名企业招聘