
-

生物通官微
陪你抓住生命科技
跳动的脉搏
综述:GDF15:从癌症恶病质的生物标志物到治疗靶点
【字体: 大 中 小 】 时间:2025年07月10日 来源:TRENDS IN Cancer 14.3
编辑推荐:
这篇综述深入探讨了生长分化因子15(GDF15)在癌症恶病质(cachexia)中的双重角色:既是疾病进展的生物标志物,又是潜在治疗靶点。文章系统梳理了GDF15通过GFRAL受体调控代谢(如食欲抑制、β-肾上腺素能信号激活)和免疫抑制的机制,并总结了靶向GDF15的抗体(如visugromab、ponsegromab)在逆转免疫治疗耐药和改善患者体重方面的临床突破。
癌症恶病质是一种复杂的代谢紊乱综合征,特征为进行性骨骼肌流失(伴或不伴脂肪减少)和功能损伤。根据国际共识,其分为三个阶段:前恶病质期(体重未明显下降)、恶病质期(6个月内体重下降>5%)和难治性恶病质期(预期生存期<3个月)。胰腺癌、食管癌等患者中恶病质发生率高达80%,而传统营养支持无法逆转这一进程。值得注意的是,最新研究发现胰腺癌患者在确诊前数月已出现肌肉和脂肪流失,提示恶病质可能是癌症早期事件。
作为TGF-β超家族成员,GDF15在生理状态下表达较低(健康成人血清浓度约0.5-2.2 ng/ml),但在应激(如线粒体功能障碍、化疗)、妊娠(第三 trimester可达70 ng/ml)及癌症(晚期患者可达10 ng/ml)时显著升高。其转录受p53、EGR1等调控,并通过整合应激反应(ISR)通路激活。有趣的是,β-地中海贫血患者GDF15水平异常升高(均值66 ng/ml),而转基因小鼠实验显示GDF15可延长寿命并改善代谢,暗示其具有保护性作用。
GFRAL作为GDF15的唯一已知受体,集中表达于延髓最后区(area postrema)和孤束核。当GDF15水平超过阈值时,通过激活RET酪氨酸激酶引发:
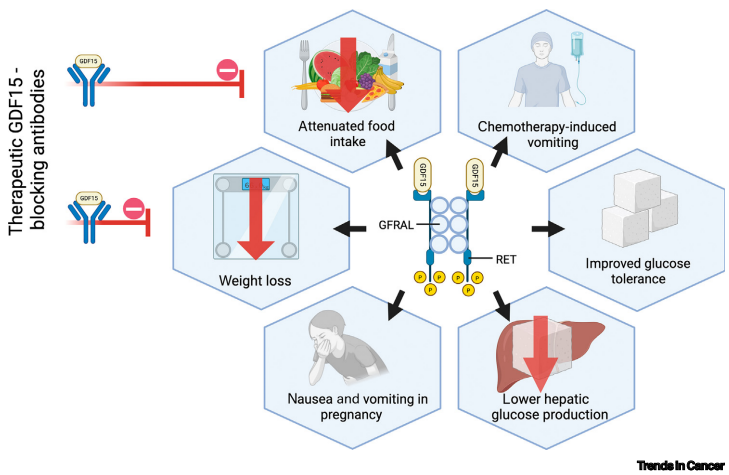
肿瘤微环境中的癌细胞、成纤维细胞和免疫细胞均可分泌GDF15。其通过以下途径促进肿瘤进展:
两项突破性临床试验验证了靶向GDF15的价值:
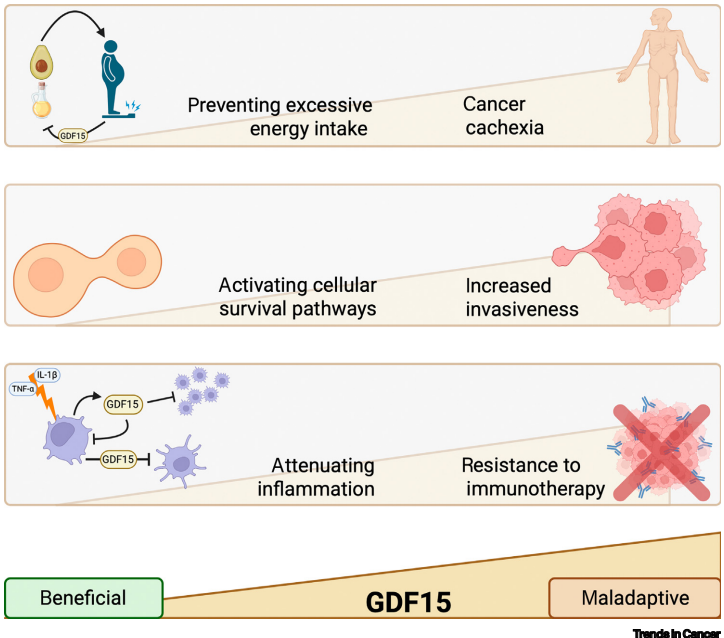
尽管GDF15靶向治疗展现出潜力,仍存在关键问题:
 生物通微信公众号
生物通微信公众号
知名企业招聘