
-

生物通官微
陪你抓住生命科技
跳动的脉搏
巨噬细胞中Fortilin缺失通过多重抗动脉粥样硬化表型改善高胆固醇血症小鼠的动脉粥样硬化
【字体: 大 中 小 】 时间:2025年07月12日 来源:Communications Biology 5.2
编辑推荐:
本研究揭示了Fortilin蛋白在巨噬细胞(MΦ)中的促动脉粥样硬化机制,通过构建巨噬细胞特异性Fortilin敲除小鼠模型(fortilinKO-MΦ-HC),发现其能显著减少主动脉斑块形成。研究证实Fortilin缺失通过增强巨噬细胞凋亡、抑制增殖和泡沫细胞形成,同时促进TGF-β1介导的血管平滑肌细胞(VSMCs)转分化和间充质干细胞(MSCs)分化,为动脉粥样硬化治疗提供了新靶点。
动脉粥样硬化作为全球头号致死疾病,其核心病理特征是动脉内膜中脂质堆积和慢性炎症。巨噬细胞在这一过程中扮演双重角色:既通过吞噬氧化低密度脂蛋白(oxLDL)形成泡沫细胞加剧病变,又通过分泌基质金属蛋白酶削弱斑块稳定性。然而,调控巨噬细胞命运的关键分子机制尚未完全阐明。Fortilin(又称TCTP)是一种多功能抗凋亡蛋白,既往研究发现其在动脉粥样斑块中高表达,但具体作用机制仍是未解之谜。
来自美国德克萨斯大学医学分部(University of Texas Medical Branch)的研究团队通过构建巨噬细胞特异性Fortilin敲除小鼠,结合成像质谱流式(IMC)等前沿技术,首次系统揭示了Fortilin调控动脉粥样硬化的多重机制。研究发现Fortilin缺失通过改变巨噬细胞命运和微环境调控,显著减轻动脉粥样硬化病变,相关成果发表于《Communications Biology》。
研究采用四大关键技术:1) 构建LysM-Cre介导的巨噬细胞特异性Fortilin敲除小鼠模型;2) 应用成像质谱流式(IMC)进行单细胞水平蛋白组学分析;3) 建立THP1人单核细胞Fortilin敲除株(THP1KO-fortilin);4) 开发TGF-β1免疫沉淀技术验证细胞转分化机制。
结果部分
Fortilin缺失显著减轻动脉粥样硬化
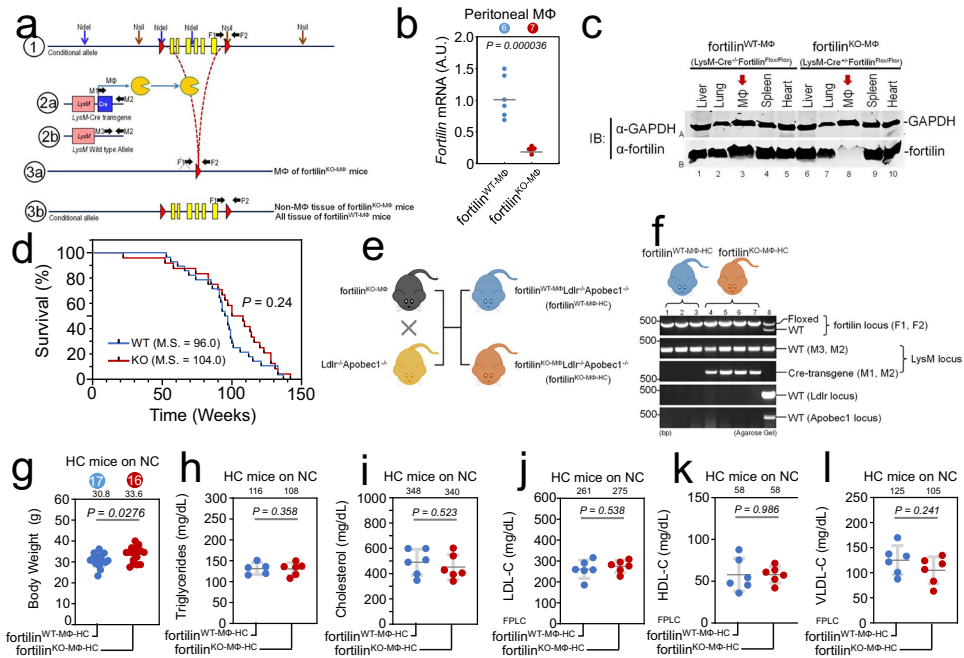
通过主动脉en face和横截面分析发现,fortilinKO-MΦ-HC小鼠斑块面积较野生型减少51.7%和33.0%,血清促炎因子(TNF-α、IFN-γ、IL-23)水平降低,而抗炎因子TGF-β1/β2升高。
IMC揭示斑块细胞组成重塑
Fortilin调控巨噬细胞命运
细胞实验表明:1) Fortilin缺失使THP1细胞对oxLDL诱导的凋亡敏感性增加112%;2) 抑制巨噬细胞增殖(BrdU掺入减少);3) 下调CD36受体使泡沫细胞形成减少95%。
促进VSMCs转分化

驱动MSCs向VSMCs分化
UCDMSCs在fortilinKO-MΦ条件培养基中表达VSMC标志物,该效应可被TGF-β1中和抗体完全阻断,证实TGF-β1是关键效应分子。
这项研究首次阐明Fortilin通过三重机制促进动脉粥样硬化:1) 维持巨噬细胞存活和增殖;2) 抑制其向VSMCs转分化;3) 阻碍MSCs向VSMCs分化。临床转化意义上,针对巨噬细胞Fortilin的小分子抑制剂可能通过同时减少斑块炎症和增加纤维帽稳定性,成为"一石二鸟"的新型治疗策略。研究采用的IMC技术为动脉粥样硬化单细胞研究提供了范式,而TGF-β1介导的细胞命运转换机制也为其他纤维化疾病研究提供了新思路。
 生物通微信公众号
生物通微信公众号
知名企业招聘