
-

生物通官微
陪你抓住生命科技
跳动的脉搏
与新型HPS1突变相关的肾脏黑变病:揭示眼皮肤白化病中黑色素肾脏沉积的分子机制
《BMC Nephrology》:Kidney melanosis associated with a novel HSP-1 Hermansky-Pudlak oculocutaneous albinism mutation: a case report
【字体: 大 中 小 】 时间:2025年07月12日 来源:BMC Nephrology 2.2
编辑推荐:
本研究报道了一例罕见的与新型HPS1基因突变(c.70G>T;p.Glu24Ter)相关的肾脏黑变病病例,通过组织病理学、光谱分析和遗传检测,揭示了Hermansky-Pudlak综合征(HPS)患者肾脏中水溶性黑色素沉积的机制,为理解溶酶体相关细胞器(LRO)功能障碍导致的跨器官黑色素代谢异常提供了新见解。
在医学界,黑色素通常被认为是皮肤和视网膜的专属色素,但近期一项关于"黑色肾脏"的病例研究打破了这一认知。这项发表在《BMC Nephrology》的研究揭示了一个令人费解的现象:为何缺乏皮肤色素沉着的白化病患者,其肾脏会像墨汁般漆黑?这个谜团直指黑色素代谢领域最核心的科学问题——这种被认为不溶于水的大分子聚合物,如何突破多重生理屏障完成"跨器官旅行"?
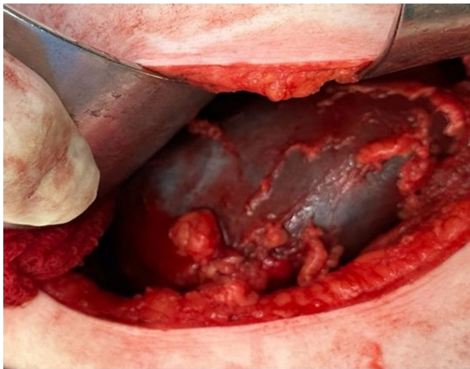
由Alaa A. Ali和Michael D. Hughson等组成的国际研究团队,通过分析一例28岁女性肾移植供体的特殊病例,揭开了这一现象背后的分子机制。这位患有Hermansky-Pudlak综合征(HPS)的供体,虽然皮肤仅呈现轻微色素减退,但其肾脏在手术中呈现出惊人的黑色外观(图1)。研究人员发现,这种独特的肾脏黑变病与一种新型HPS1基因突变(c.70G>T;p.Glu24Ter)直接相关,该突变导致编码蛋白提前终止,影响了溶酶体相关细胞器(LRO)的正常功能。
研究团队采用了多学科技术手段:通过基因检测确认致病突变;组织病理学分析显示黑色素主要沉积在近端肾小管上皮细胞和管腔内巨噬细胞中;Fontana-Masson染色特异性标记黑色素;创新性地建立了尿液黑色素提取和分光光度定量方法,测定肾脏组织黑色素浓度达2 mg/g,并首次证实HPS患者尿液中存在水溶性黑色素。
肾脏病理特征
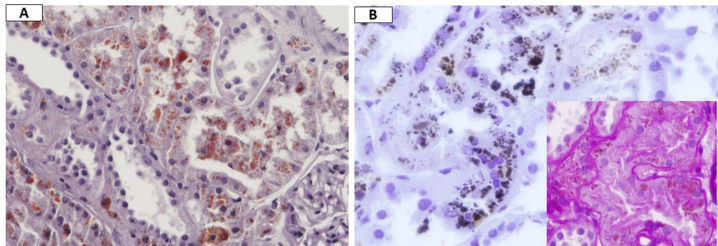
活检显示>60个正常肾小球,近端小管上皮内可见细至粗大的棕色颗粒(图3A),管腔内可见被CD68阳性巨噬细胞包裹的更大颗粒。这些颗粒PAS染色阴性,Fontana-Masson染色阳性(图3B),证实为黑色素而非含铁血黄素或脂褐素。
黑色素代谢分析
分光光度法测定显示黑色素特征性吸收光谱(表1)。尿液黑色素主要为水溶性,推算其真黑色素(eumelanin)排泄量为3.9 mmol/mol肌酐,与健康人群相当。这表明肾脏黑变病并非由黑色素过量产生所致,而是由于HPS1突变导致的溶酶体降解功能障碍。
遗传学发现
基因检测发现 homozygous HPS1 c.70G>T突变,预计产生截短蛋白(p.Glu24Ter)。毛发显微观察显示供体毛发色素颗粒数量与颜色显著减少(图2B),证实其为不完全性眼皮肤白化病(OCA)。

这项研究首次系统阐释了HPS相关肾脏黑变病的病理机制:HPS1突变导致黑色素体(melanosome)等LRO发育异常,使黑色素无法正常储存于皮肤,而以水溶性小分子形式进入循环,经肾小球滤过后被近端小管摄取。由于溶酶体功能缺陷,黑色素不能被有效降解,最终在肾脏异常蓄积。
该发现具有多重意义:①拓展了对HPS多系统受累的认识,将肾脏列为新的靶器官;②提出黑色素"肾肠循环"假说,为理解黑色素系统代谢提供新视角;③建立尿液黑色素检测方法,为HPS患者肾功能监测提供新指标。尽管移植3年后供受体肾功能均正常,但研究者强调需长期随访HPS可能导致的肾、肺和结肠病变。这项研究为罕见病诊疗提供了重要范式,提示对白化病患者应评估肾脏受累风险。
 生物通微信公众号
生物通微信公众号