
-

生物通官微
陪你抓住生命科技
跳动的脉搏
丹参酮通过调节肠道菌群-TMAO轴改善高脂饮食诱导的动脉粥样硬化
【字体: 大 中 小 】 时间:2025年07月12日 来源:BMC Microbiology 4
编辑推荐:
本研究针对动脉粥样硬化(AS)临床治疗药物有限的现状,探索了丹参酮通过调控肠道菌群和氧化三甲胺(TMAO)的治疗潜力。贵州医科大学团队通过APOE-/-小鼠模型发现,丹参酮能显著增加乳酸杆菌丰度、降低毛螺菌科水平,同时抑制TMAO生成及NF-κB炎症通路,为心血管疾病提供了新的菌群-代谢干预策略。
心血管疾病长期占据全球死因首位,其中动脉粥样硬化(Atherosclerosis, AS)是心脑血管事件的主要病理基础。尽管他汀类药物等现有治疗手段取得一定成效,但仍有相当比例患者存在残余风险。近年来,肠道菌群及其代谢产物氧化三甲胺(Trimethylamine N-oxide, TMAO)被证实与AS发生发展密切相关――特定菌群可将饮食中的胆碱转化为促动脉硬化的TMAO,同时激活NF-κB等炎症通路。然而,如何通过天然药物精准调控这一"肠-血管轴"仍是待解难题。
贵州医科大学临床医学院的研究团队在《BMC Microbiology》发表的最新研究中,首次揭示了传统中药活性成分丹参酮(Tanshinone)通过重塑肠道微生态平衡、阻断TMAO生成来改善AS的新机制。研究人员采用高脂饮食(HFD)喂养APOE-/-(载脂蛋白E敲除)小鼠构建AS模型,通过16S rRNA基因测序、LC-MS/MS靶向代谢组学和分子生物学技术,系统评估了丹参酮对肠道菌群结构、TMAO代谢及血管炎症的影响。
关键技术方法
实验选用30只6周龄雄性APOE-/-小鼠,分为正常饮食组、HFD模型组和HFD+丹参酮(30mg/kg/天)干预组。通过油红O染色、Masson染色评估主动脉斑块;收集粪便进行16S rRNA测序分析菌群变化;采用LC-MS/MS检测血浆TMAO、TMA等代谢物;Western blot和qPCR检测NF-κB通路关键分子表达。
菌群重构与代谢调控
16S rRNA测序显示丹参酮显著提升乳酸杆菌(Lactobacillus)丰度(p<0.05),同时抑制HFD诱导的毛螺菌科(Lachnospiraceae)过度增殖(p<0.001)。功能预测分析表明,丹参酮组菌群的脂代谢功能显著增强。代谢组学数据证实,丹参酮使血浆TMAO水平降低42%(p<0.01),但 paradoxically升高其前体胆碱浓度,提示其可能通过抑制菌群胆碱-TMA转化酶活性发挥作用。
炎症通路抑制
分子机制研究发现,丹参酮组主动脉组织磷酸化NF-κB(p-NF-κB)蛋白表达较模型组降低58%(p<0.01),下游炎症因子IL-1β、TNF-α的mRNA水平同步下降(p<0.05)。这与其上调的乳酸杆菌产生短链脂肪酸(SCFAs)、抑制毛螺菌科相关内毒素释放的菌群重构特征高度吻合。
病理改善证据
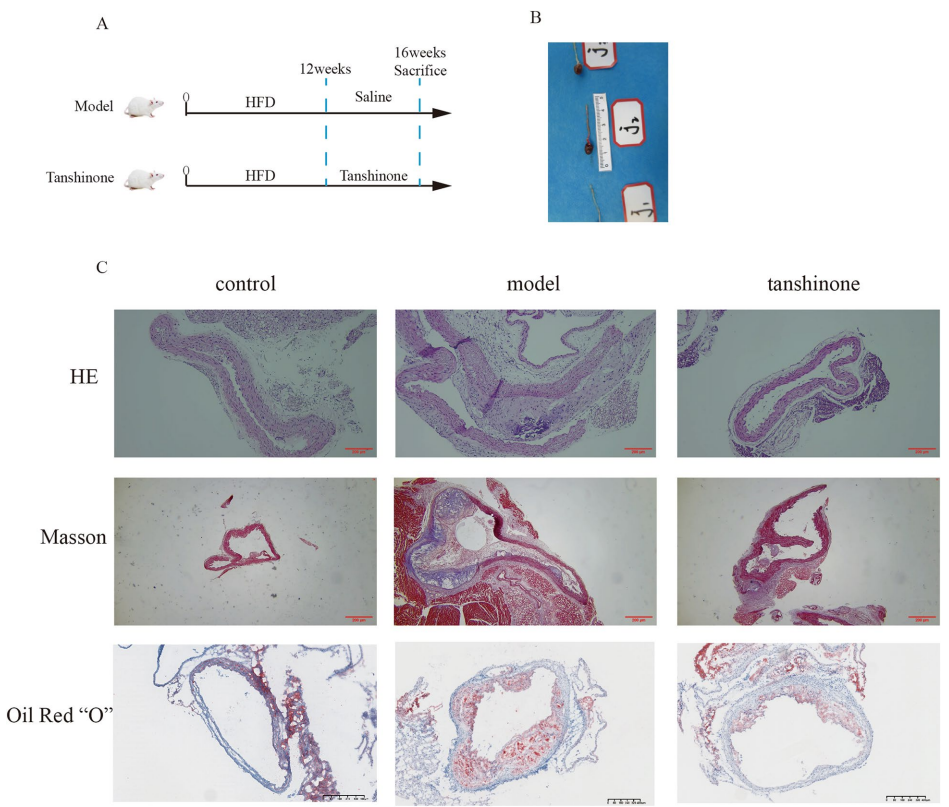
油红O染色显示丹参酮组主动脉斑块面积较模型组减少67%(p<0.001),Masson染色提示胶原纤维含量增加1.8倍,HE染色显示血管壁结构完整性明显改善。
这项研究首次阐明丹参酮通过"乳酸杆菌↑-毛螺菌科↓-TMAO↓-NF-κB↓"的多靶点级联反应发挥抗AS作用。其创新性在于:①发现丹参酮可特异性富益生菌并抑制促炎菌群;②揭示其降低TMAO但不影响前体胆碱的独特代谢调控模式;③为中药"多成分-多靶点"作用机制提供微生物组学证据。该成果不仅为AS治疗提供了新的菌群干预策略,也为开发靶向FMO3(黄素单加氧酶3)或菌群酶的天然药物奠定基础。未来研究可进一步解析丹参酮中具体有效单体成分,并探索其与现有降脂药物的协同效应。
 生物通微信公众号
生物通微信公众号
知名企业招聘