
-

生物通官微
陪你抓住生命科技
跳动的脉搏
增强5T4 mRNA疫苗效力:CD70 mRNA-LNPs通过ADCC和T细胞激活在前列腺癌治疗中的应用
【字体: 大 中 小 】 时间:2025年07月19日 来源:Journal of Nanobiotechnology 10.6
编辑推荐:
本研究针对前列腺癌治疗中传统疗法效果有限的难题,创新性地将5T4肿瘤相关抗原与免疫激活因子CD70通过脂质纳米颗粒(LNPs)共递送。研究发现5T4+CD70 mRNA-LNPs能显著增强体液免疫(5T4特异性抗体)和细胞免疫(CD8+T细胞与NK细胞活性),在小鼠模型中实现肿瘤抑制和生存期延长。该策略为mRNA疫苗联合免疫调节因子的临床应用提供了新思路。
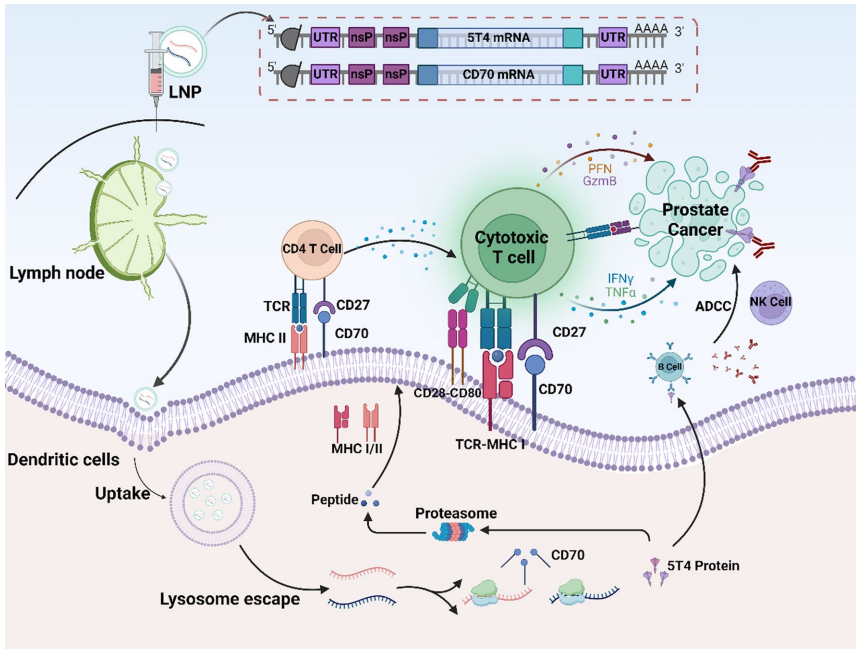
前列腺癌作为男性高发恶性肿瘤,传统疗法对晚期患者效果有限,亟需新型治疗策略。尽管mRNA疫苗在肿瘤免疫治疗中展现出快速定制和高效激活免疫的优势,但单一肿瘤相关抗原(TAA)疫苗常因肿瘤微环境(TME)的免疫抑制而疗效不足。中山大学的研究团队创新性地将胎盘源性肿瘤抗原5T4与共刺激分子CD70通过脂质纳米颗粒(LNPs)联合递送,在《Journal of Nanobiotechnology》发表的研究表明,这种组合能协同激活先天性与适应性免疫,为前列腺癌治疗提供了突破性方案。
研究采用优化序列的5T4和CD70 mRNA,通过自主开发的离子化脂质E12A1A3构建LNPs递送系统。利用B16-OVA和RM-1前列腺癌小鼠模型,通过流式细胞术、ELISpot和RNA测序等技术,系统评估了免疫应答效果。
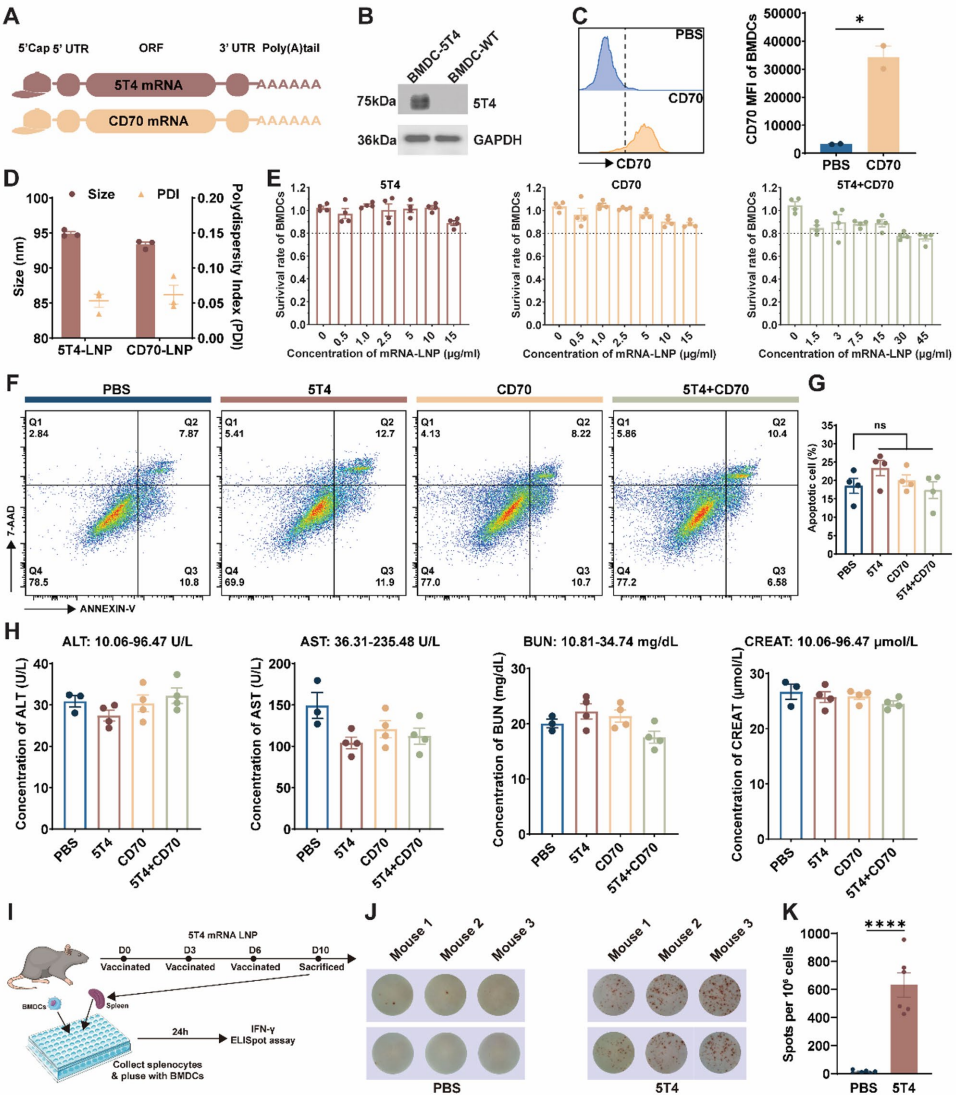
mRNA-LNPs的制备与表征
研究团队首先优化了5T4和CD70的开放阅读框(ORF),合成的mRNA经Western blot验证可在树突状细胞(BMDCs)高效表达。动态光散射显示LNPs粒径为90-100nm,封装效率>90%。安全性实验证实1μg/ml剂量下BMDCs存活率>85%,小鼠肝肾功能指标正常。
免疫激活机制
5T4+CD70组合使BMDCs的MHC-II和共刺激分子(CD80/CD86)表达提升2-3倍,促进T细胞分泌IFN-γ和TNF-α。在无瘤小鼠中,该组合使5T4特异性抗体水平提高4倍,CD8+T细胞杀伤效率达70%。RNA测序显示该疗法显著上调cDC1相关基因(IRF8、CLE9A)和T细胞激活标记(CD27、CXCR6)。
肿瘤模型验证
在B16-OVA模型中,CD70使OVA特异性IgG提高3倍,NK细胞活化标记CD69+比例增加50%。前列腺癌RM-1模型显示,联合治疗组肿瘤体积<500mm3,生存期延长5天。免疫荧光证实肿瘤部位IFN-γ表达显著增强,脾脏中央记忆T细胞(TCM)比例提升2倍。
讨论与意义
该研究首次将LNPs技术应用于5T4靶向治疗,克服了病毒载体疫苗的基因毒性风险。CD70通过三重机制增强疗效:1)促进生发中心B细胞分化;2)激活NK细胞介导的ADCC;3)诱导TCM形成长效免疫记忆。值得注意的是,CD70的短暂表达特性避免了慢性刺激导致的免疫抑制,这为其他肿瘤的联合免疫治疗提供了范式。未来需在灵长类模型中验证长期安全性,并探索与PD-1抑制剂的联用潜力。
 生物通微信公众号
生物通微信公众号
知名企业招聘