
-

生物通官微
陪你抓住生命科技
跳动的脉搏
婴儿早期补充Bifidobacterium infantis M-63通过建立双歧杆菌优势肠型发挥抗炎作用
《Pediatric Research》:Anti-inflammatory effects of Bifidobacterium infantis M-63 during the early postnatal period in term infants
【字体: 大 中 小 】 时间:2025年07月19日 来源:Pediatric Research 3.1
编辑推荐:
本研究针对新生儿早期肠道菌群建立关键期,通过随机对照试验证实:补充Bifidobacterium infantis M-63可显著增加婴儿肠道双歧杆菌丰度,降低促炎因子IFN-γ和IL-1β水平,同时提升有益代谢物吲哚-3-乳酸(ILA)和短链脂肪酸(SCFA)产量。该成果为通过益生菌干预塑造健康肠道微环境提供了新证据,发表于《Pediatric Research》。
生命最初的100天是塑造人体肠道微生态的关键窗口期。在这个阶段,肠道菌群的组成不仅影响婴儿的免疫发育,还与远期健康密切相关。然而,现代生活方式、抗生素使用等因素常导致婴儿肠道菌群失调,表现为双歧杆菌减少而肠杆菌科增多,这种失衡可能引发炎症反应,甚至增加过敏、代谢性疾病等风险。如何通过安全有效的方式优化新生儿肠道菌群,成为儿科和微生物学研究的热点问题。
Morinaga Milk Industry Co., Ltd(日本森永乳业)的研究团队在《Pediatric Research》发表了一项突破性研究。他们发现,给健康足月儿早期补充特定益生菌株Bifidobacterium infantis M-63,不仅能快速建立双歧杆菌优势肠道环境,还能显著降低炎症水平。这种"菌株-代谢物-免疫"的三重调控机制,为预防婴儿炎症相关疾病提供了新思路。
研究人员采用多组学技术开展这项工作:通过16S rRNA测序分析111名婴儿的肠道菌群动态;采用LC-MS/MS检测吲哚类代谢物;结合ELISA和多重免疫分析定量粪便炎症标志物(如calprotectin)和细胞因子(如IL-1β)。所有样本采集时间点覆盖新生儿期至3月龄,并采用严格的随机双盲对照设计。
主要发现如下:
肠道菌群组成
补充B. infantis M-63使双歧杆菌相对丰度显著提升(q<0.05),同时抑制肠杆菌科生长。通过PAM聚类分析鉴定出6种肠型,其中双歧杆菌优势型(ET-Bifi 1/2)与母乳喂养率正相关(p<0.05)。
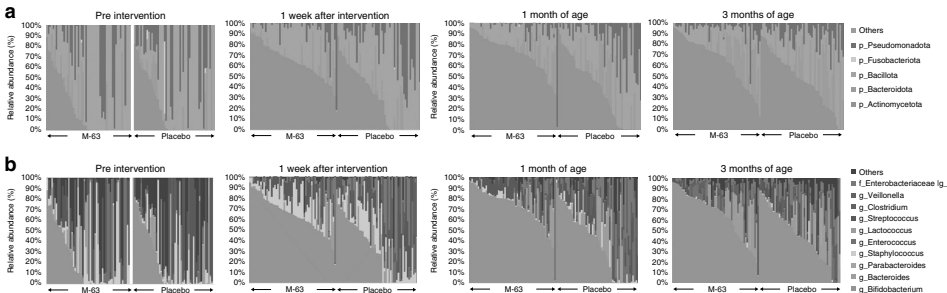
代谢物特征
双歧杆菌优势肠型中,吲哚-3-乳酸(ILA)、吲哚-3-醛(IAld)等色氨酸代谢物水平显著高于其他肠型(p<0.05)。这些物质可通过芳香烃受体(AhR)通路发挥抗炎作用。
免疫调节
ET-Bifi 1肠型婴儿的促炎因子IFN-γ和IL-1β水平较ET-Ent肠型降低2-3倍(p<0.05),同时粪便钙卫蛋白(炎症标志物)水平显著下降,而分泌型IgA(sIgA)有所升高。
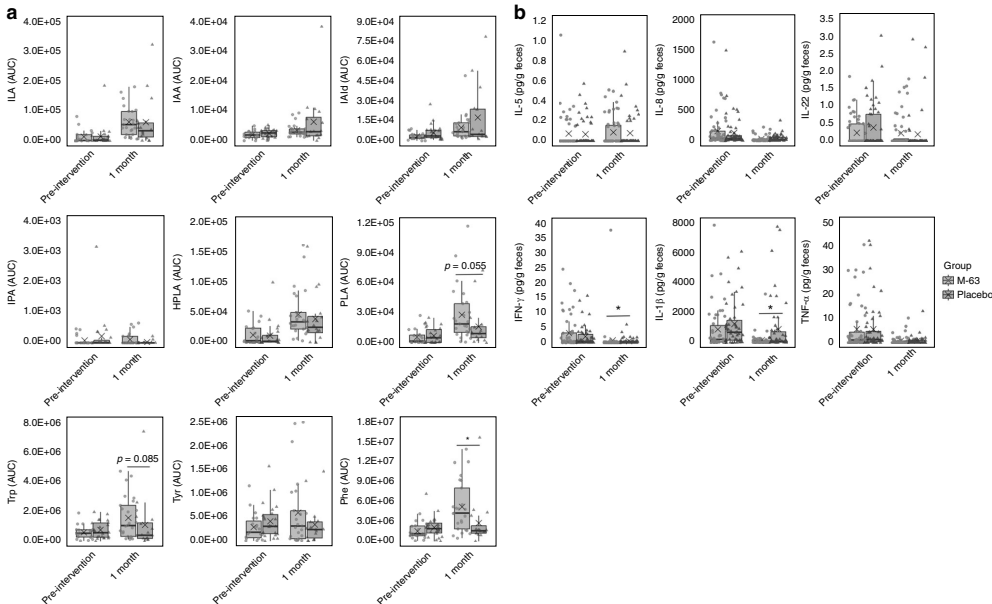
动态演变规律
通过追踪菌群变迁发现,母亲妊娠期增重不足可能影响婴儿双歧杆菌定植速度。早期形成双歧杆菌优势集群(Cluster III)的婴儿,其乙酸产量和IL-22水平显著优于其他集群(p<0.05)。
这项研究首次证实:单一益生菌株B. infantis M-63可通过塑造特定肠型发挥抗炎作用。其机制涉及:①优先利用母乳寡糖(HMOs)竞争性抑制致病菌;②产生ILA等AhR配体调节免疫;③促进乙酸等SCFA生成。该发现为婴幼儿配方食品开发和炎症预防提供了精准干预靶点,后续可进一步探索其对过敏性疾病等的长期影响。
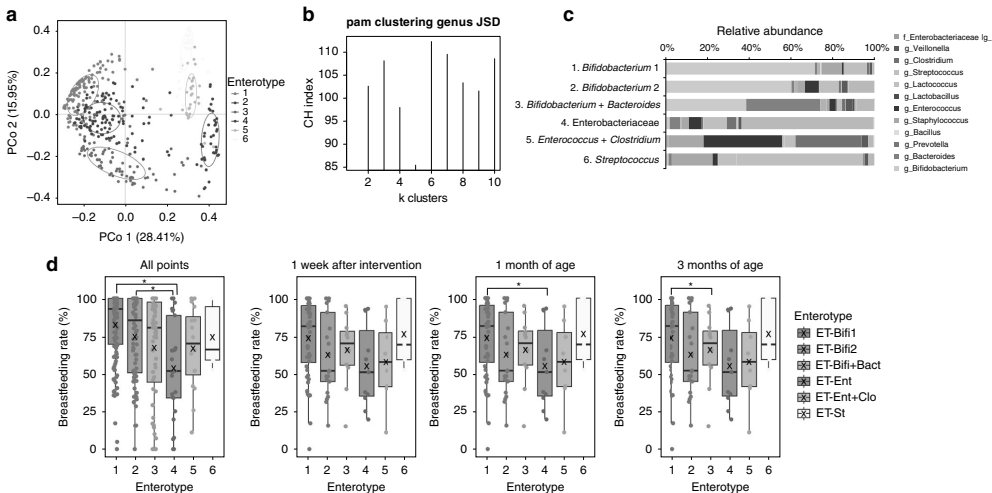
值得注意的是,研究也揭示了个体差异:母乳喂养不足可能削弱益生菌效果,提示未来需结合喂养策略进行个性化干预。这项来自日本团队的工作,为全球婴幼儿肠道菌群研究提供了高质量循证依据。
 生物通微信公众号
生物通微信公众号