
-

生物通官微
陪你抓住生命科技
跳动的脉搏
免疫检查点抑制剂联合治疗晚期黑色素瘤的安全性差异:基于FAERS数据库的NIVO-IPI与NIVO-RELA药物警戒学研究
【字体: 大 中 小 】 时间:2025年07月20日 来源:BMC Cancer 3.4
编辑推荐:
本研究针对晚期黑色素瘤治疗中两种免疫检查点抑制剂(ICIs)联合方案――纳武利尤单抗联合伊匹木单抗(NIVO-IPI)与纳武利尤单抗联合瑞拉利单抗(NIVO-RELA)的安全性差异展开。研究人员通过FDA不良事件报告系统(FAERS)数据库进行不成比例分析,发现NIVO-IPI更易引发胃肠道、内分泌及肝胆毒性,而NIVO-RELA心脏特异性风险更高。该研究为临床治疗方案选择提供了重要安全性依据。
黑色素瘤作为最具侵袭性的皮肤恶性肿瘤,其治疗一直是肿瘤学领域的重大挑战。随着免疫检查点抑制剂(Immune checkpoint inhibitors, ICIs)的出现,晚期黑色素瘤的治疗格局发生了革命性变化。然而,不同ICI联合方案带来的安全性差异却成为临床决策的痛点――医生们面临着一个关键问题:如何在疗效和毒性之间取得最佳平衡?
这一问题在两种重要联合方案中尤为突出。2015年获批的纳武利尤单抗联合伊匹木单抗(Nivolumab plus ipilimumab, NIVO-IPI)虽然疗效显著,但高达60%的3-4级免疫相关不良事件(irAEs)发生率令人望而生畏。而2022年新获批的纳武利尤单抗联合瑞拉利单抗(Nivolumab plus relatlimab, NIVO-RELA)虽然毒性较低,但其安全性特征尚未完全阐明。临床前研究表明,CTLA-4抑制剂(伊匹木单抗)和LAG-3抑制剂(瑞拉利单抗)作用于不同的免疫检查点通路,理论上会导致不同的毒性谱,但缺乏真实世界的大规模安全性数据验证。
为解决这一关键问题,研究人员开展了一项基于FDA不良事件报告系统(FAERS)的大规模药物警戒学研究。该研究创新性地采用不成比例分析方法,比较了2015年第四季度至2024年第四季度期间7482例NIVO-IPI和185例NIVO-RELA治疗相关不良事件报告。通过计算报告比值比(ROR)和信息成分(IC)等指标,系统评估了两种方案的安全性差异。
研究方法上,研究团队首先对FAERS数据库进行了严格的数据清洗,包括去重、病例筛选和MedDRA术语编码。主要采用不成比例分析方法,计算ROR和IC值及其95%置信区间(95% CI),并设置病例数≥3作为信号检测阈值。同时分析了不良事件发生时间(TTO),采用Kruskal-Wallis检验比较组间差异。
研究结果部分揭示了两种方案的显著安全性差异:
临床基线特征
数据显示,NIVO-IPI组不良事件报告量是NIVO-RELA组的40倍(7482 vs 185例),主要反映了两者上市时间的差异。值得注意的是,NIVO-IPI组死亡率更高(18.59% vs 13.51%),提示其毒性可能更严重。
不成比例分析
在系统器官分类(SOC)层面,NIVO-IPI显示出更广泛的多器官毒性信号,包括:
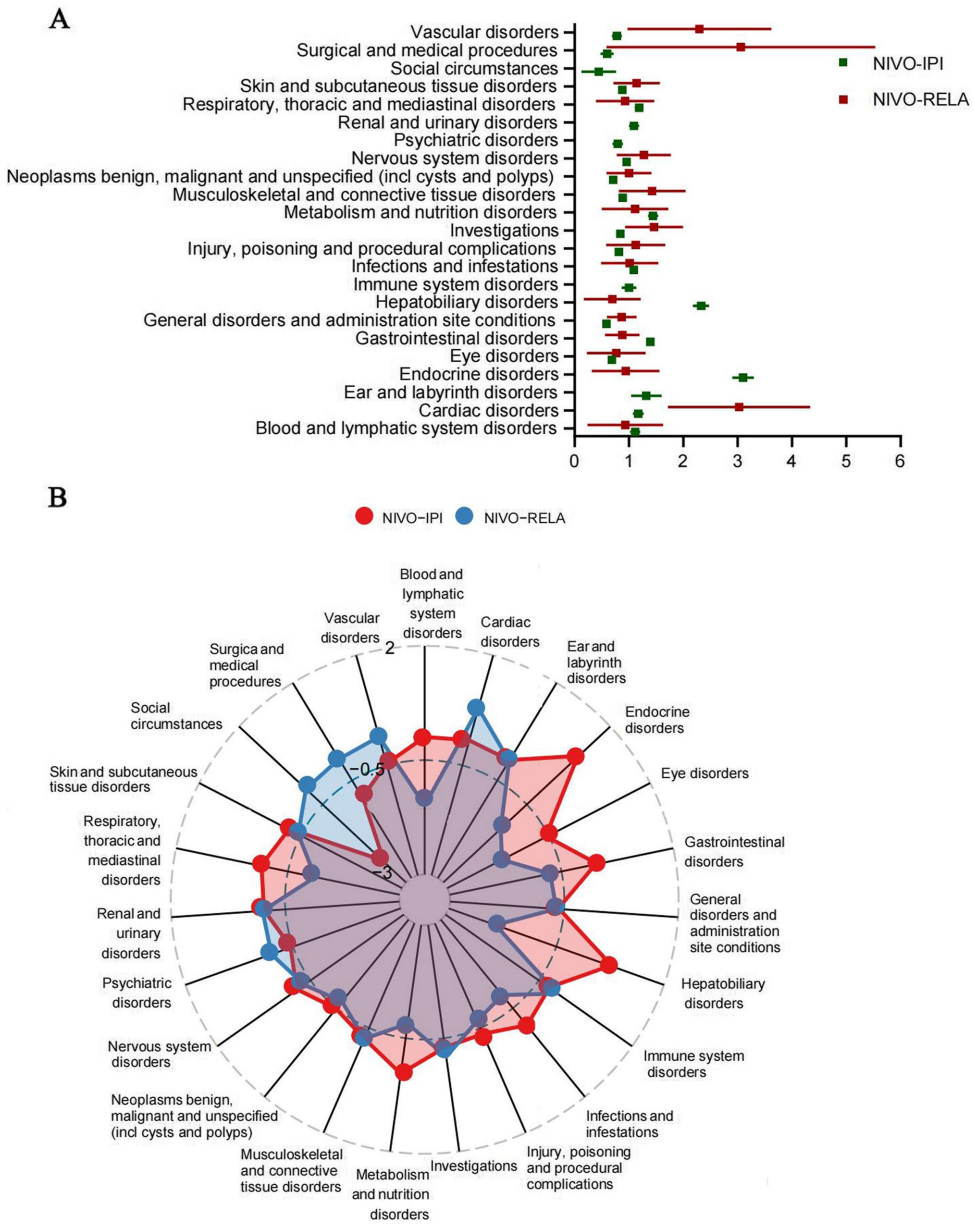
而NIVO-RELA则表现出显著的心脏疾病(ROR=2.84)和血管疾病(ROR=2.04)风险。在优选术语(PT)层面,NIVO-IPI最常见的毒性是结肠炎、垂体炎和肝炎,而NIVO-RELA则以心肌炎、肌钙蛋白升高和重症肌无力为特征性毒性。
发生时间分析
约80%的不良事件发生在治疗开始后3个月内。NIVO-IPI组中位发生时间为42天(IQR 18-91天),NIVO-RELA组为57天(IQR 18-89天),但差异无统计学意义(p=0.66)。

研究结论强调,NIVO-IPI和NIVO-RELA展现出截然不同的安全性特征:前者带来更广泛的免疫相关毒性,后者则主要表现为心脏特异性风险。这一发现具有重要的临床指导价值――治疗选择应基于个体化风险评估,对NIVO-IPI患者需重点监测肝功能和内分泌指标,而NIVO-RELA患者则应定期进行心脏评估。
该研究的创新性在于首次通过真实世界大数据系统比较了两种ICI联合方案的安全性差异,弥补了临床试验样本量有限、随访时间短的不足。特别是发现了NIVO-RELA的心脏毒性信号,这一发现在其关键临床试验RELATIVITY-047中并未充分体现。研究结果直接影响了临床实践,为NCCN指南推荐的治疗方案选择提供了重要安全性依据。
值得注意的是,研究也存在一定局限性,包括FAERS数据的自发报告性质导致的偏倚、NIVO-RELA样本量较小、以及缺乏详细的临床背景信息等。未来需要通过更大规模的前瞻性研究验证这些发现,并进一步探索毒性发生的分子机制。
 生物通微信公众号
生物通微信公众号
知名企业招聘