
-

ЙъОпНЁ№ЩОў
ЕгДгЧҘЧЎЙъГьҝЖјј
Мш¶ҜөДВцІ«
ЧЫКцЈә°ЧЮјВ«ҙјёәФШЛ®ДэҪәУГУЪ°©Цў°РПтУл¶аДЈКҪЦОБЖөДРӯН¬ІЯВФСРҫҝ
ЎҫЧЦМеЈә ҙу ЦР РЎ Ўҝ КұјдЈә2025Дк07ФВ22ИХ АҙФҙЈәDiscover Oncology 2.8
ұајӯНЖјцЈә
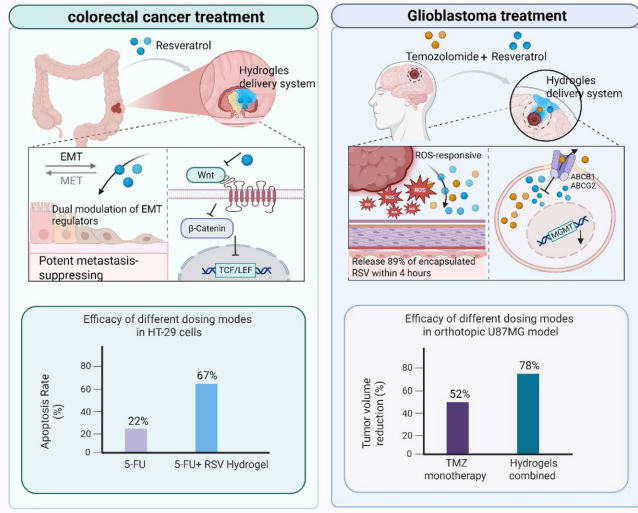
ЎЎЎЎХвЖӘЧЫКцПөНіМҪМЦБЛ°ЧЮјВ«ҙј(RSV)УлЛ®ДэҪәөЭЛНПөНіөДРӯН¬ҝ№ЦЧБц»ъЦЖЎЈЧчХЯЦёіцRSVНЁ№эТЦЦЖWnt/ҰВ-cateninЎўPI3K/AktөИНЁВ··ў»У¶а°РөгЧчУГЈ¬ө«ГжБЩҙъР»ҝмЎўЙъОпАыУГ¶ИөН(<5%)өИМфХҪЎЈЛ®ДэҪәЖҫҪиpH/ОВ¶ИПмУҰРФЎўЧФРЮёҙөИМШРФЈ¬ҝЙМбЙэRSVОИ¶ЁРФ(°ь·вВКЎЦ80%)ІўКөПЦЦЧБцОў»·ҫі(TME)ҙҘ·ўКН·ЕЈ¬ФЪҪбЦұіҰ°©(ТЦЦЖҰВ-cateninәЛЧӘО»58%)әНҪәЦКДёПё°ыБц(ROSПмУҰРФКН·Е89%)ДЈРНЦРХ№ПЦПФЦшБЖР§ЎЈ
°ЧЮјВ«ҙј(RSV)ЧчОӘМмИ»¶а·УЈ¬НЁ№э¶аЦШ»ъЦЖ¶Фҝ№°©ЦўЈәТЦЦЖPI3K/AktНЁВ·(ёО°©ЦРp-AktҪөөН>50%)ЎўЧи¶ПWnt/ҰВ-cateninРЕәЕ(ИйПЩ°©IC50=0.98ҰМM)ТФј°ұн№ЫТЕҙ«өчҝШ(Оё°©ЦРSEMA3AЖф¶ҜЧУјЧ»щ»ҜҪөөН40%)ЎЈИ»¶шЖдБЩҙІУҰУГКЬПЮУЪҝмЛЩҙъР»(ҝЪ·юЙъОпАыУГ¶И<5%)әНјББҝТААөРФЛ«ПаР§УҰЎӘЎӘөНЕЁ¶ИјӨ»оSIRT1ҙЩҙж»оЈ¬¶ш25ҰМMТФЙПФтУХөјөтНцЎЈ
ЦЗДЬЛ®ДэҪәНЁ№эИэҙуҙҙРВҝЛ·юRSVИұПЭЈә

ФЪҪбЦұіҰ°©ЦРЈ¬ФШТ©Л®ДэҪәК№5-·ъДтаЧаӨ(5-FU)өтНцВКҙУ22%МбЙэЦБ67%Ј¬Жд»ъЦЖОӘЈә
ҫЎ№Ь4DҙтУЎЛ®ДэҪә(ИзHAMA-GelMA)ТСКөПЦ91%ФШТ©Р§ВКЈ¬ө«ЕъБҝЙъІъТ»ЦВРФ(ҝЧҫ¶Ж«Іо>40ҰМmҪ«У°ПмТ©Оп·ЦІј)әНіӨЖЪЙъОпПаИЭРФИФКЗЖҝҫұЎЈРВРЛCRISPR-Cas9№ІөЭЛНПөНі(ИзЦ¬ЦКМеДЈ°еЛ®ДэҪә)НЁ№эPLK1»щТтұајӯУлRSVБӘУГЈ¬ОӘMYCЗэ¶Ҝ№ЗИвБцМṩәПіЙЦВЛАІЯВФЈ¬ө«РиҫҜМиФӨҙжҝ№Cas9ҝ№Ме(ИЛИәСфРФВК5-95%)өДёЙИЕЎЈ
ХвіЎЛ®ДэҪәҪйөјөДТ©ОпөЭЛНёпГьЈ¬ХэҪ«КөСйКТөД·ЦЧУ·ўПЦЧӘ»ҜОӘ¶Фҝ№°©ЦўөДҫ«ЧјОдЖчЈ¬¶шҪвҫц№жДЈ»ҜЙъІъУлГвТЯФӯРФЖҪәвҪ«іЙОӘПВТ»ҪЧ¶ОөДЦч№Ҙ·ҪПтЎЈ
 ЙъОпНЁОўРЕ№«ЦЪәЕ
ЙъОпНЁОўРЕ№«ЦЪәЕ
ЦӘГыЖуТөХРЖё
ҪсИХ¶ҜМ¬ | ИЛІЕКРіЎ | РВјјКхЧЁАё | ЦР№ъҝЖС§ИЛ | ФЖХ№МЁ | BioHot | ФЖҪІМГЦұІҘ | »бХ№ЦРРД | МШјЫЧЁАё | јјКхҝмС¶ | Гв·СКФУГ
°жИЁЛщУР ЙъОпНЁ
Copyright© eBiotrade.com, All Rights Reserved
БӘПөРЕПдЈә
ФБICPұё09063491әЕ