
-

生物通官微
陪你抓住生命科技
跳动的脉搏
高原脑水肿患者外泌体通过改变氧化应激反应诱导小鼠认知功能障碍的机制研究
【字体: 大 中 小 】 时间:2025年07月25日 来源:Translational Psychiatry 5.8
编辑推荐:
本研究针对高原脑水肿(HACE)患者认知功能障碍的机制展开探索,发现HACE患者来源的外泌体通过下调STAMBP蛋白表达,激活氧化应激反应和神经炎症通路,导致小鼠海马神经元死亡和认知功能损伤。研究人员采用外泌体脑区注射结合行为学评估,结合蛋白质组学和免疫荧光技术,首次揭示了外泌体介导的神经损伤新机制,为HACE的早期干预提供了潜在治疗靶点。
当登山者快速进入高海拔地区时,高原脑水肿(HACE)就像一位不速之客悄然降临。这种由急性缺氧引发的神经系统疾病,不仅带来头痛呕吐等躯体症状,更会留下持久的认知功能障碍记忆减退、注意力不集中等后遗症。尽管血管性水肿和细胞毒性理论部分解释了其发病机制,但患者脑内"分子快递"外泌体在疾病进程中的作用始终是个未解之谜。
中央民族大学的研究团队在《Translational Psychiatry》发表的研究给出了突破性答案。他们发现HACE患者血液中的外泌体竟是导致认知障碍的"危险包裹",这些直径仅30-150纳米的囊泡能够穿越血脑屏障,在海马齿状回(DG)区域引发连锁反应:通过下调STAMBP蛋白表达打破氧化应激平衡,激活的小胶质细胞像失控的"清道夫"般释放炎症因子,最终导致神经元树突棘减少和突触可塑性损伤。这项研究不仅揭示了外泌体在HACE中的致病作用,更发现了STAMBP这一关键调控靶点。
研究人员采用多学科技术手段展开攻关:从11例HACE患者血清中分离外泌体,通过精确定位注射技术将其递送至小鼠海马DG区;采用开放旷场、新奇物体识别等系列行为学测试评估认知功能;运用OLINK蛋白质组学筛选差异表达蛋白;结合高尔基染色和免疫荧光技术观察神经元形态变化;通过检测MDA、SOD等氧化应激指标解析分子机制。
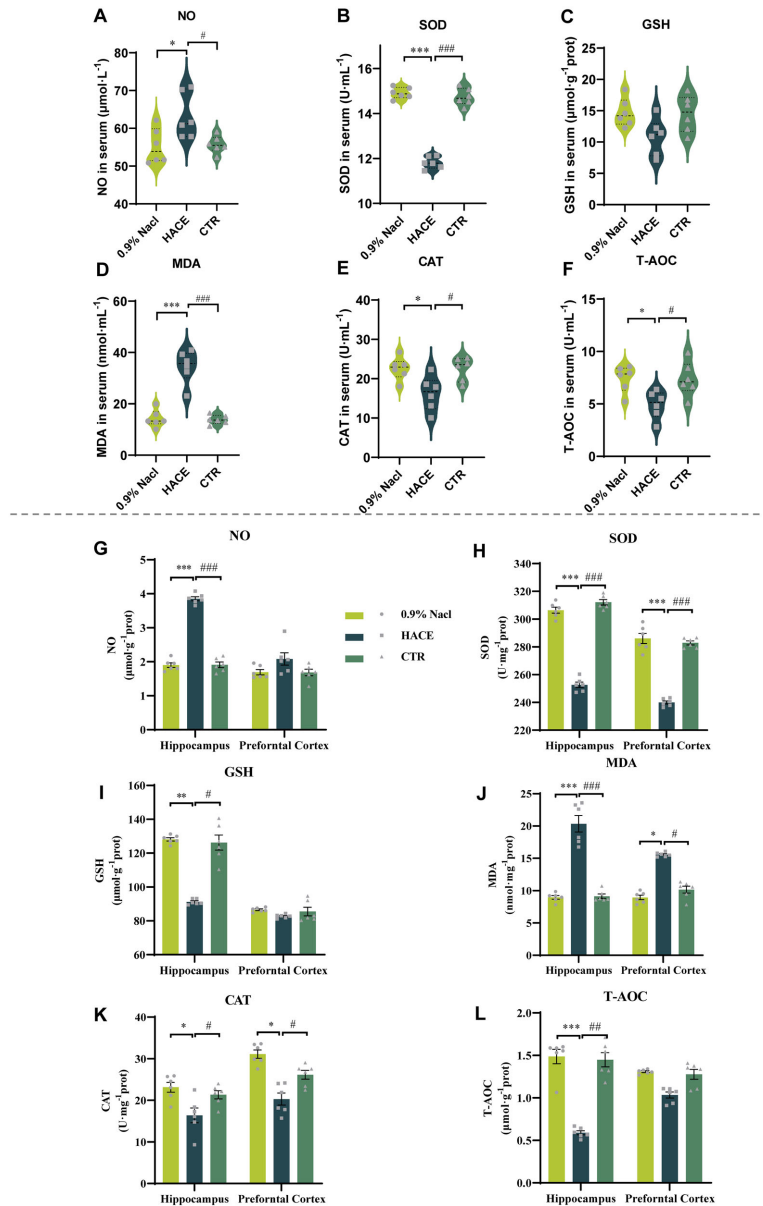
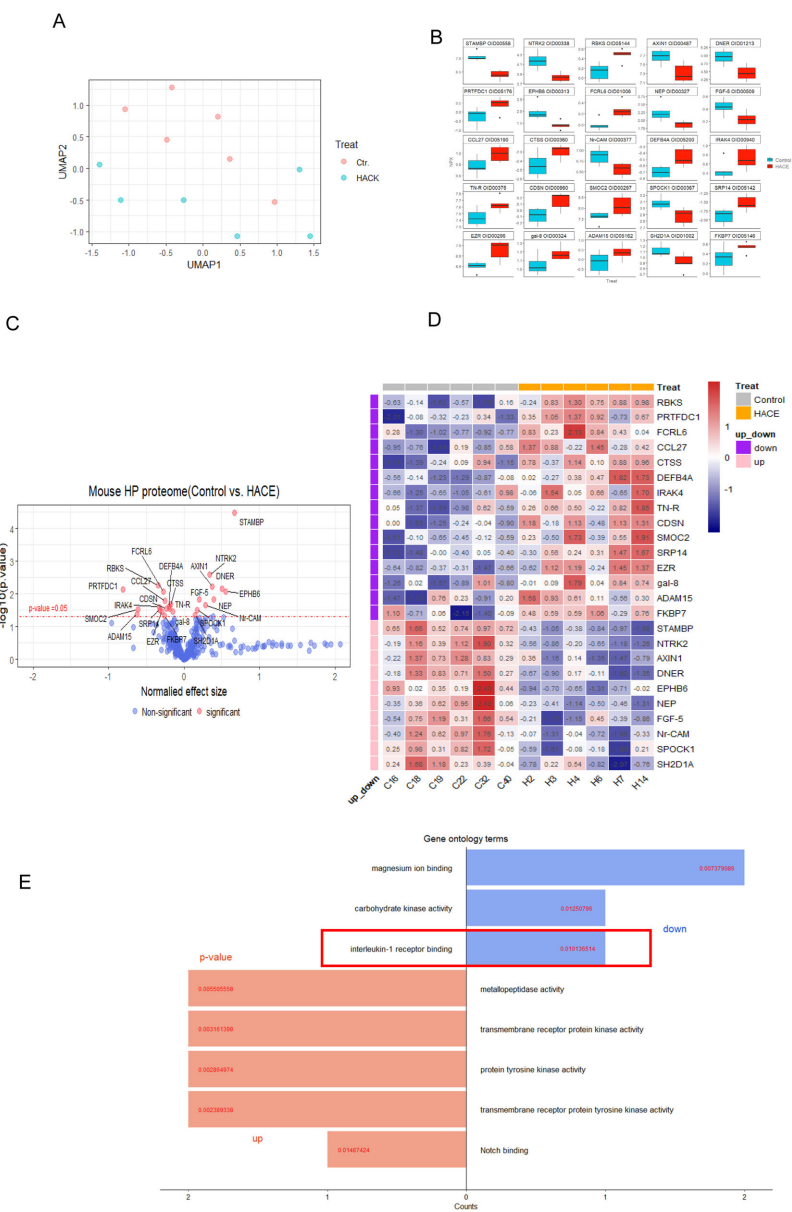
研究结果显示,HACE外泌体注射组小鼠在新奇物体识别测试中探索时间减少41.7%,Y迷宫自发交替率降低35.2%,表现出显著认知障碍。分子层面发现海马区NO水平升高2.3倍,SOD活性异常增加1.8倍,而神经保护因子GSH-Px下降至对照组的60%。蛋白质组学鉴定出25个差异表达蛋白,其中STAMBP下调最显著,该蛋白与神经干细胞增殖密切相关。
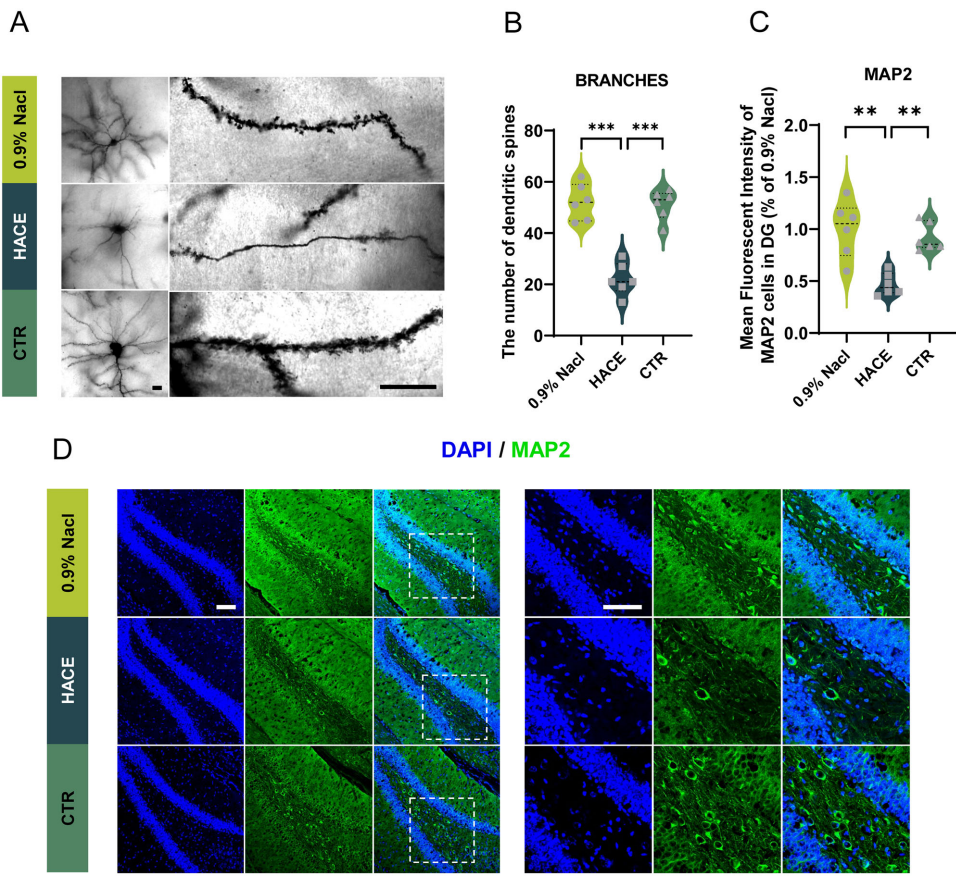
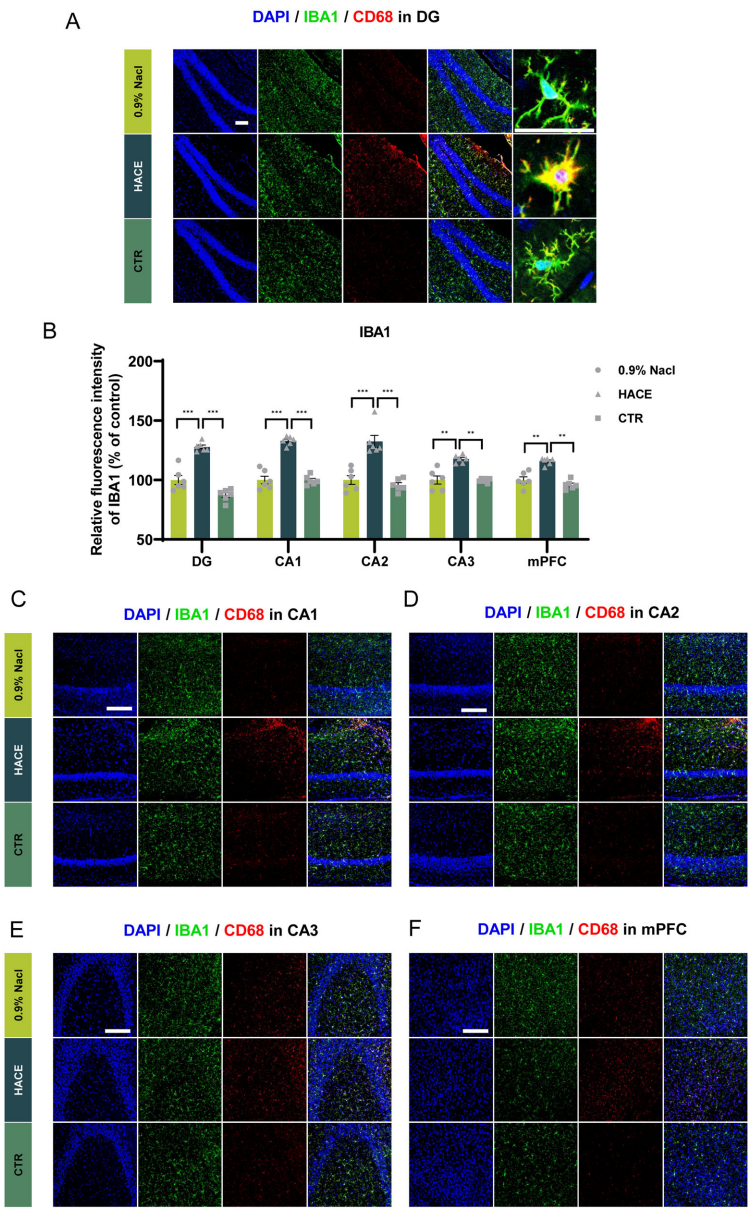
免疫荧光结果显示,HACE组小鼠DG区MAP2阳性神经元减少42%,树突棘密度降低37.5%。更值得注意的是,小胶质细胞标志物IBA1在CA1、CA3等区域的表达量增加2.1倍,且呈现胞体增大、突起缩短的活化形态。这些异常变化通过GO富集分析发现与"白细胞介素-1受体结合"通路密切相关,提示神经炎症与氧化应激存在交叉对话。
这项研究首次系统阐释了HACE患者外泌体通过STAMBP-氧化应激-神经炎症轴导致认知功能障碍的级联机制。从转化医学角度看,发现STAMBP等15个上调和10个下调的差异蛋白为开发早期诊断标志物提供了分子库;从治疗策略看,靶向外泌体介导的病理信号传递或将成为干预HACE的新思路。研究不仅深化了对高原病发病机制的认识,也为其他缺氧性脑损伤疾病的研究提供了方法学借鉴。
未来研究可进一步探索:STAMBP调控神经干细胞增殖的具体机制;外泌体中哪些特定miRNA或蛋白质 cargo 起关键作用;以及通过药物干预STAMBP表达能否逆转认知损伤。这些问题的解答将推动HACE治疗从对症支持向靶向治疗的转变。
 生物通微信公众号
生物通微信公众号
知名企业招聘