
-

生物通官微
陪你抓住生命科技
跳动的脉搏
特瑞普利单抗联合维迪西妥单抗治疗上尿路尿路上皮癌引发间质性肺病的首例病例报告及机制探讨
【字体: 大 中 小 】 时间:2025年07月25日 来源:BMC Pulmonary Medicine 2.6
编辑推荐:
本研究报道了全球首例PD-1抑制剂特瑞普利单抗(toripalimab)联合HER2靶向抗体偶联药物(ADC)维迪西妥单抗(disitamab vedotin)治疗上尿路尿路上皮癌(UTUC)诱发间质性肺病(ILD)的病例。通过多学科诊疗和糖皮质激素冲击疗法成功控制病情,揭示了免疫联合疗法潜在的肺部毒性风险,为临床制定个体化治疗方案提供重要依据。
在肿瘤免疫治疗领域,PD-1抑制剂与抗体药物偶联物(ADCs)的联合应用正掀起新的革命浪潮。然而这场革命背后潜藏着未知的风险――当两种"抗癌利器"强强联手时,它们可能意外激活免疫系统的"双刃剑"效应。上尿路尿路上皮癌(UTUC)作为泌尿系统罕见的"隐匿杀手",仅占尿路上皮癌的5-10%,却以侵袭性强、预后差著称。2025年欧洲泌尿外科学会(EAU)指南虽将PD-1抑制剂联合ADC列为晚期UTUC的一线方案,但关于这种组合疗法安全性的数据仍如"雾里看花"。
成都中医药大学附属医院重症医学科的研究团队在《BMC Pulmonary Medicine》发表的重要病例,首次揭开了这种联合疗法可能引发的"免疫风暴"面纱。该研究报道了一位76岁女性UTUC患者在接受特瑞普利单抗联合维迪西妥单抗治疗后,突发威胁生命的间质性肺病(ILD),通过系列影像学监测和糖皮质激素冲击治疗,最终绘制出从病情恶化到转危为安的完整临床图谱。
研究人员采用多学科协作模式,关键运用了以下技术方法:(1)超声引导下经皮肾穿刺活检确诊UTUC;(2)连续胸部CT动态监测肺部病变;(3)动脉血气分析评估呼吸功能;(4)PD-1抑制剂相关毒性分级系统;(5)高剂量甲基强的松龙脉冲疗法。所有数据均来自该真实世界病例的完整医疗记录。
【病例展示】
通过病理切片和免疫组化染色(
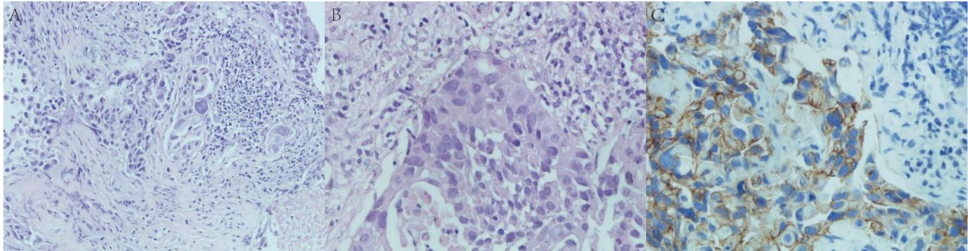
),确诊患者为HER2(3+)阳性UTUC伴多发转移。基线CT显示肺部正常(
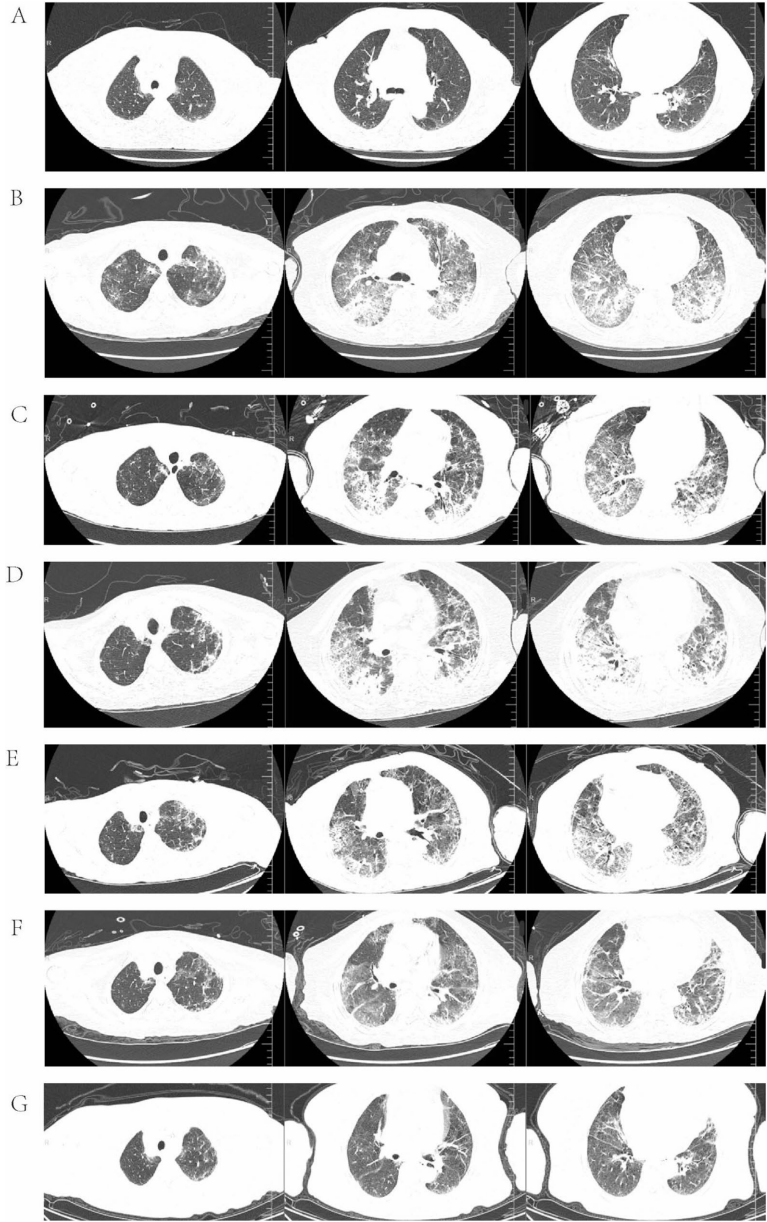
),但联合用药两次后即出现典型ILD影像学改变(
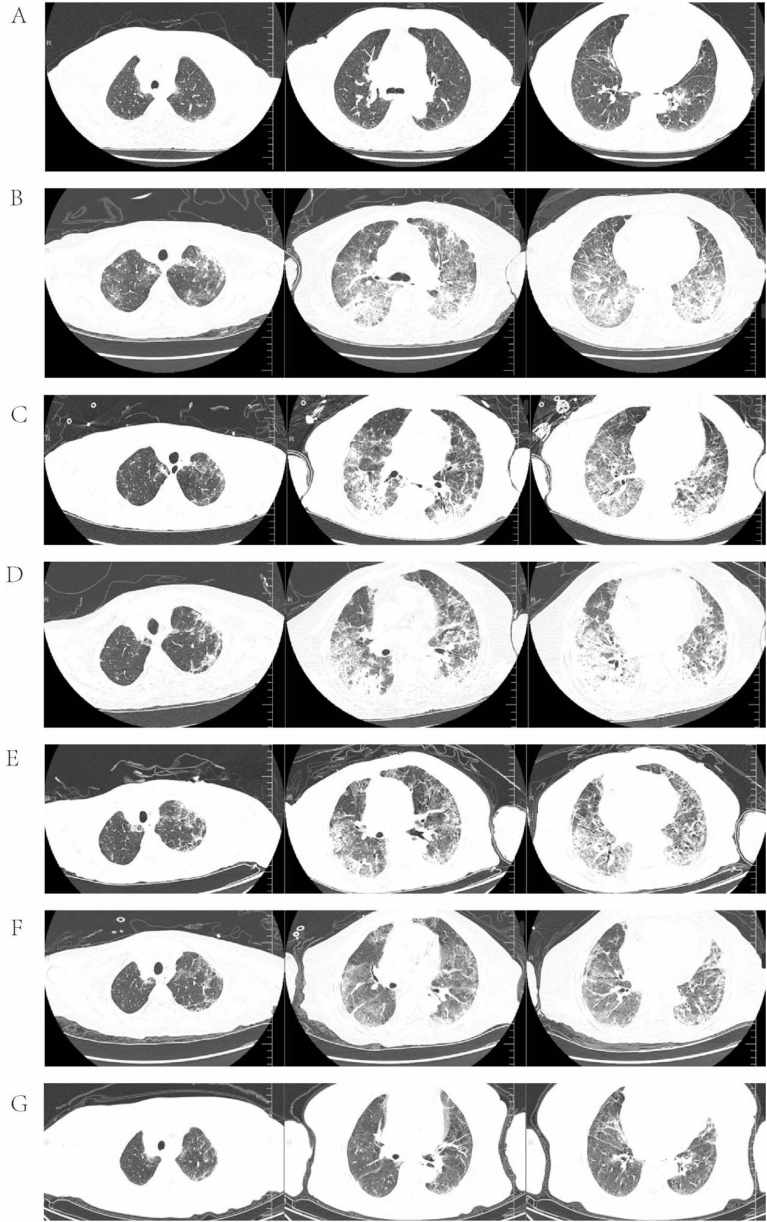
)。
【诊疗过程】
当激素减量导致病情反复时(
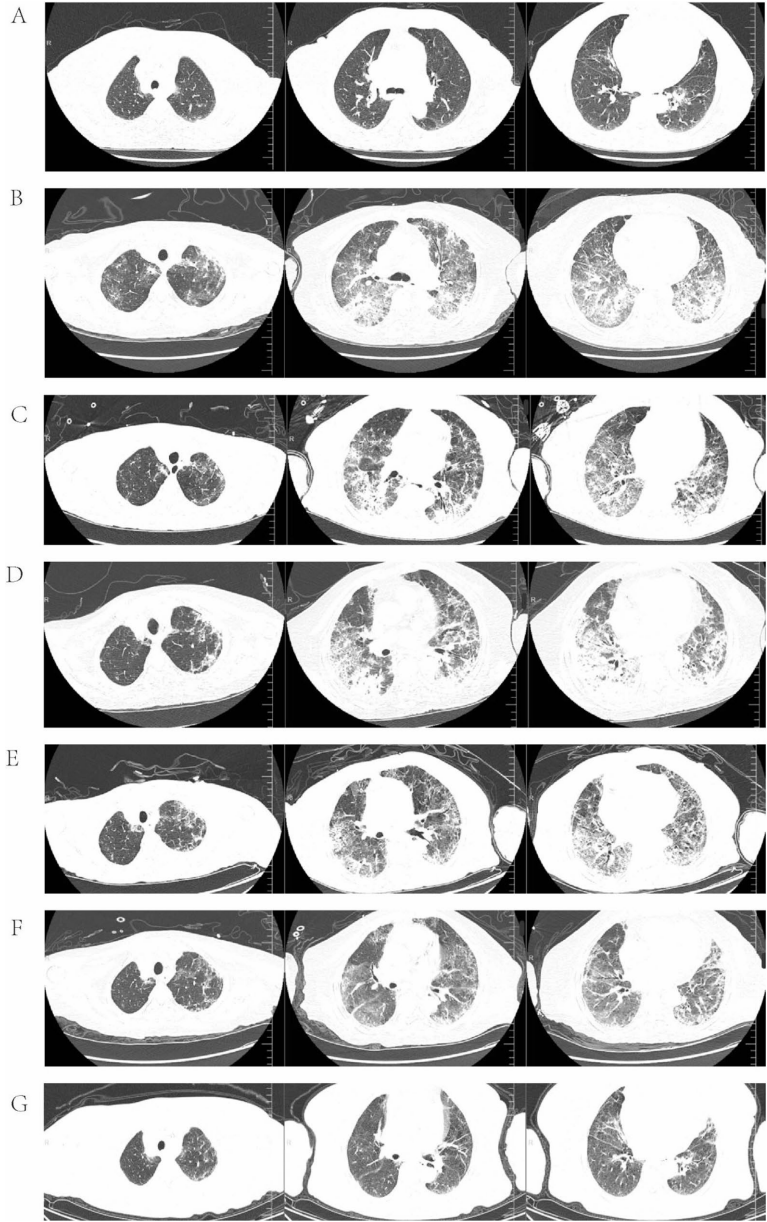
),采用80mg甲基强的松龙联合静脉免疫球蛋白的强化方案,最终实现肺部病变显著吸收(
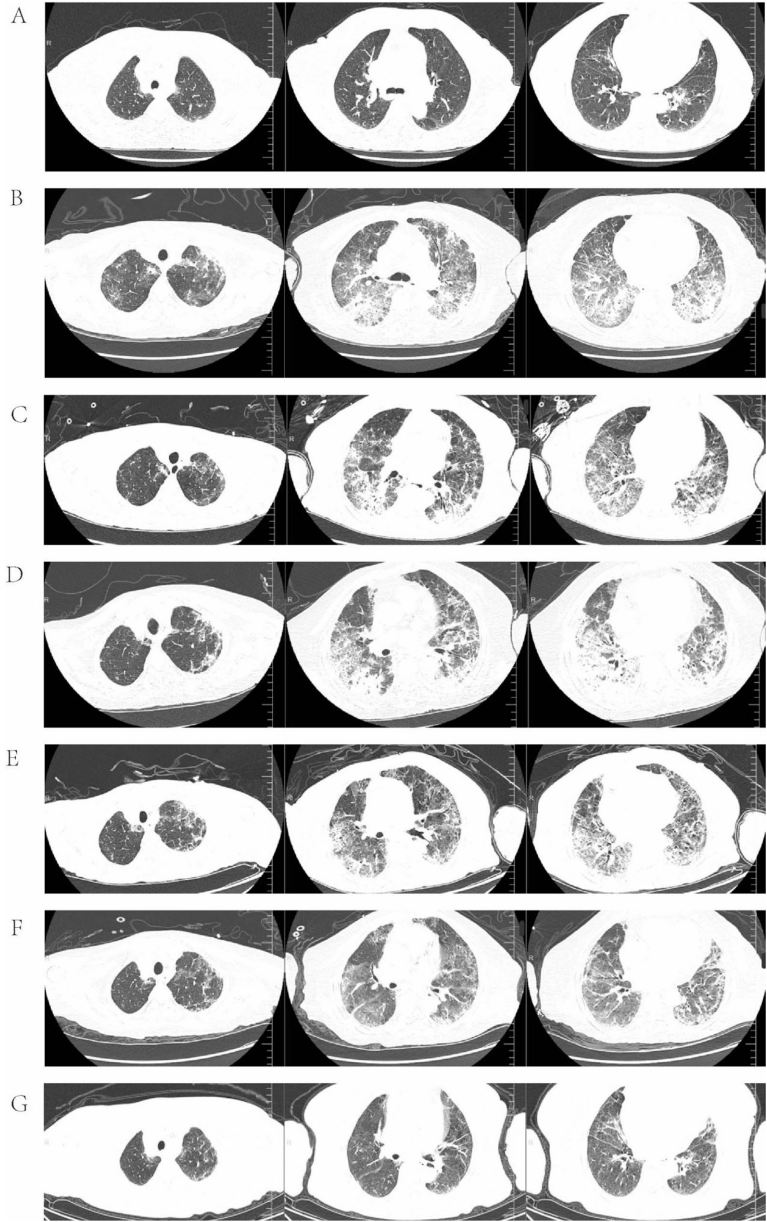
)。
【讨论启示】
该病例揭示了三个关键发现:首先,PD-1抑制剂与ADC联用可能产生协同毒性,通过T细胞过度活化(ICIs作用)和组织直接损伤(ADCs旁观者效应)双重机制诱发ILD;其次,激素骤停易导致病情反弹,提示需要缓慢减量;最后,在停用PD-1抑制剂后继续ADC治疗未再出现不良反应,为临床决策提供重要参考。
这项研究犹如一记警钟,提醒临床医生在追求疗效的同时需警惕"免疫治疗双刃剑"。未来需要建立生物标志物预警系统,平衡肿瘤控制与毒性风险。正如作者Ding P和Lin HH强调的,对高龄UTUC患者实施联合免疫治疗时,必须制定个体化的风险收益评估方案,方能在抗癌道路上行稳致远。
【局限性】
本病例存在以下局限性。首先,作为单例病例,无法确定 ILD 是由 PD -1抑制剂、 ADC 还是两者联合作用引起的;需要更大规模的队列研究来证实因果关系。其次,缺乏药物浓度监测或肺组织活检,限制了我们深入研究潜在机制的能力。第三,患者高龄(76岁)及肺储备功能的潜在下降可能增加了 ILD 的易感性,目前缺乏可靠的生物标志物来预测免疫相关毒性。此外,本病例报告可能存在选择性偏差和回忆性偏差,可能会忽略病情较轻或治疗反应不明显的病例。最后,虽然进行了文献综述,但可能不够详尽或未涵盖最新研究,这可能导致在理解疾病发病机制和最佳治疗策略方面存在差距。这些局限性凸显了开展更全面的研究以更好地阐明这些疗法与 ILD 发展之间的关系的必要性。
 生物通微信公众号
生物通微信公众号
知名企业招聘