
-

生物通官微
陪你抓住生命科技
跳动的脉搏
基于半机制群体药代动力学-药效学模型评估Bitopertin对红细胞生成和血红蛋白合成的下游效应
【字体: 大 中 小 】 时间:2025年07月26日 来源:Journal of Pharmacokinetics and Pharmacodynamics 2.2
编辑推荐:
研究人员针对GlyT1抑制剂Bitopertin可能引发的贫血风险,开发了整合红细胞生成和血红蛋白合成通路的半机制群体PKPD模型。通过分析67名健康受试者120天给药数据,该模型成功量化了Bitopertin对RET、RBC、MCH和IRF等生物标志物的剂量-时间效应,并模拟了四种不同作用机制(A-D)对造血系统的差异化影响,为临床评估药物安全性提供了创新建模框架。
在药物研发过程中,准确评估化合物对造血系统的影响始终是平衡疗效与安全性的关键挑战。红细胞生成(Erythropoiesis)作为维持组织氧供的核心生理过程,其复杂调控机制涉及造血干细胞分化、血红蛋白(Hemoglobin)合成等多阶段通路。GlyT1(Glycine Transporter 1)抑制剂Bitopertin在神经系统疾病研究中意外发现会通过干扰血红蛋白合成导致贫血,这一现象凸显了建立定量预测模型的迫切需求。
为系统评估Bitopertin的造血系统影响,罗氏制药研究与早期开发部门(Roche Pharma Research and Early Development, Pharmaceutical Sciences, Roche Innovation Center Basel, Switzerland)联合乌普萨拉大学的研究团队,在《Journal of Pharmacokinetics and Pharmacodynamics》发表了创新性研究成果。他们利用67名健康受试者为期240天(120天给药+120天随访)的临床试验数据,构建了首个整合红细胞生成全通路的半机制群体PKPD模型,为药物安全性评估提供了新范式。
研究采用多层级技术方法:首先基于Phase 1临床试验队列(62例10-60mg Bitopertin或安慰剂组),采集RET、RBC、MCH、IRF等动态血液学指标;其次建立包含前体细胞(PRE)、网织红细胞(RET)和成熟红细胞(RBC)的四室转运模型,通过SAEM算法估计参数;最后采用VPC验证模型对未参与建模的Hbtot数据的预测能力。
【模型结构】
研究团队扩展了既往血红蛋白周转模型,创新性地将骨髓(橙色)与血液(红色)区室联动建模。核心发现包括:
【机制模拟】
模型成功区分四种药物靶点作用机制:
【模型验证】
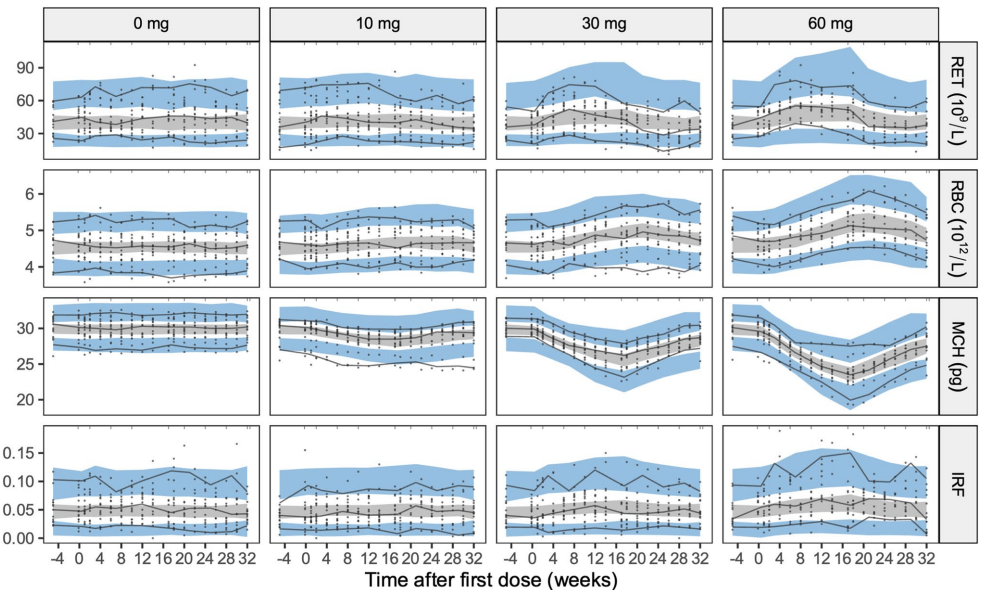
这项研究创建了首个能同时解析红细胞生成动力学和血红蛋白合成的PKPD模型框架,具有三重突破意义:
该研究的局限在于未显式纳入铁代谢通路,且受试者年龄<50岁。未来可通过纳入患者数据进一步验证模型的泛化能力,但其创新性的"机制嵌入+数据驱动"建模思路,已为评估造血系统药物毒性树立了新标准。
 生物通微信公众号
生物通微信公众号
知名企业招聘