
-

ЙъОпНЁ№ЩОў
ЕгДгЧҘЧЎЙъГьҝЖјј
Мш¶ҜөДВцІ«
miR-200јТЧеНЁ№эөчҝШTbx5/Gata4/Mef2c»щТтјББҝУ°ПмРДјЎПё°ы·Ц»ҜУлРДФа·ўУэөД»ъЦЖСРҫҝ
ЎҫЧЦМеЈә ҙу ЦР РЎ Ўҝ КұјдЈә2025Дк07ФВ30ИХ АҙФҙЈәNature Communications 14.7
ұајӯНЖјцЈә
ЎЎЎЎұҫСРҫҝХл¶ФПИМмРФРДФаІЎ(CHD)ЦРЧӘВјТтЧУ(TFs)јББҝГфёРРФОКМвЈ¬НЁ№э№№ҪЁPMIS-miR-200ЧӘ»щТтРЎКуДЈРНЈ¬КЧҙОҪТКҫmiR-200јТЧеНЁ№э°РПтөчҝШTbx5/Gata4/Mef2cөИРДФа·ўУэ№ШјьТтЧУЈ¬О¬іЦРДјЎПё°ы(CMs)·Ц»ҜОИМ¬ЎЈөҘәЛ¶аЧйС§·ЦОц·ўПЦmiR-200cТЦЦЖөјЦВTBX5+ОҙіЙКмCM4Пё°ыИәТміЈА©ФцЈ¬Іў°йЛжNppaөИ°Р»щТтИҫЙ«ЦКҝӘ·ЕРФёДұдЈ¬ОӘПИМмРФРДФаІЎ·ўІЎ»ъЦЖМṩРВјыҪвЎЈ
РДФа·ўУэКЗТ»ёцҫ«ГЬөчҝШөД№эіМЈ¬ЧӘВјТтЧУИзTbx5ЎўGata4әНMef2cөДјББҝК§әв»бөјЦВСПЦШөДПИМмРФРДФаІЎЎЈИ»¶шЈ¬ХвР©№ШјьТтЧУФЪ·ўУэ№эіМЦРөДҫ«И·өчҝШ»ъЦЖЙРІ»ГчИ·ЎЈҪьДкСРҫҝ·ўПЦmicroRNA(miRNA)ФЪЖч№Щ·ўУэЦРЖрЦШТӘөчҝШЧчУГЈ¬ө«miR-200јТЧеФЪРДФа·ўУэЦРөД№ҰДЬИФКЗҝХ°ЧЎЈ
ГА№ъ°®әЙ»ӘҙуС§өДСРҫҝИЛФұНЁ№эҙҙРВөДPMIS(Plasmid-based microRNA Inhibitor System)јјКхЈ¬№№ҪЁБЛМШТмРФТЦЦЖmiR-200aәНmiR-200cөДЧӘ»щТтРЎКуДЈРНЎЈСРҫҝ·ўПЦЈ¬ТЦЦЖХыёцmiR-200јТЧе»бөјЦВЕЯМҘЖЪЦВЛАЈ¬°йЛжРДКТјдёфИұЛр(VSD)әНРДјЎұдұЎөИСПЦШұнРНЎЈөҘәЛ¶аЧйС§(snRNA-seq+ATAC-seq)·ЦОцҪТКҫБЛТ»ёц¶АМШөДTBX5+/Nppa+ОҙіЙКмРДјЎПё°ыИәМе(CM4)Ј¬ХвР©Пё°ыұнПЦіцТміЈөДИҫЙ«ЦКҝӘ·ЕДЈКҪәНЧӘВј»оРФЎЈёГСРҫҝКЧҙОІыГчmiR-200јТЧеНЁ№эҫ«И·өчҝШРДФа·ўУэ№ШјьЧӘВјТтЧУөДјББҝЈ¬О¬іЦРДјЎПё°ыХэіЈ·Ц»ҜҪшіМөД·ЦЧУ»ъЦЖЈ¬Па№ШіЙ№ы·ўұнФЪЎ¶Nature CommunicationsЎ·ЎЈ
СРҫҝІЙУГөДЦчТӘјјКх°ьАЁЈә1)PMISЧӘ»щТтРЎКуДЈРН№№ҪЁЈ»2)ЕЯМҘРДФаЧйЦҜЗРЖ¬әНГвТЯУ«№в·ЦОцЈ»3)өҘәЛ¶аЧйС§ІвРт(snRNA-seqәНATAC-seqБӘәП·ЦОц)Ј»4)RNAЛЩВК·ЦОцФӨІвПё°ы·ўУэ№мјЈЈ»5)SCENIC+Лг·Ё№№ҪЁ»щТтөчҝШНшВзЎЈ
СРҫҝҪб№ы
miR-200јТЧеКЗРДФаФзЖЪ·ўУэөД№ШјьөчҝШТтЧУ
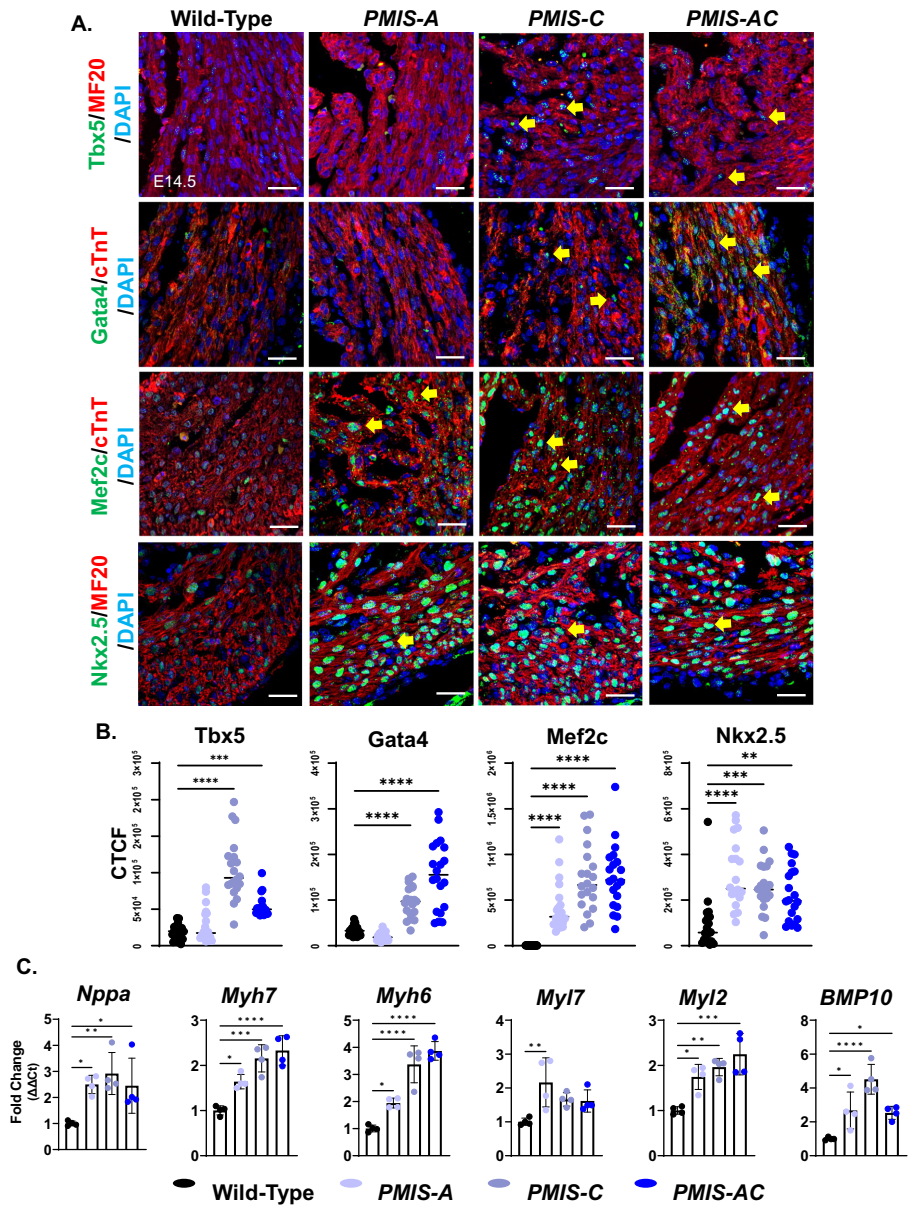
НЁ№эqPCRјмІв·ўПЦmiR-200a/cФЪE12.5-E16.5ЕЯМҘРДФаЦРёЯұнҙпЎЈТЦЦЖХыёцmiR-200јТЧе(PMIS-AC)өјЦВЕЯМҘЖЪЦВЛАЈ¬РДФаіцПЦРДКТјдёфИұЛрәНРДјЎұдұЎөИСПЦШ»ыРОЈ¬АаЛЖУЪTbx5ЗГіэұнРНЎЈWestern blotЦӨКөmiR-200ТЦЦЖөјЦВTbx5ЎўGata4ЎўMef2cәНPitx2ө°°ЧЛ®ЖҪПФЦшЙэёЯЎЈ

ТЦЦЖmiR-200ёДұдРДјЎПё°ыЧӘВјТтЧУұнҙпЖЧ
ГвТЯУ«№вПФКҫPMIS-CәНPMIS-ACРЎКуЧуРДКТРДјЎПё°ыЦРTbx5ұнҙпТміЈЙэёЯЈ¬¶шХэіЈЗйҝцПВTbx5ЦчТӘФЪРД·ҝјЎПё°ыұнҙпЎЈН¬КұјмІвөҪNkx2.5өИ·ЗЦұҪУ°РұкөДұнҙпЙПөчЈ¬ұнГчҙжФЪ№г·әөДЧӘВјЦШұаіМЎЈ
өҘәЛЧӘВјЧй·ЦОцҪТКҫТміЈРДјЎПё°ыИәМе
НЁ№э·ЦОц12,507ёцРДФаПё°ыәЛЈ¬јш¶Ёіц5ёцРДјЎПё°ыСЗИәЎЈPMIS-CРЎКуЦРCM4Пё°ыұИАэПФЦшФцјУ(22.37% vs WT 1.44%)Ј¬ёГИәМеН¬КұұнҙпРД·ҝұкЦҫОпNppaәНРДКТұкЦҫОпTbx5Ј¬RNAЛЩВК·ЦОцұнГчCM4ҙҰУЪ·ўУэФзЖЪЧҙМ¬ЎЈ
ИҫЙ«ЦКҝЙј°РФ·ЦОцҪТКҫTBX5өчҝШНшВз
ATAC-seqПФКҫCM4Пё°ыЦРNppa»щТтЧщИҫЙ«ЦКҝӘ·ЕРФПФЦшФцјУЎЈMotif·ЦОц·ўПЦCM4МШТмРФё»јҜT-boxјТЧеҪбәПО»өгЈ¬SCENIC+Лг·ЁФӨІвTBX5КЗЗэ¶ҜCM4ЧӘВјМШХчөД№ШјьөчҝШТтЧУЎЈ
miR-200cРВ°РұкIrx1өДјш¶Ё
СРҫҝ·ўПЦmiR-200cҝЙЦұҪУ°РПтIrx1өД3'UTRЈ¬PMIS-CРЎКуЦРIrx1ұнҙпЙэёЯЎЈIrx1+Пё°ыФЪ·ўУэФзЖЪё»јҜЈ¬МбКҫЖдҝЙДЬІОУлРДјЎПё°ыіЙКм№эіМөчҝШЎЈ
ҪбВЫУлТвТе
ёГСРҫҝКЧҙОІыГчmiR-200јТЧеНЁ№эҫ«И·өчҝШTbx5өИРДФа·ўУэ№ШјьТтЧУөДјББҝЈ¬О¬іЦРДјЎПё°ыХэіЈ·Ц»ҜҪшіМөД·ЦЧУ»ъЦЖЎЈ·ўПЦОҙіЙКмCM4Пё°ыИәМеөДҙжФЪОӘАнҪвПИМмРФРДФаІЎ·ўІЎМṩБЛРВКУҪЗЎЈPMISјјКхОӘСРҫҝmiRNAјТЧе№ҰДЬМṩБЛРВ№ӨҫЯЈ¬TBX5-miR-200cөчҝШЦбөД·ўПЦОӘРДФаФЩЙъТҪС§СРҫҝҝӘұЩБЛРВЛјВ·ЎЈСРҫҝ»№ҪЁБўБЛРДФа·ўУэЦРЧӘВјТтЧУјББҝГфёРРФЎўmiRNAөчҝШәНұн№ЫТЕҙ«ЦШЛЬЦ®јдөД№ҰДЬБӘПөЈ¬ОӘПИМмРФРДФаІЎөДХп¶ПәНЦОБЖМṩБЛЗұФЪРВ°РөгЎЈ
 ЙъОпНЁОўРЕ№«ЦЪәЕ
ЙъОпНЁОўРЕ№«ЦЪәЕ
ЦӘГыЖуТөХРЖё
ҪсИХ¶ҜМ¬ | ИЛІЕКРіЎ | РВјјКхЧЁАё | ЦР№ъҝЖС§ИЛ | ФЖХ№МЁ | BioHot | ФЖҪІМГЦұІҘ | »бХ№ЦРРД | МШјЫЧЁАё | јјКхҝмС¶ | Гв·СКФУГ
°жИЁЛщУР ЙъОпНЁ
Copyright© eBiotrade.com, All Rights Reserved
БӘПөРЕПдЈә
ФБICPұё09063491әЕ