
-

生物通官微
陪你抓住生命科技
跳动的脉搏
Wolfram综合征患者胰岛移植长期随访研究:揭示β细胞替代疗法在单基因糖尿病中的代谢获益与神经保护困境
【字体: 大 中 小 】 时间:2025年07月31日 来源:Acta Diabetologica 2.9
编辑推荐:
本研究针对Wolfram综合征(WS)这一罕见单基因糖尿病存在的β细胞缺陷和神经退行性病变双重挑战,通过10年随访首次证实胰岛移植在非自身免疫性胰岛素缺乏患者中的长期有效性。意大利San Raffaele医院团队采用双次胰岛输注(总IEQ达593,692)联合CXCR1/2抑制剂reparixin方案,使59岁WS患者实现HbA1c从7.6%显著改善、胰岛素需求降低70%,且低血糖事件从每月3-4次降至1次。研究创新性证明在缺乏胰岛自身抗体(anti-GAD/IA-2/ZnT8阴性)情况下,β细胞替代疗法可获得优于T1D的移植物存活,为干细胞治疗单基因糖尿病提供关键临床证据。
在糖尿病研究领域,Wolfram综合征(WS)犹如一个复杂的医学谜题――这种由WFS1基因突变引发的罕见病,不仅导致儿童期爆发的胰岛素依赖型糖尿病,还伴随着进行性神经退化和多系统衰竭。传统胰岛素治疗虽能控制血糖,却无法阻止β细胞的持续凋亡和神经功能的恶化。更棘手的是,这类非自身免疫性糖尿病患者的胰岛可能面临不同于1型糖尿病(T1D)的生存环境,这为细胞替代疗法带来了全新的科学命题。
意大利米兰San Raffaele医院(IRCCS Ospedale San Raffaele)糖尿病研究所的Davide Catarinella团队,在《Acta Diabetologica》发表了一项历时10年的里程碑式研究。他们追踪了一位59岁WS患者接受胰岛移植后的完整病程,首次揭示:在没有自身免疫攻击(anti-GAD/IA-2/ZnT8抗体持续阴性)的情况下,移植胰岛可展现惊人的长期活力,同时暴露出神经退行性病变与免疫抑制治疗的复杂交互作用。
研究人员采用双次胰岛输注技术(总胰岛当量IEQ达593,692),配合创新性的CXCR1/2信号通路抑制剂reparixin(2.772 mg/kg/h×7天)和常规免疫抑制方案(他克莫司+西罗莫司)。通过动态监测代谢指标、神经功能评估和基因检测,构建了WS多系统病变的完整演化图谱。
代谢控制方面,移植后数据显示:空腹C肽从检测不到升至稳定水平(0.8-1.2 ng/mL),胰岛素需求从0.29 IU/kg降至0.09 IU/kg,HbA1c维持在6.5%以下。尤为关键的是,严重低血糖事件从每月3-4次锐减至每年12次,证实β细胞替代能根本性改善WS的"脆性糖尿病"特征。
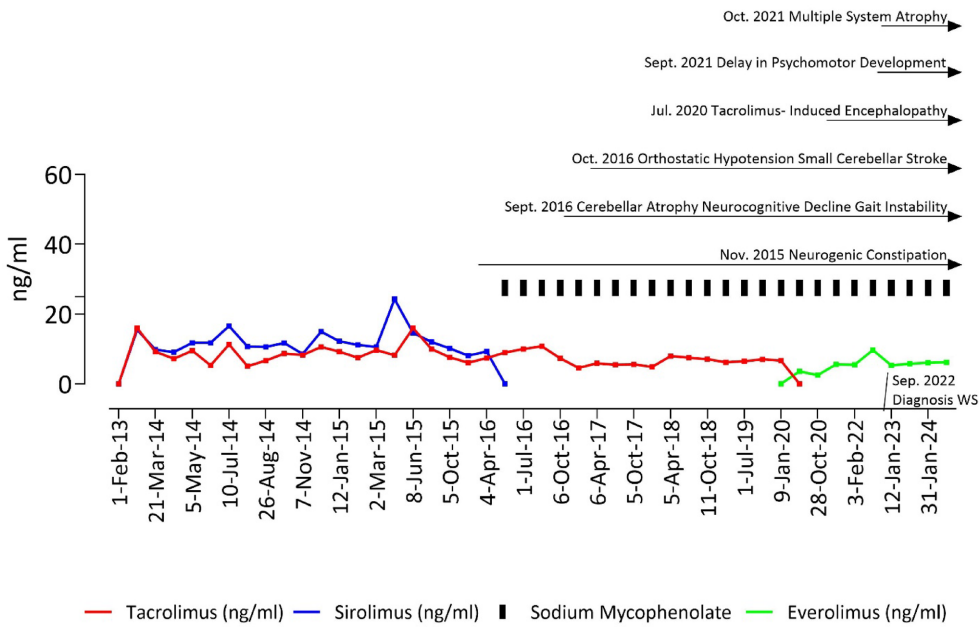
神经病变进展却呈现矛盾现象:尽管代谢控制改善,患者仍出现小脑萎缩、自主神经功能障碍和认知下降。脑MRI显示桥脑小脑区萎缩,神经心理学评估发现前向记忆(MMSE 26/30)和执行功能损伤。值得注意的是,免疫抑制剂转换(他克莫司→依维莫司)未能缓解症状,提示神经退化可能独立于药物毒性,是WS固有的病理过程。
遗传诊断转折:移植后7年,基因检测发现WFS1基因c.1839G>A(p.Trp613*)杂合突变,最终修正诊断为典型WS。这一发现解释了两个关键现象:①患者糖尿病史长达43年却缺乏胰岛自身抗体;②其神经病变模式符合WS特征而非单纯糖尿病并发症。
这项研究具有三重突破意义:首先,它首次证明胰岛移植在非自身免疫性胰岛素缺乏症中的长期有效性,为单基因糖尿病开辟了细胞治疗新路径;其次,揭示WS患者胰岛可能具有独特的生存优势――没有自身免疫攻击的环境使移植胰岛存活时间(>10年)超过多数T1D案例;最后,提出代谢控制与神经保护的不平行改善这一关键科学问题,为未来联合治疗策略指明方向。
随着干细胞技术发展,该案例更具前瞻性启示:WS患者的非自身免疫背景可能使其成为干细胞衍生胰岛(SC-islets)治疗的理想对象。研究者特别指出,未来采用基因校正的自体iPSC(诱导多能干细胞)可能进一步规避免疫排斥风险,实现真正的病因治疗。
这项跨越十年的医学追踪,不仅改写了WS的治疗范式,更重塑了人们对β细胞替代疗法适用范围的认知――当糖尿病源于β细胞"内乱"而非免疫系统"误攻"时,细胞治疗或许能创造更大的生命奇迹。
 生物通微信公众号
生物通微信公众号
知名企业招聘