
-

ЙъОпНЁ№ЩОў
ЕгДгЧҘЧЎЙъГьҝЖјј
Мш¶ҜөДВцІ«
Ҫб№№ЗчН¬УлЛ®ҪйөјөДөЧОпДЈДвКөПЦИЛАаҝ№Ме¶ФЙсҫӯ°ұЛбГёөД№г·әТЦЦЖ
ЎҫЧЦМеЈә ҙу ЦР РЎ Ўҝ КұјдЈә2025Дк08ФВ02ИХ АҙФҙЈәNature Communications 15.7
ұајӯНЖјцЈә
ЎЎЎЎұҫСРҫҝХл¶ФБчёРІЎ¶ҫЙсҫӯ°ұЛбГё(NA)ұЈКШҙЯ»ҜО»өгЈ¬ҝӘ·ўБЛ№гЖЧЦРәНҝ№МеNCS.1.xПөБРЎЈНЁ№эОИ¶Ё»ҜNAМҪХл(sNAps)·ЦАлјЗТдBПё°ыЈ¬ҪбәПАд¶іөзҫөјјКхҪвОцҝ№Ме-ҝ№ФӯёҙәПОпҪб№№Ј¬·ўПЦЖдНЁ№эAsp-Arg»щРтәНЛ®·ЦЧУНшВзДЈДвНЩТәЛбөЧОпҪбәПДЈКҪЈ¬КөПЦ¶ФH1N1ЎўH5N1ј°BРНБчёРІЎ¶ҫөДҪ»ІжұЈ»ӨЎЈёГСРҫҝОӘУҰ¶ФёЯЦВІЎРФЗЭБчёРH5N1өДИ«ЗтБчРРМṩБЛРВРНЦОБЖІЯВФЈ¬·ўұнУЪЎ¶Nature CommunicationsЎ·ЎЈ
БчёРІЎ¶ҫИзН¬ЧФИ»ҪзЧоҪЖ»«өДұдРОХЯЈ¬ГҝДкНЁ№эҝ№ФӯЖҜТЖәНЦШЧйТэ·ўјҫҪЪРФБчРРЈ¬¶шёЯЦВІЎРФЗЭБчёРH5N1ёьұ»КАҪзОАЙъЧйЦҜБРОӘЧоҫЯҙуБчРРЗұБҰөДНюРІЎЈҫЎ№ЬХл¶ФСӘДэЛШ(HA)өД№гЖЧЦРәНҝ№Ме(bnAbs)ФшҙшАҙПЈНыЈ¬ө«ҪьЖЪVIR-2482өИәтСЎТ©ОпөДБЩҙІКФСйК§°Ьұ©В¶іцЖдҫЦПЮРФЎӘЎӘ¶ФAРНБчёРІЎ¶ҫЦРGroup 2 HAСЗРНөДТЦЦЖР§БҰІ»ЧгЎЈХвҙЩК№ҝЖС§јТҪ«Дҝ№вЧӘПтІЎ¶ҫұнГжБнТ»ёц№Шјьө°°ЧЈәЙсҫӯ°ұЛбГё(NA)ЎЈ
ГА№ъ№ъБўОАЙъСРҫҝФәТЯГзСРҫҝЦРРД(Vaccine Research Center, National Institutes of Health)өДJulia LederhoferНЕ¶УБӘәП»ӘКў¶ЩҙуС§ө°°ЧЦКЙијЖСРҫҝЛщ(Institute for Protein Design, University of Washington)өДСРҫҝИЛФұЈ¬ФЪЎ¶Nature CommunicationsЎ··ўұнБЛТ»ПоН»ЖЖРФСРҫҝЎЈЛыГЗҙУH3N2ҝөёҙХЯМеДЪ·ЦАліцДЬН¬Кұ°РПтA/BРНБчёРNAҙЯ»ҜО»өгөДҝ№МејТЧеNCS.1.xЈ¬НЁ№эАд¶іөзҫөјјКхКЧҙОҪТКҫХвР©ҝ№МеИзәОАыУГ"Л®·ЦЧУЗЕБә"КөПЦҝзСЗРНұЈ»ӨЈ¬ОӘУҰ¶ФөұЗ°H5N1И«ЗтЗЭРуТЯЗйМṩБЛИ«РВҪвҫц·Ҫ°ёЎЈ
СРҫҝНЕ¶УФЛУГИэПоәЛРДјјКхЈә1) јЖЛг»ъЙијЖөДОИ¶Ё»ҜNAЛДҫЫМе(sNAps)ЧчОӘМҪХлЈ¬ҙУҝөёҙХЯНвЦЬСӘөҘәЛПё°ы(PBMCs)ЦР·ЦСЎјЗТдBПё°ыЈ»2) 2.29?і¬ёЯ·ЦұжВКАд¶іөзҫөҪвОцҝ№Ме-NAёҙәПОпҪб№№Ј»3) ҪЁБў°ьә¬H5N1 clade 2.3.4.4bөИБчРРЦкөДІЎ¶ҫТЦЦЖМеПө(IRINA/ELLA)ЎЈ
ҝ№Ме·ўПЦУлМШХчјш¶Ё
НЁ№э·ЗБчРРСЗРНN4/N5 NAМҪХлЈ¬СРҫҝХЯҙУөҘёц№©Ме·ЦАліцХјBПё°ыҝв50%ТФЙПөДҝЛВЎјТЧеNCS.1.xЎЈХвР©ҝ№МеДЬҪбәПH1N1ЎўH5N1ј°BРНVictoriaЖЧПөІЎ¶ҫNAЈ¬ө«¶ФGroup 2СЗРНИзN2ҪбәПҪПИхЎЈ¶АМШөДIGHV4-31 * 03/IGKV2-28 * 01»щТтК№УГәННкИ«Т»ЦВөДCDRH3РтБР°өКҫЖд·ўУэ№мјЈёЯ¶ИұЈКШЎЈ
Ҫб№№ЙъОпС§Н»ЖЖ
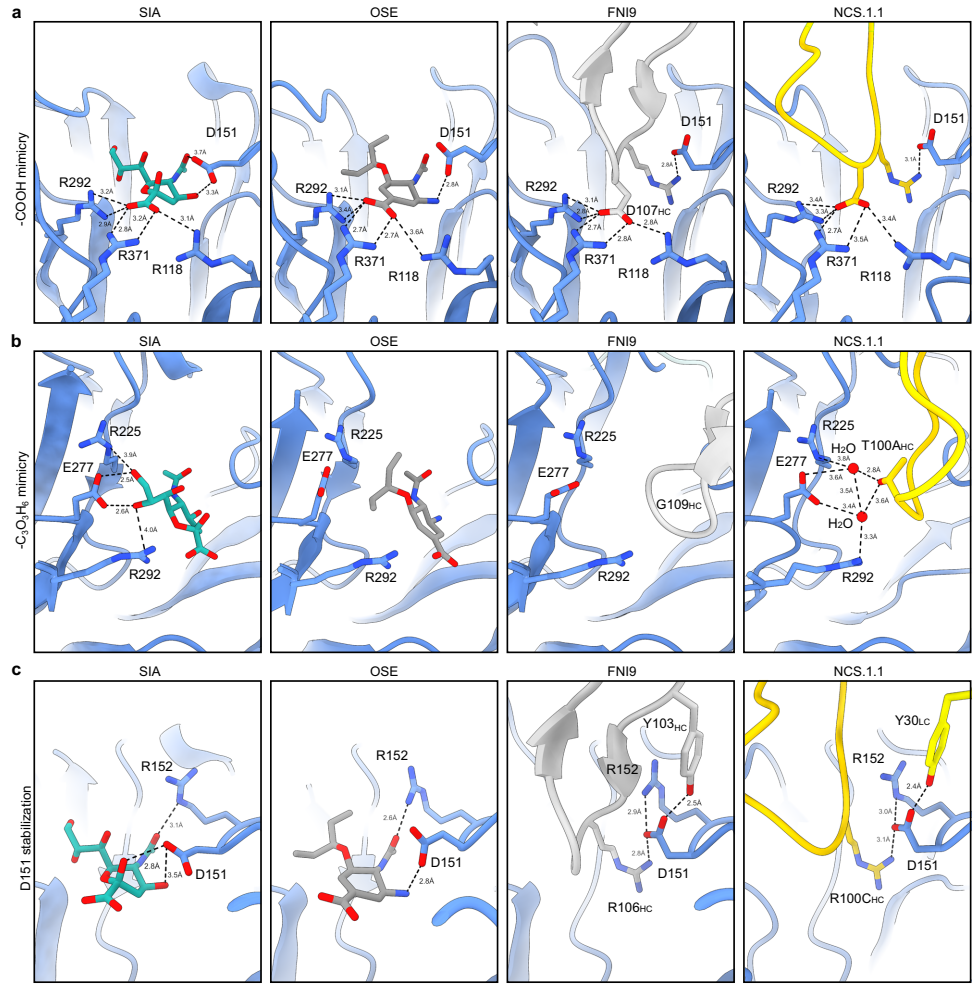
Ад¶іөзҫөҪб№№ПФКҫNCS.1.1НЁ№эCDRH3өДAsp-Arg(D100BHC-R100CHC)»щРтІеИлNAҙЯ»ҜҝЪҙьЈ¬УлR118NAЎўR293NAРОіЙАлЧУНшВзЎЈёьҫӘИЛөДКЗЈ¬БҪёцЛ®·ЦЧУҫ«И·ДЈДвБЛНЩТәЛбC8/C9фЗ»щөДҝХјдО»ЦГЈ¬ХвЦЦ"Л®ҪйөјөДЛшФҝҪбәП"»ъЦЖФЪ3.36?өДN5-DB16ёҙәПОпҪб№№ЦРөГөҪСйЦӨЎЈ
№ҰДЬРФСйЦӨ
ФЪІЎ¶ҫТЦЦЖКФСйЦРЈ¬NCS.1.x¶ФH5N1 clade 2.3.4.4b(CH23/TX24Цк)өД°лКэТЦЦЖЕЁ¶И(IC50)ҙпҰМg/mlј¶Ј¬Улҫӯөдҝ№Ме1G01ПаөұЎЈ¶ҜОпКөСйПФКҫЈ¬10 mg/kgјББҝПВNCS.1.1¶ФH1N1№Ҙ»чМṩНкИ«ұЈ»ӨЈ¬¶ФҪьЖЪұ¬·ўөДДМЕЈФҙH5N1(өВЦЭЦк)ТІДЬСУіЩ·ўІЎКұјд4МмЎЈ
ХвПоСРҫҝҪТКҫБЛҝ№МеНЁ№эҪб№№ЗчН¬Ҫш»Ҝ°РПтNAұЈКШО»өгөДИ«РВ»ъЦЖЈә1) ҝзОпЦЦұЈКШөДAsp-Arg/Arg-Asp»щРтЈ»2) Л®·ЦЧУҪйөјөД№№ПуҝЙЛЬРФЈ»3) ЗбБҙРӯН¬ОИ¶ЁҙЯ»ҜІР»щD151NAЎЈПаҪПУЪРЎ·ЦЧУТЦЦЖјБИз°ВЛҫЛыОӨ(OSE)Ј¬ХвАаҝ№МеҫЯУРёьіӨ°лЛҘЖЪәНёьУЕЧйЦҜ·ЦІјЈ¬МШұрККәПёЯОЈИЛИәФӨ·АЎЈЛжЧЕH5N1ФЪІёИй¶ҜОпјдҙ«ІҘДЬБҰФцЗҝЈ¬ёГСРҫҝОӘҝӘ·ў"NA+HA"Л«°РөгТЯГз/ҝ№МеЧйәПМṩБЛАнВЫТАҫЭЈ¬ҝЙДЬёДұдОҙАҙБчёРҙуБчРРөДУҰ¶Ф·¶КҪЎЈ
 ЙъОпНЁОўРЕ№«ЦЪәЕ
ЙъОпНЁОўРЕ№«ЦЪәЕ
ЦӘГыЖуТөХРЖё
ҪсИХ¶ҜМ¬ | ИЛІЕКРіЎ | РВјјКхЧЁАё | ЦР№ъҝЖС§ИЛ | ФЖХ№МЁ | BioHot | ФЖҪІМГЦұІҘ | »бХ№ЦРРД | МШјЫЧЁАё | јјКхҝмС¶ | Гв·СКФУГ
°жИЁЛщУР ЙъОпНЁ
Copyright© eBiotrade.com, All Rights Reserved
БӘПөРЕПдЈә
ФБICPұё09063491әЕ