
-

生物通官微
陪你抓住生命科技
跳动的脉搏
卢旺达如何在马尔堡病毒疫情爆发10天内启动研究性疫苗的快速响应
《npj Vaccines》:How Rwanda mounted a research response with an investigational vaccine just ten days into a Marburg outbreak
【字体: 大 中 小 】 时间:2025年08月02日 来源:npj Vaccines 6.5
编辑推荐:
本文记录了卢旺达在2024年9月马尔堡病毒病(MVD)疫情爆发后,仅用10天即启动cAd3-Marburg疫苗的II期开放标签临床试验的突破性实践。研究团队通过"百日使命"(100DM)框架整合政府、CEPI、Sabin等多方资源,验证了在突发疫情中并行推进疫苗研发、伦理审查与临床试验的可行性,为全球突发传染病防控提供了"速度+科学"的范本。
2024年9月,卢旺达首次报告马尔堡病毒病(MVD)疫情,这个致死率高达88%的丝状病毒迅速引发全球关注。与传统疫情响应不同,卢旺达政府创造了一项纪录――从疫情宣布到启动研究性疫苗临床试验仅用10天,这背后是名为"百日使命"(100DM)的流行病防控创新框架在发挥作用。
疫情爆发前,卢旺达卫生部(MoH)已与CEPI、BioNTech等机构建立"百日使命"合作伙伴关系,并于2024年9月11日刚完成裂谷热病毒模拟演练。当9月27日确诊首例MVD病例后,卢旺达生物医学中心(RBC)立即启动多线并行机制:一方面采用WHO核心协议(Solidarity CORE)进行应急备案,另一方面根据疫情特点调整试验设计――放弃操作复杂的环形疫苗接种,转为对1700名医护人员和高风险接触者实施开放标签II期试验。
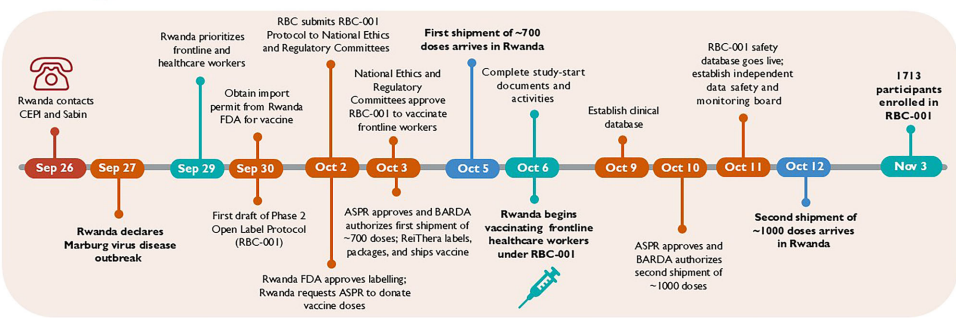
关键技术支持包括:1) 采用Sabin研究所开发的黑猩猩腺病毒3型载体疫苗(cAd3-Marburg),该疫苗已在美国和非洲完成I期试验;2) 通过CEPI协调快速获取意大利ReiThera公司生产的临床批次疫苗;3) 卢旺达FDA与伦理委员会同步审查机制;4) IQVIA提供的临床试验质量管理系统。
研究结果显示:1) 响应速度突破:从9月27日疫情宣布到10月6日首例接种仅10天,刷新疫苗应急响应纪录;2) 操作模式创新:建立"政府主导-企业协同"的伙伴关系,其中RBC作为试验申办方,Sabin提供疫苗,IQVIA承担CRO职能;3) 接种规模可观:截至10月底完成1700人接种,主要覆盖医护人员和确诊病例接触者;4) 安全监测体系:通过移动接种点和既有医疗网络实现高效随访。
该研究的里程碑意义在于:首次验证了"百日使命"框架在真实疫情中的可行性,证明通过预置合作伙伴关系、并行流程设计和灵活试验方案,能大幅缩短疫苗研发周期。尽管非随机设计限制了效力评估,但为今后应对突发疫情提供了可复制的"快速研究响应"模板。正如作者Sabin Nsanzimana强调的,这种成功依赖于三个核心要素:预存的候选疫苗、高度协调的伙伴关系,以及政府对科学决策的坚定支持。
论文发表于《npj Vaccines》时,研究团队特别指出:当前MVD疫苗研发面临的核心矛盾是疫情规模小难以开展随机对照试验(RCT),而本次1700人规模的II期试验虽无法解决效力证据问题,但建立的快速响应机制对未来更大规模疫情具有重要借鉴价值。随着BioNTech卢旺达mRNA疫苗工厂的建成,该国将具备更完整的疫苗研发-生产链条,为全球传染病防控贡献"非洲方案"。
 生物通微信公众号
生物通微信公众号