
-

生物通官微
陪你抓住生命科技
跳动的脉搏
综述:哮喘的全面解析:流行病学、表型、病理生理学及新兴疗法的综述
【字体: 大 中 小 】 时间:2025年08月03日 来源:The Egyptian Journal of Bronchology 1.0
编辑推荐:
这篇综述系统梳理了哮喘(asthma)的流行病学特征、临床表型(phenotypes)、病理生理机制(如Th2/Th17通路)及个体化治疗策略。文章重点探讨了嗜酸性(eosinophilic)与中性粒细胞性(neutrophilic)哮喘的免疫差异,强调生物制剂(如抗IL-5/IL-4/13)对重症哮喘的突破性疗效,并指出肥胖(obesity)、GERD等共病对疾病管理的挑战。推荐临床采用表型导向(phenotype-based)策略,结合数字监测工具(如ACT/HADS量表)优化诊疗。
哮喘作为古老的呼吸系统疾病,其认知从希波克拉底时代延续至今。全球约2.6亿患者受困于这种以慢性气道炎症、支气管高反应性(BHR)和可变性气流阻塞为特征的异质性疾病。流行病学数据显示欧洲发病率约6%,而美国年经济负担高达819亿美元。值得注意的是,女性在35岁后患病率比男性高20%,且非过敏性哮喘占比超60%,凸显性别差异的临床意义。
哮喘的复杂表型可通过四大维度解析:
临床分型:运动诱发性支气管收缩(EIB)常见于运动员,其"渗透理论"认为气道脱水激活肥大细胞;职业性哮喘(OA)中,低分子量物质(如异氰酸盐)与高分子量物质(如动物蛋白)分别引发速发/迟发反应;重症哮喘(占5-10%)对高剂量ICS反应不佳,需区分"难治性"与"依从性不足";哮喘-慢阻肺重叠综合征(ACOS)患者住院风险增加2倍,符合"荷兰假说"的共病机制。
触发因素:过敏性(IgE介导)与非过敏性哮喘在发病年龄、炎症标志物(如FeNO)及治疗反应上存在显著差异。
病理机制:嗜酸性(T2-high)表型以IL-5/IL-13驱动为特征,对抗IL-5生物制剂(如美泊利单抗)敏感;中性粒细胞(T2-low)表型则与IL-17/TNF-α相关,对糖皮质激素抵抗。
疾病程度:GINA指南按症状频率分为间歇性至持续性四级,其中重度持续型患者FEV1常低于60%预计值。
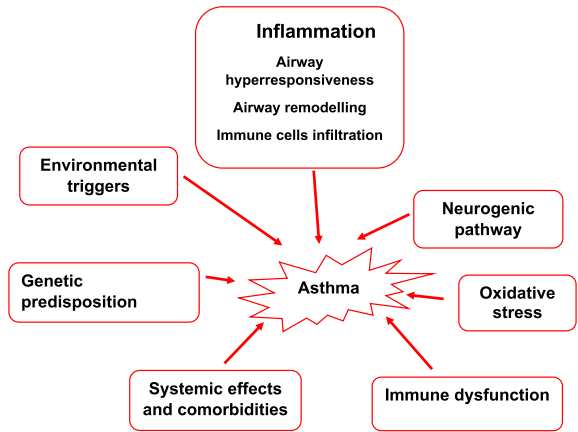
免疫轴:Th2细胞通过IL-4/IL-13促进IgE生成,而IL-5招募嗜酸性粒细胞引发组织损伤;Th17则通过IL-17激活中性粒细胞浸润。
氧化应激:活性氧(ROS)通过NF-κB通路放大炎症,同时破坏抗氧化防御系统。
神经调节:P物质(substance P)与降钙素基因相关肽(CGRP)直接诱发支气管收缩,并增强血管通透性。
遗传易感:ADAM33和丝聚蛋白(filaggrin)基因多态性与气道重塑相关。
40%患者合并焦虑/抑郁,HADS量表评分与急性发作次数正相关。GERD通过迷走神经反射加重症状,但PPI对无症状者无效(证据等级B)。肥胖患者脂肪组织分泌的IL-6可提升气道高反应性,体重减轻5%即能改善肺功能。
SYGMA试验证实布地奈德/福莫特罗较SABA降低64%急性发作。靶向治疗中,度普利尤单抗(抗IL-4/13)对FeNO>25ppb且血嗜酸粒细胞>150/μL患者最有效(FEV1提升320ml)。非药物干预如呼吸训练(膈肌呼吸法)可使ACT评分提高3分。
数字医疗(如AI症状监测)与内型特异性生物标志物(如IL-33)研发将成为精准医学的关键。当前亟需头对头比较生物制剂的RCT研究,并探索微生物组-环境互作对疾病修饰的影响。
 生物通微信公众号
生物通微信公众号
知名企业招聘