
-

生物通官微
陪你抓住生命科技
跳动的脉搏
EGLN1在结直肠癌中的预后价值与免疫微环境调控机制的多组学解析
【字体: 大 中 小 】 时间:2025年08月04日 来源:Discover Oncology 2.9
编辑推荐:
本研究针对结直肠癌(CRC)预后标志物匮乏的临床难题,通过生物信息学与实验验证相结合的策略,首次系统揭示了缺氧诱导因子脯氨酰羟化酶EGLN1在CRC中的肿瘤抑制功能。研究人员利用TCGA、GEO等多组学数据,结合体外功能实验,证实EGLN1低表达与CRC不良预后显著相关,其通过调控HIF-1信号通路、免疫检查点分子(如PDCD1)及肿瘤微环境免疫细胞浸润(如中性粒细胞、NK细胞)发挥抑癌作用。该发现为CRC提供了新的预后标志物和潜在治疗靶点。
在恶性肿瘤的诊疗战场上,结直肠癌始终是威胁人类健康的顽固敌人。据统计,2023年仅美国就有15.3万新发病例和5.2万死亡病例,晚期患者五年生存率不足15%。面对这一严峻形势,科学家们一直在寻找能精准预测预后和指导治疗的新型生物标志物。其中,缺氧诱导因子(HIF)通路因其在肿瘤代谢重编程中的核心作用备受关注,而作为该通路关键调控因子的EGLN1(又称PHD2),却在结直肠癌领域笼罩着重重迷雾――它究竟是助纣为虐的"帮凶",还是守护基因组的"卫士"?
广西医科大学附属贵港市人民医院和广西医科大学肿瘤医院的研究团队在《Discover Oncology》发表的重要研究,首次通过多维度解析揭开了EGLN1在结直肠癌中的神秘面纱。研究人员整合TCGA、GEO等6大公共数据库的组学数据,结合湿实验验证,构建了从分子机制到临床价值的完整证据链。
研究主要采用生物信息学分析(包括差异表达分析、GSEA、ESTIMATE和CIBERSORT算法)结合体外功能实验(稳定敲低细胞系构建、克隆形成和划痕实验)的技术路线。关键数据来源于GSE39582(训练集,n=566)、TCGA-COAD(验证集)和GSE14333(验证集)队列,蛋白质水平验证采用CPTAC数据集。
3.1 EGLN1在正常与肿瘤组织中的差异表达
研究发现EGLN1在CRC组织中的mRNA和蛋白水平均显著低于正常组织(p<0.0001),ROC曲线下面积达0.955,展现出优异的诊断效能。这种表达差异在配对样本分析中同样显著,提示EGLN1可能具有组织特异性抑癌功能。
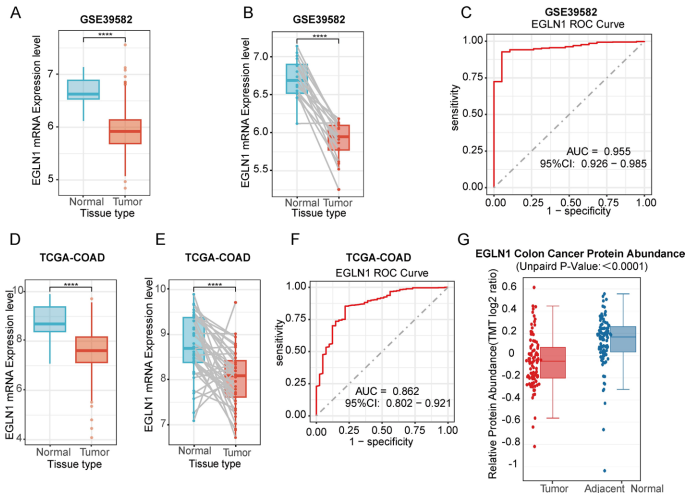
3.2 EGLN1与临床特征的关系
低EGLN1表达组中晚期(III-IV期)患者比例更高(52% vs 42%,p=0.018),且与pMMR(错配修复正常)和CIN+(染色体不稳定)显著相关(p<0.001)。这种特征分布提示EGLN1低表达可能促进基因组不稳定性,加速肿瘤进展。
3.3 功能富集分析
对825个差异基因的分析显示,EGLN1主要富集于抗原呈递、氧应激反应等生物学过程,其分子功能涉及CXCR趋化因子受体结合、MAPK酪氨酸磷酸酶活性等。KEGG分析揭示HIF-1、B细胞受体等关键通路被显著激活,这些通路与肿瘤免疫逃逸密切相关。
3.4 EGLN1与免疫标志物的相关性
研究发现EGLN1与免疫刺激分子(CD86、IL-6)正相关,而与抑制性检查点PDCD1(PD-1)负相关(r=-0.26)。更令人振奋的是,EGLN1高表达组中免疫评分显著升高(p<0.001),中性粒细胞和活化NK细胞浸润增加,而Treg细胞减少,这种免疫微环境特征与更好的临床预后相符。
3.6 预后分析
生存分析显示EGLN1高表达组无复发生存期(RFS)显著延长(HR=0.477,p=0.006),多因素分析证实其独立预后价值(HR=0.583,p=0.045)。Nomogram预测模型C-index达0.669,为临床决策提供了量化工具。
3.7 EGLN1敲低促进肿瘤恶性行为
功能实验为机制研究画上点睛之笔:稳定敲低EGLN1的RKO细胞增殖能力提升2.1倍(p<0.001),迁移速度加快40%,从实验角度验证了其抑癌功能。
这项研究首次系统阐明了EGLN1在结直肠癌中的多层面作用:既是可靠的预后标志物,又是免疫微环境的"调控开关",更是抑制肿瘤进展的"分子刹车"。其创新性体现在三方面:① 发现EGLN1表达与pMMR/CIN+的特殊关联,为理解基因组不稳定性提供了新视角;② 揭示EGLN1通过CXCL10-CCR1等轴
 生物通微信公众号
生物通微信公众号
知名企业招聘