
-

生物通官微
陪你抓住生命科技
跳动的脉搏
利用高度适应性Barnase-Barstar系统实现埃及伊蚊遗传生物防治新突破
【字体: 大 中 小 】 时间:2025年08月06日 来源:Communications Biology 5.1
编辑推荐:
本研究针对埃及伊蚊(Ae. aegypti)传播登革热等疾病的防控难题,创新性地将源自解淀粉芽孢杆菌(Bacillus amyloliquefaciens)的毒素-解毒剂系统Barnase-Barstar(Bn-Bs)应用于蚊虫遗传控制。研究人员通过细胞实验和转基因蚊构建,证实Bn可在埃及伊蚊中诱导组织特异性致死效应,而Bs能有效挽救该毒性,为开发基于毒素-解毒剂对的基因驱动系统(如Killer-Rescue和underdominance系统)提供了新型分子工具。该成果发表于《Communications Biology》,为蚊媒疾病防控提供了可调控的遗传控制策略。
在全球气候变化和杀虫剂抗性加剧的背景下,埃及伊蚊(Aedes aegypti)作为登革热、寨卡病毒和黄热病的主要传播媒介,其防控形势日益严峻。传统控制方法面临地理范围扩大和抗药性产生的双重挑战,亟需开发新型防控策略。虽然基于Wolbachia共生菌、不育昆虫技术(SIT)和归巢核酸内切酶基因驱动系统已取得进展,但这些方法在持久性、侵入性和社区接受度方面存在局限。特别是需要一种既能长期维持又不会向周边种群扩散的"局部基因驱动"系统,其中基于负向杂种优势(underdominance)的设计尤为引人关注。
英国皮尔布赖特研究所(The Pirbright Institute)的Katherine Nevard等研究人员创新性地将细菌源性的毒素-解毒剂对Barnase-Barstar(Bn-Bs)系统引入蚊虫遗传控制领域。Barnase是一种细胞外核糖核酸酶(110个氨基酸),Barstar(89个氨基酸)是其特异性抑制剂,二者在解淀粉芽孢杆菌中天然存在,具有结合亲和力高、分子量小且无需辅因子等特点。研究人员通过埃及伊蚊细胞系(Aag2)实验和转基因蚊构建,系统评估了该系统的适用性,相关成果发表在《Communications Biology》期刊。
研究采用的主要技术包括:1) 质粒转染Aag2细胞评估Bn毒性和Bs挽救效应;2) 构建含PUb-Bs-TRE-Bn的转基因埃及伊蚊品系;3) 利用组织特异性启动子(AeAct4驱动间接飞行肌表达、AeCPA驱动中肠表达)研究Bn的时空效应;4) 通过飞行能力测试和生育力分析评估表型;5) 使用Cre/loxP系统分离双转基因元件。
研究结果部分显示:
【Bn在Aag2细胞中具有致死性且可被Bs挽救】
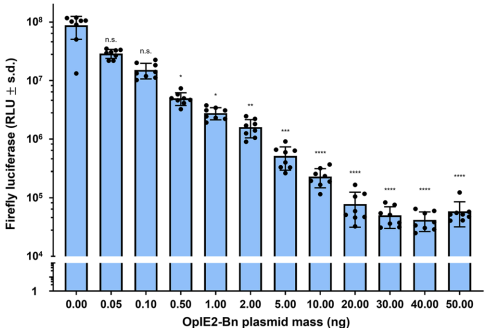
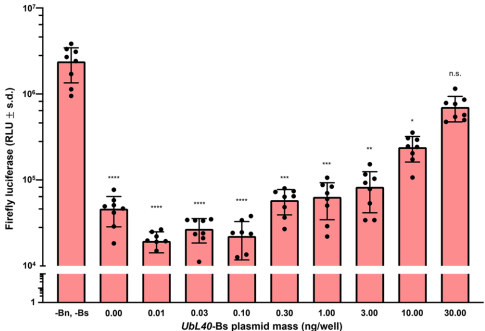
转染实验表明,OpIE2启动子驱动的Bn表达导致萤火虫荧光素酶(PUb-Fluc)活性剂量依赖性下降,而UbL40启动子表达的Bs能剂量依赖性地逆转该效应。
【转基因蚊中Bn表达导致组织特异性表型】
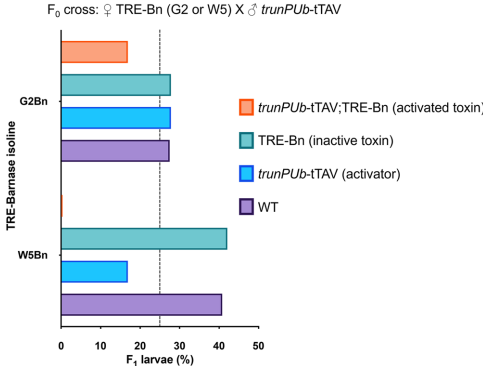
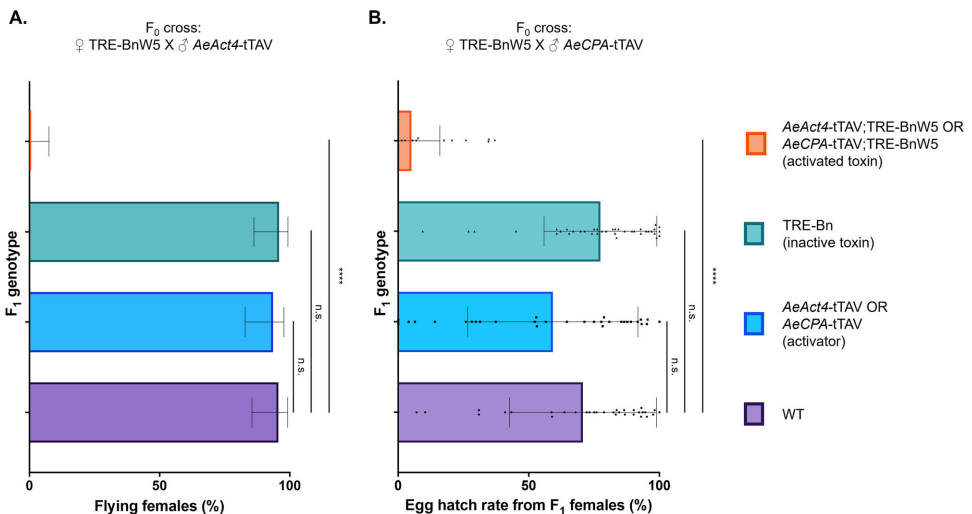
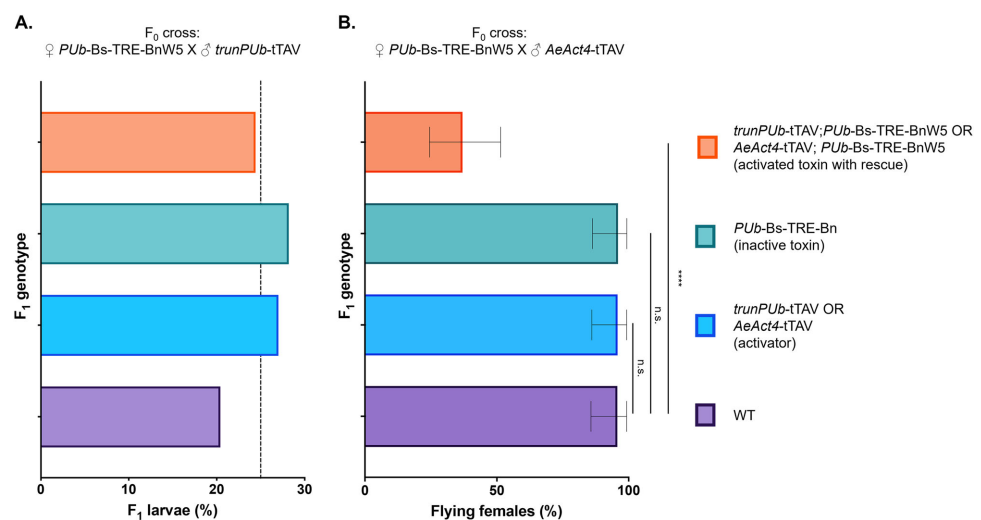
与trunPUb-tTAV激活的普遍性Bn表达导致100%致死率不同,AeAct4-tTAV驱动的飞行肌特异性表达使所有雌蚊丧失飞行能力,AeCPA-tTAV驱动的中肠表达则使卵孵化率从70.7%降至5.1%。
【Bs可挽救Bn的致死效应】
PUb-Bs能完全挽救trunPUb-tTAV诱导的普遍性Bn致死,但对飞行肌特异性Bn表型仅部分挽救,提示解毒剂表达水平需与毒素匹配。
研究结论指出,Bn-Bs系统首次在昆虫中实现可编程的组织特异性致死控制,其分子量小(总编码序列<200个氨基酸)、无需辅因子且正交性好的特点,为构建underdominance或Killer-Rescue基因驱动系统提供了理想元件。特别是通过组合不同组织特异性启动子,理论上可用单对Bn-Bs实现双毒素-解毒剂underdominance系统,克服传统设计需要两对独立系统的限制。该研究不仅拓展了蚊媒遗传控制的分子工具箱,其模块化设计理念也可推广至其他病媒昆虫的防控应用。
 生物通微信公众号
生物通微信公众号
知名企业招聘