
-

生物通官微
陪你抓住生命科技
跳动的脉搏
综述:HMGB1作为骨重塑关键调节因子的研究进展
【字体: 大 中 小 】 时间:2025年08月09日 来源:Stem Cell Research & Therapy 7.3
编辑推荐:
这篇综述系统阐述了高迁移率族蛋白B1(HMGB1)在骨重塑中的双重调控作用:作为损伤相关分子模式(DAMP)通过RAGE/TLRs受体协调成骨细胞(BMSCs)迁移与破骨细胞(BMMs)分化,在急性损伤时促进修复,而在慢性炎症(如OA、骨质疏松)中导致骨吸收失衡。文章创新性提出HMGB1氧化还原状态(fr-HMGB1/ds-HMGB1)决定其促炎或趋化功能,为靶向治疗骨代谢疾病提供新思路。
这个高度保守的核蛋白由215个氨基酸构成,包含两个DNA结合域(A-box/B-box)和酸性C末端。其功能受乙酰化、甲基化等翻译后修饰调控,特别是C23/C45/C106位半胱氨酸的氧化状态决定活性:完全还原型(fr-HMGB1)发挥趋化作用,而二硫键型(ds-HMGB1)则激活炎症反应。HMGB1可通过主动分泌(如巨噬细胞)或被动释放(细胞死亡)进入胞外空间。
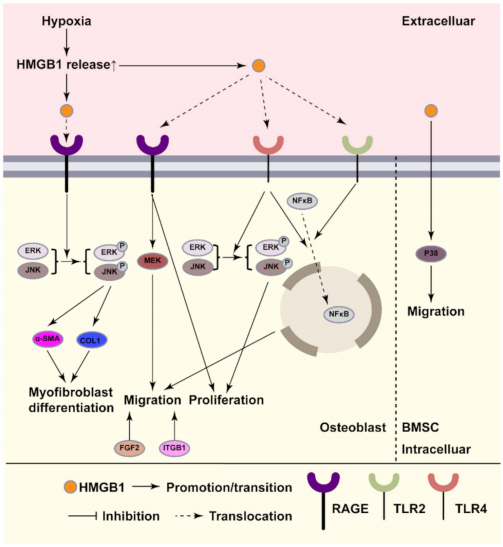
在破骨细胞方面,RANKL通过NOX1/ROS/p38通路抑制HO-1,触发HMGB1释放。胞外HMGB1通过TLR4促进前体细胞分化,并通过RAGE介导肌动蛋白重构完成成熟。成骨细胞中,HMGB1激活RAGE/MEK和TLR/NF-κB通路,促进迁移增殖。有趣的是,低氧条件下HMGB1-TLR4激活ERK/JNK可增强MG-63细胞增殖,而通过RAGE则诱导纤维化转变。
HMGB1通过RAGE/TLR2直接刺激内皮细胞(ECs)形成新生血管,并通过招募EPCs/HSCs间接促进血运重建。作为警报素,其与LPS形成的复合物可激活巨噬细胞产生IL-6、TNF-α等细胞因子。值得注意的是,ds-HMGB1诱导M1型极化加剧炎症,而fr-HMGB1与CXCL12协同可唤醒G0期干细胞进入GAlert状态。
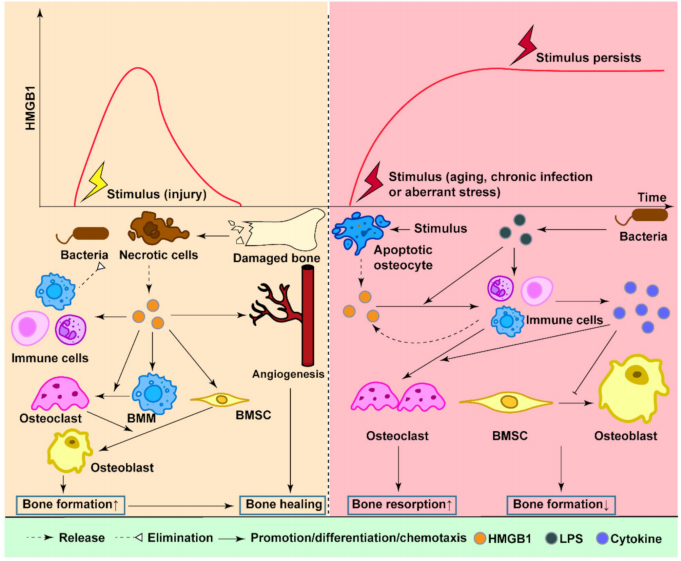
骨质疏松中衰老的骨细胞通过Cx43/miR21/PTEN通路凋亡,释放HMGB1和RANKL。OA患者滑液HMGB1水平升高,通过TLR2/4促进软骨细胞肥大分化,驱动H型血管异常增生。牙周炎时,HMGB1-LPS复合物刺激PDLCs产生IL-17等细胞因子,放大炎症级联反应。
局部应用3S-HMGB1(模拟fr-HMGB1)在糖尿病大鼠模型中显著改善骨整合,而中和抗体可缓解慢性炎症性骨破坏。未来研究需明确:①不同病理状态下RAGE/TLRs的优先激活模式;②骨细胞与其他细胞源HMGB1的贡献度;③疾病阶段转换中ds/fr-HMGB1比例动态变化。
 生物通微信公众号
生物通微信公众号
知名企业招聘