
-

生物通官微
陪你抓住生命科技
跳动的脉搏
TACE联合同步消融对比单纯TACE治疗神经内分泌肿瘤肝转移的疗效与安全性分析:基于病理分级和原发部位的比较研究
【字体: 大 中 小 】 时间:2025年08月09日 来源:Journal of Cancer Research and Clinical Oncology 2.8
编辑推荐:
本研究针对神经内分泌肿瘤(NENs)肝转移患者的治疗难题,通过回顾性分析108例患者的临床数据,比较了经动脉化疗栓塞术(TACE)与TACE联合同步微波消融(MWA)在不同病理分级(G1/G2/G3)和原发部位(胰腺/胃肠等)患者中的疗效差异。研究发现同步消融可显著延长G1/G2级患者的中位无进展生存期(PFS)(28.0 vs 18.0个月,P=0.009),尤其对胰腺来源肿瘤(PNETs)患者效果更优(中位PFS 32.0 vs 22.0个月,P=0.025)。研究为临床选择个体化介入治疗方案提供了重要循证依据。
神经内分泌肿瘤(NENs)作为一组起源于弥散神经内分泌系统的异质性肿瘤,其发病率在过去30年间增长了6倍,已成为消化系统肿瘤领域的重要临床挑战。尤其令人关注的是,这类肿瘤具有极强的肝脏转移倾向,约50-80%的病例会出现肝转移,而肝转移灶的进展程度直接决定患者预后。目前对于不可手术的神经内分泌肿瘤肝转移患者,经动脉化疗栓塞术(TACE)和局部消融治疗是主要的介入治疗手段,但关于这两种治疗方式的优劣比较,特别是针对不同病理分级和原发部位患者的差异化疗效,尚缺乏高质量的循证医学证据。
针对这一临床难题,复旦大学附属中山医院介入治疗科联合上海医学影像研究所的研究团队开展了一项重要研究。该研究通过回顾性分析2006-2022年间收治的108例神经内分泌肿瘤肝转移患者的临床资料,系统比较了单纯TACE与TACE联合同步微波消融(MWA)在不同WHO分级(G1/G2/G3)和原发部位(胰腺/胃肠等)患者中的疗效差异。相关研究成果发表在《Journal of Cancer Research and Clinical Oncology》上,为临床实践提供了重要参考。
研究人员采用了多学科协作的研究方法,主要技术路线包括:1)基于WHO 2019分级标准对入组患者进行病理分级(G1/G2/G3);2)根据治疗方式将患者分为同步消融组(46例)和单纯TACE组(62例);3)采用m-RECIST标准评估治疗效果;4)通过Kaplan-Meier法和Cox回归模型分析无进展生存期(PFS)和总生存期(OS)等预后指标。所有患者均来自复旦大学附属中山医院,经过严格的纳入排除标准筛选。
研究结果部分呈现了丰富的发现:
所有患者分析显示,虽然同步消融组的中位PFS(19.0月)略高于TACE组(18.3月),但差异未达统计学意义(P=0.134)。在OS方面,两组的中位OS分别为59.0月和46.8月(P=0.465),同样无显著差异。
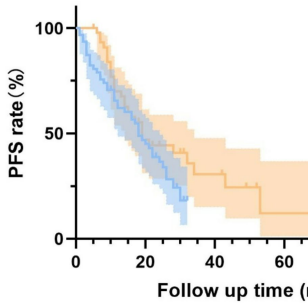
分级亚组分析获得突破性发现:在G2级患者中,同步消融显著延长中位PFS(28.0 vs 18.0月,P=0.009),而OS虽有延长趋势(59.0 vs 47.0月)但未达统计学差异。特别值得注意的是,对于G1/G2级患者这一重要亚群,同步消融组的PFS优势更为明显(28.0 vs 18.0月,P=0.009)。
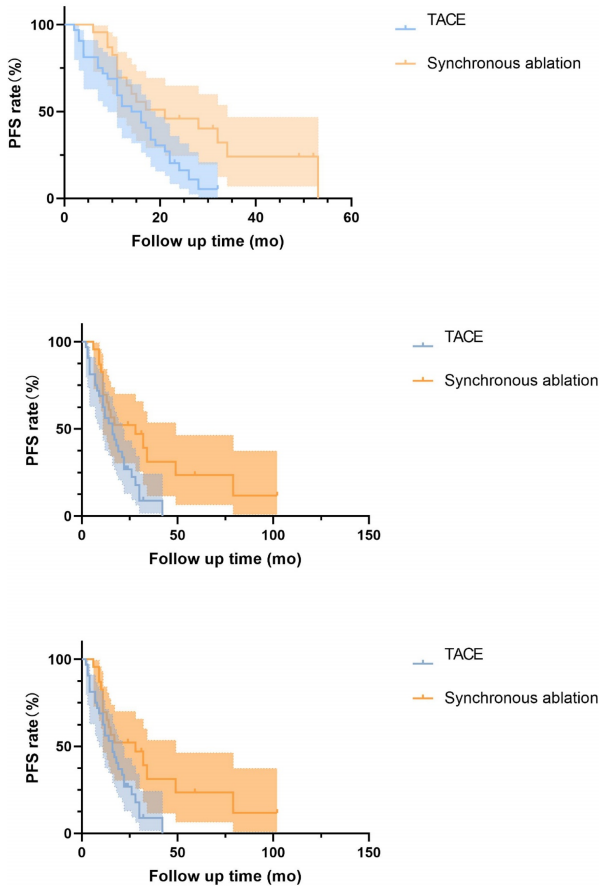
原发部位分析揭示:在胰腺神经内分泌肿瘤(pNETs)肝转移患者中,同步消融组的中位PFS显著优于单纯TACE组(32.0 vs 22.0月,P=0.025),而两组OS分别为111.0月和46.8月(P=0.161)。这一发现为胰腺来源患者的治疗选择提供了重要依据。
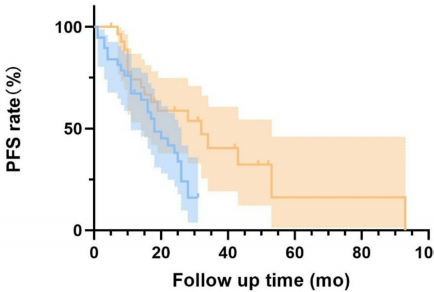
预后因素分析表明:CA-199是OS的独立预测因子(P=0.045);而原发部位(P=0.001)、白蛋白(Alb,P<0.030)和CEA(P<0.006)则是PFS的独立预测因素。这些生物标志物的发现为预后评估提供了新思路。
研究结论部分强调,对于神经内分泌肿瘤肝转移患者,特别是WHO G1/G2级和胰腺来源的患者,TACE联合同步微波消融治疗可显著延长无进展生存期,且安全性良好。这一发现具有重要的临床指导价值:首先,为介入科医师制定个体化治疗方案提供了循证依据;其次,明确了病理分级和原发部位在治疗决策中的重要性;最后,研究采用的"点面结合"治疗策略(消融处理主要病灶+TACE处理微小病灶)为综合介入治疗模式的优化提供了新思路。
该研究的创新性在于首次系统比较了同步消融联合TACE与单纯TACE在不同病理特征神经内分泌肿瘤肝转移患者中的疗效差异,填补了该领域的知识空白。虽然研究存在样本量有限、回顾性设计等局限性,但其发现为后续前瞻性多中心研究奠定了基础,对推动神经内分泌肿瘤肝转移的精准介入治疗具有重要意义。
 生物通微信公众号
生物通微信公众号
知名企业招聘