
-

ЩњЮяЭЈЙйЮЂ
ХуФузЅзЁЩњУќПЦММ
ЬјЖЏЕФТіВЋ
ПьЫйNGSМьВтММЪѕдкМБаддчгзСЃЯИАћАзбЊВЁжаНвЪОвўФфадPML-RARAШкКЯЕФСйДВМлжЕ
ЁЖnpj Precision OncologyЁЗЃКDetection of cytogenetically cryptic PML-RARA fusion in acute promyelocytic leukemia by rapid next generation sequencing
ЁОзжЬхЃК Дѓ жа аЁ ЁП ЪБМфЃК2025Фъ08дТ11Ше РДдДЃКnpj Precision Oncology 8
БрМЭЦМіЃК
ЁЁЁЁБОбаОПеыЖдМБаддчгзСЃЯИАћАзбЊВЁЃЈAPLЃЉеяЖЯжадМ1%ЕФвўФфадВЁР§ЃЈГЃЙцFISHМьВтвѕадЃЉЃЌЭЈЙ§ВЩгУ48аЁЪБПьЫйNGSММЪѕГЩЙІМьГіPML-RARAШкКЯЛљвђЃЌжЄЪЕСЫИУММЪѕЖдAPLдчЦкеяЖЯЕФЙиМќзїгУЁЃбаОПЭХЖгдкЕфаЭDICжЂзДЕЋFISHвѕадВЁР§жаЃЌРћгУOncomine Myeloid Assay GX v2ЭЌЪБМьГіPML(3)-RARA(3)ШкКЯКЭFLT3-ITDЭЛБфЃЌЮЊATRA+ATOОЋзМжЮСЦЬсЙЉвРОнЃЌНЋЗжзгеяЖЯжмЦкДгДЋЭГRT-PCRЕФ16ЬьЫѕЖЬжС2ЬьЃЌЯджјИФЩЦЛМепдЄКѓЁЃ
МБаддчгзСЃЯИАћАзбЊВЁЃЈAPLЃЉзїЮЊМБадЫшЯЕАзбЊВЁЃЈAMLЃЉжазюОпжЮСЦЯЃЭћШДгжзюазЯеЕФбЧаЭЃЌЦфеяЖЯЫйЖШжБНгОіЖЈЛМепЩњДцТЪЁЃОЁЙмPML-RARAШкКЯЛљвђЕФЗЂЯжЪЙAPLГЩЮЊЪзИіПЩжЮгњЕФГЩШЫAMLЃЌЕЋСйДВШдУцСйСНДѓРЇОГЃКвЛЪЧдМ5-30%ЛМепдкШЗеяЕБЬьЛђДЮШеЫРгкУжЩЂадбЊЙмФкФ§бЊЃЈDICЃЉЃЌЖўЪЧдМ1%ВЁР§ДцдкГЃЙцКЫаЭЗжЮіКЭFISHМьВтвѕадЕФвўФфадвзЮЛЁЃетаЉ"ТЉЭјжЎгу"ЭљЭљвђеяЖЯбгЮѓДэЪЇATRAЃЈШЋЗДЪНЮЌМзЫсЃЉЛЦН№жЮСЦДАПкЃЌЭЙЯдЯжгаеяЖЯЬхЯЕЕФжиДѓММЪѕЦПОБЁЃ
еыЖдетвЛСйДВЭДЕуЃЌМгжнДѓбЇЪЅЕибЧИчЗжаЃЃЈUniversity of California San DiegoЃЉЕФбаОПЭХЖгHailee St. LouisЕШШЫдкЁЖnpj Precision OncologyЁЗЗЂБэЭЛЦЦадбаОПЁЃЫћУЧВЩгУМЏГЩЛЏNGSВпТдЃЌдк51ЫъХЎадAPLвЩЫЦВЁР§жаЃЌЕБДЋЭГFISHКЭСїЪНЯИАћЪѕЃЈЯдЪОCD34+/HLA-DR+ЗЧЕфаЭБэаЭЃЉОљГЪвѕадЪБЃЌЭЈЙ§Oncomine Myeloid Assay GX v2 panelдк48аЁЪБФкЭЌВНМьГіPML(3)-RARA(3)ЖЬбЧаЭШкКЯКЭFLT3-ITDЭЛБфЃЌНЯЭтЫЭRT-PCRЬсЧА14ЬьЫјЖЈеяЖЯЁЃИУЛМепНгЪмATRA+ATOЃЈШ§бѕЛЏЖўЩщЃЉСЊКЯжЮСЦКѓбИЫйДяЭъШЋЛКНтЃЌжЄЪЕвўФфадbcr3бЧаЭЖдБъзМЗНАИУєИаЁЃ
ЙиМќММЪѕАќРЈЃК1ЃЉRARAЖЯСбЬНеыFISHМьВтЃЛ2ЃЉАаЯђ45ИіDNAЛљвђКЭ34ИіRNAШкКЯЧ§ЖЏЛљвђЕФNGS panelЃЛ3ЃЉGenexusМЏГЩВтађЦНЬЈЪЕЯж48аЁЪБжмзЊЃЛ4ЃЉЭтжмбЊгыЙЧЫшБъБОЕФЖрФЃЬЌбщжЄЁЃ
ЁОбаОПНсЙћЁП
• СйДВгыЪЕбщЪвЬиеїЃКЛМепГЪЯжАзЯИАћдіЖрЃЈ20,540/mm3ЃЉЁЂбЯжиDICЃЈЯЫЮЌЕААзд66 mg/dLЃЉЕШЕфаЭAPLБэЯжЃЌЕЋСїЪНЯдЪОCD34+/HLA-DR+УЌЖмБэаЭЃЌЙЧЫшЛюМьМћДѓСПCD117+/MPO+дЪМЯИАћЁЃ
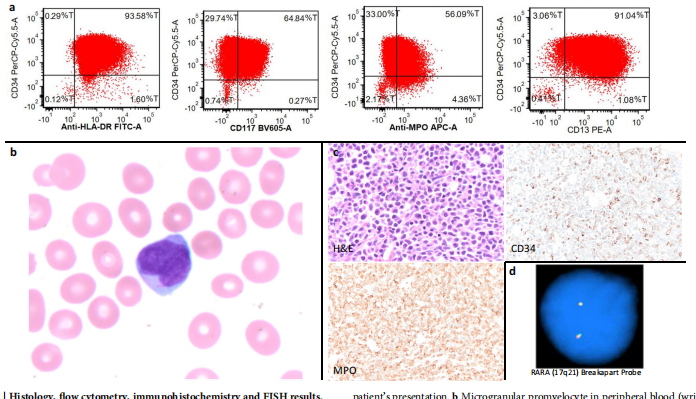
• ЗжзгеяЖЯЭЛЦЦЃКNGSТЪЯШМьГіPMLЕк3ФкКЌзггыRARAЕк3ЭтЯдзгШкКЯЃЌЖдгІbcr3ЖЬбЧаЭЃЌЭЌЪБЗЂЯжFLT3-ITDЃЈ48МюЛљжиИДЃЉЃЌЖјДЋЭГFISHЪЙгУAbbott RARAЖЯСбЬНеыЮДФмЗЂЯжвьГЃЁЃ

• жЮСЦЯьгІЃКЦєЖЏATRAКѓГіЯжЗжЛЏзлКЯеїЃЈАзЯИАћ>50,000/mm3ашВхЙмЃЉЃЌЕїећЗНАИЮЊATRA+ШЅМзбѕШсКьУЙЫиКѓЛёЭъШЋЛКНтЃЌЫцЗУЙЧЫшFLT3-ITDзЊвѕЁЃ
ИУбаОППЊДДадЕижЄЪЕЃКПьЫйNGSПЩЭЛЦЦAPLеяЖЯЕФ"ЫЋУЄЧј"ЁЊЁЊМШФмЪЖБ№вўФфадвзЮЛЃЈСщУєЖШГЌдНFISHЃЉЃЌгжПЩЭЌВНМьВтFLT3-ITDЕШЙВЭЛБфЃЛЦф"ШЋКЯвЛ"МьВтФЃЪННЯДЋЭГЗжзгМьВтзщКЯЃЈКЫаЭ+FISH+RT-PCR+ЭЛБфЩИВщЃЉНкЪЁ80%ЪБМфЁЃгШЦфЖдгкЮЂПХСЃаЭAPLЃЈеМвўФфВЁР§жївЊбЧаЭЃЉетРрвзЮѓеяИпЮЃШКЬхЃЌИУММЪѕНЋеяЖЯжмЦкбЙЫѕжСжЮСЦОіВпЙиМќДАПкЦкФкЃЌЪЙдчЦкЫРЭіТЪДгРњЪЗ30%НЕжСПЩЗРЗЖЮЇЁЃ
ЬжТлВПЗжЧПЕїЃКNGSдкШкКЯЛљвђМьВтжаОпга"Ш§ЮЌгХЪЦ"ЁЊЁЊПеМфЩЯПЩЪЖБ№ЗЧPMLАщТТЃЈШчSTAT5B-RARAЕШATRAФЭвЉбЧаЭЃЉЃЌЪБМфЩЯЪЕЯжГЌПьЫйжмзЊЃЌЭЈСПЩЯМцШнDNA/RNAЙВЗжЮіЁЃИУАИР§ЮЊНЋNGSФЩШыAPLвЛЯпеяЖЯТЗОЖЬсЙЉLevel 1AжЄОнЃЌЭЌЪБЦєЪОСйДВЃКЖдгкDICАщЗЧЕфаЭСїЪНБэаЭЕФAMLЃЌгІЬјЙ§"ж№ВНХХВщ"ДЋЭГСїГЬЃЌжБНгЦєЖЏNGSМьВтвдЧРЖсжЮСЦЯШЛњЁЃЫцзХВтађГЩБОНЕЕЭЃЌетжжВпТдгаЭћГЩЮЊбЊвКжзСіМБжЂеяЖЯЕФаТБъзМЁЃ
 ЩњЮяЭЈЮЂаХЙЋжкКХ
ЩњЮяЭЈЮЂаХЙЋжкКХ
НёШеЖЏЬЌ | ШЫВХЪаГЁ | аТММЪѕзЈРИ | жаЙњПЦбЇШЫ | дЦеЙЬЈ | BioHot | дЦНВЬУжБВЅ | ЛсеЙжааФ | ЬиМлзЈРИ | ММЪѕПьбЖ | УтЗбЪдгУ
АцШЈЫљга ЩњЮяЭЈ
Copyright© eBiotrade.com, All Rights Reserved
СЊЯЕаХЯфЃК
дСICPБИ09063491КХ