
-

生物通官微
陪你抓住生命科技
跳动的脉搏
Nrf2在成年小鼠大脑中以细胞特异性方式调控稳态转录特征和炎症反应
《iScience》:Nrf2 controls homeostatic transcriptional signatures and inflammatory responses in a cell-type specific manner in the adult mouse brain
【字体: 大 中 小 】 时间:2025年08月13日 来源:iScience 4.1
编辑推荐:
本研究揭示了转录因子Nrf2在成年小鼠大脑中的细胞特异性作用。为解决Nrf2在不同脑细胞类型中的功能差异问题,爱丁堡大学团队通过构建小胶质细胞、星形胶质细胞和脑内皮细胞特异性敲除小鼠模型,结合RNA-seq技术发现:内源性Nrf2在稳态条件下维持细胞特异性转录程序,并在系统性炎症中意外表现出促炎作用。该研究颠覆了传统认为Nrf2仅具抗炎功能的认知,为神经退行性疾病的靶向治疗提供了新视角。
在神经科学领域,转录因子Nrf2(核因子E2相关因子2)一直被视为对抗神经炎症的"守护者",但其在特定脑细胞中的精确作用机制却长期笼罩在迷雾中。传统观点认为,这个通过调控抗氧化反应元件(ARE)的转录因子主要发挥抗炎作用,然而这些认知大多基于药物激活实验,而忽略了内源性Nrf2的基础功能。更关键的是,大脑作为高度异质性的器官,包含小胶质细胞、星形胶质细胞和脑内皮细胞(BECs)等多种细胞类型,它们对Nrf2信号的反应可能千差万别――这正是爱丁堡大学(University of Edinburgh)医学研究团队试图解开的谜题。
为揭示这一细胞特异性机制,研究人员构建了三种诱导型条件性敲除小鼠模型:Nfe2l2Micro(小胶质细胞特异性)、Nfe2l2Astro(星形胶质细胞特异性)和Nfe2l2Endo(内皮细胞特异性)。通过流式细胞分选结合RNA测序技术,团队系统分析了Nrf2缺失对不同脑细胞转录组的影响,并采用脂多糖(LPS)诱导的系统性炎症模型评估其免疫调节功能。
主要技术方法
研究采用他莫昔芬诱导的Cre-loxP系统实现细胞特异性基因敲除;通过流式细胞术(FACS)分选CD11b+CD45low小胶质细胞、ACSA-2+星形胶质细胞和CD31+CD45-脑内皮细胞;利用RNA-seq进行全转录组分析;通过qPCR验证基因敲除效率;采用生物信息学工具(DESeq2、Enrichr)进行差异表达基因和通路富集分析。
Nrf2控制小胶质细胞、星形胶质细胞和BECs中不同的转录特征
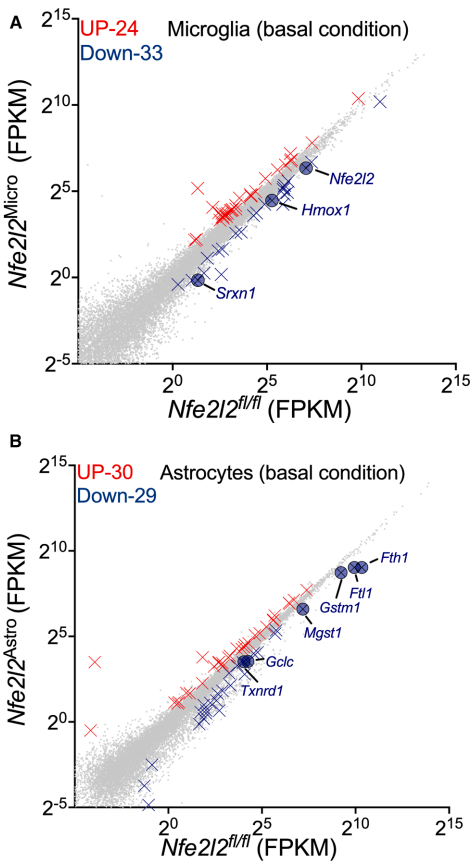
RNA-seq数据显示,在稳态条件下,Nrf2缺失导致三类细胞出现截然不同的转录变化:小胶质细胞中33个基因下调(如Hmox1、Srxn1),涉及氧化应激反应和铁离子稳态;星形胶质细胞中29个基因下调(如Gstm1、Fth1),影响谷胱甘肽代谢;而脑内皮细胞则呈现独特的血管相关基因变化。值得注意的是,三类细胞间仅有少量重叠基因(
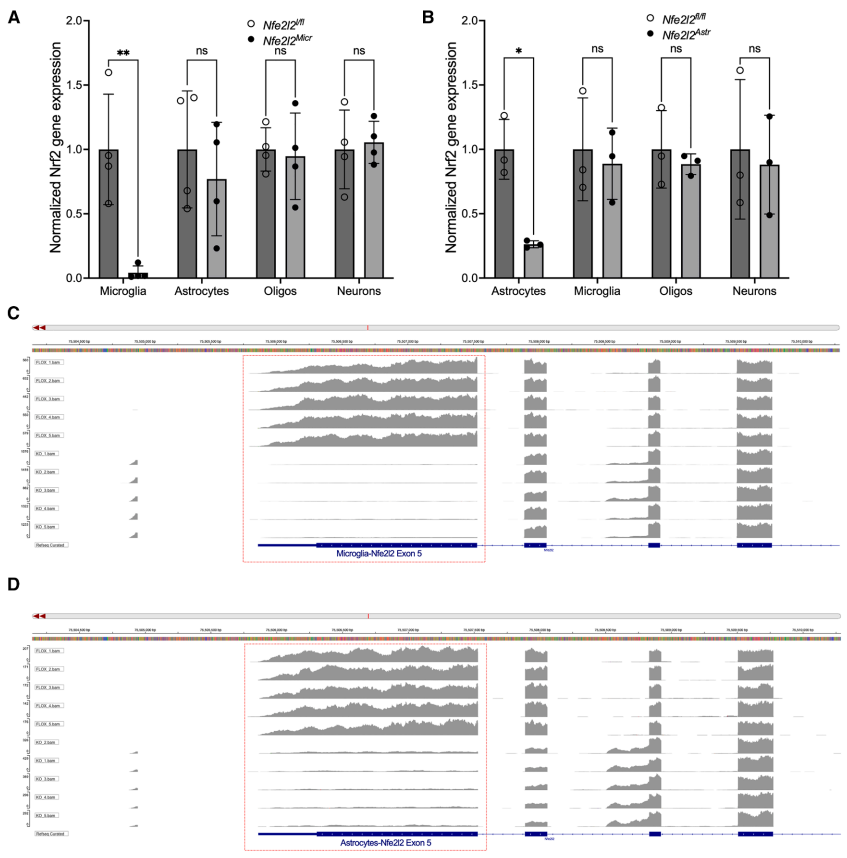
Nrf2调控系统性炎症中的炎症反应
当面临LPS挑战时,Nrf2缺失的小胶质细胞和星形胶质细胞表现出惊人的炎症反应减弱:小胶质细胞中100个LPS诱导基因表达降低(如Csf3、Timp1),涉及白细胞跨内皮迁移通路;星形胶质细胞中128个基因下调(如Irak1、Myc),影响MAPK和JAK-STAT信号通路。相反,脑内皮细胞的炎症反应几乎不受Nrf2缺失影响(
Nrf2在基础状态下介导小胶质细胞的促炎基因表达
最出人意料的发现是,即使在无刺激状态下,Nrf2缺失就足以降低小胶质细胞中促炎基因的基础表达水平。这种"内源性促炎"特性在星形胶质细胞和脑内皮细胞中并未观察到,揭示了Nrf2在神经免疫调控中的双重角色(
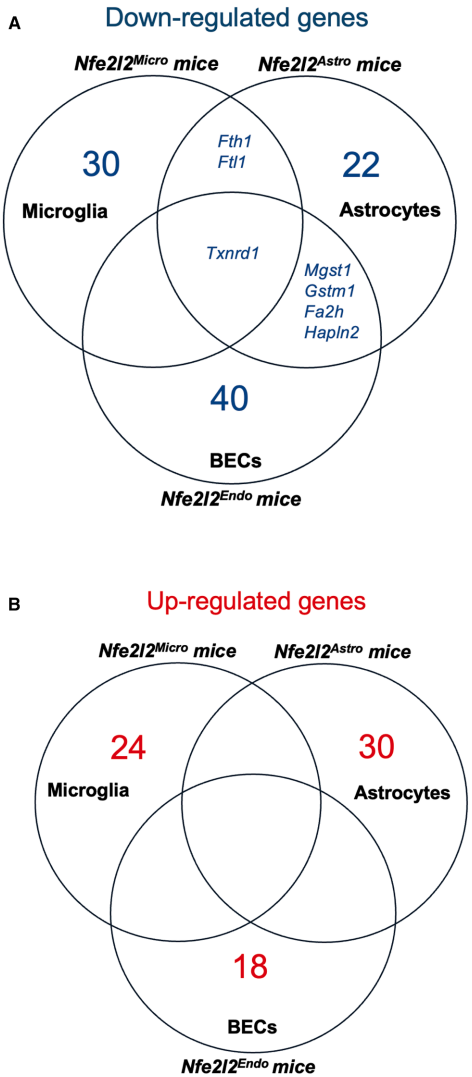
这项研究彻底改变了我们对Nrf2神经保护机制的理解:它不仅不是单纯的"抗炎卫士",反而在某些脑细胞中充当着炎症反应的"幕后推手"。这一发现对神经退行性疾病治疗策略具有深远影响――提示未来开发Nrf2靶向药物时,必须考虑细胞特异性递送问题。例如,三萜类化合物RTA-404(已获批治疗弗里德赖希共济失调)可能通过血脑屏障作用于内皮细胞,但其对小胶质细胞的作用可能需要重新评估。研究还建立了宝贵的小鼠模型资源,为后续探索Nrf2在阿尔茨海默病、帕金森病等疾病中的细胞特异性作用奠定了基础。
值得注意的是,这种细胞类型依赖性的Nrf2功能可能解释其在感染防御(需要促炎)与慢性炎症(需要抗炎)中看似矛盾的作用。正如通讯作者Jing Qiu指出的:"Nrf2就像一把双刃剑,关键在于我们如何根据疾病类型和病程阶段,精准调控特定细胞的Nrf2活性。"这一发现为开发下一代神经免疫调节剂提供了全新的理论框架。
 生物通微信公众号
生物通微信公众号