
-

生物通官微
陪你抓住生命科技
跳动的脉搏
组蛋白变体macroH2A1.1通过PARP依赖性修复通路调控拓扑异构酶1活性揭示癌症治疗新靶点
【字体: 大 中 小 】 时间:2025年08月13日 来源:Nature Communications 15.7
编辑推荐:
本研究揭示了组蛋白变体macroH2A1.1通过结合poly(ADP-ribose)(PAR)协调拓扑异构酶1(TOP1)切割复合体(TOP1cc)修复的新机制。研究人员发现macroH2A1.1选择性剪接异常可预测癌细胞对TOP1抑制剂(TOP1i)敏感性,为卵巢癌等恶性肿瘤的精准治疗提供了新型表观遗传标志物。该成果发表于《Nature Communications》,为理解转录相关基因组不稳定性及开发联合治疗策略奠定基础。
DNA在复制和转录过程中产生的扭转应力是基因组不稳定的主要来源。作为解决DNA超螺旋的关键酶,拓扑异构酶1(TOP1)通过形成瞬态的TOP1-DNA切割复合体(TOP1cc)来维持基因组稳定性。然而,当这些复合体异常稳定时,就会转化为具有细胞毒性的DNA损伤。尽管已知TOP1在基因组热点区域高度富集,但长期以来科学家们困惑于这些区域为何能避免过度的TOP1cc积累。这项发表在《Nature Communications》的研究,由约翰霍普金斯大学医学院(Johns Hopkins University School of Medicine)的Tae-Hee Lee和Philipp Oberdoerffer团队主导,揭示了组蛋白变体macroH2A1.1通过独特的表观遗传机制调控TOP1活性的全新机制。
研究人员采用多学科交叉的研究策略,主要包括:CUT&RUN测序技术绘制全基因组范围内macroH2A1.1和TOP1的染色质定位图谱;TOP1共价加合物测序(TOP1 CAD-Seq)定量检测TOP1cc动态变化;基于MS2转录报告系统实时监测修复因子募集;以及NCI60癌细胞库的药物敏感性分析等关键技术方法。
macroH2A1.1定义TOP1许可性染色质域
通过CUT&RUN测序发现,macroH2A1.1与TOP1在转录起始位点(TSS)等基因组区域显著共定位,这种关联不同于传统的异染色质标记H3K27me3。免疫共沉淀证实,在拓扑异构酶抑制剂camptothecin(CPT)处理下,macroH2A1.1与TOP1的相互作用显著增强,且依赖于PARP1的催化活性。

macroH2A1.1防止TOP1:DNA损伤积累
改良的TOP1 CAD-Seq分析显示,macroH2A1.1缺失导致TSS附近TOP1cc清除延迟,特别是在高转录活性基因区域。通过RADAR检测发现,表达PAR结合缺陷型突变体macroH2A1.1 G224E的细胞表现出与敲除细胞相似的TOP1cc修复缺陷。
PAR结合缺陷型macroH2A1.1损害TOP1cc清除
实验证实macroH2A1.1的PAR结合域对其修复功能至关重要。表达G224E突变体的细胞虽然能正常定位于染色质,但无法有效促进TOP1cc的清除,这直接证明了PAR结合能力在修复过程中的核心作用。
macroH2A1.1连接PARP1活性与TOP1cc修复因子组装
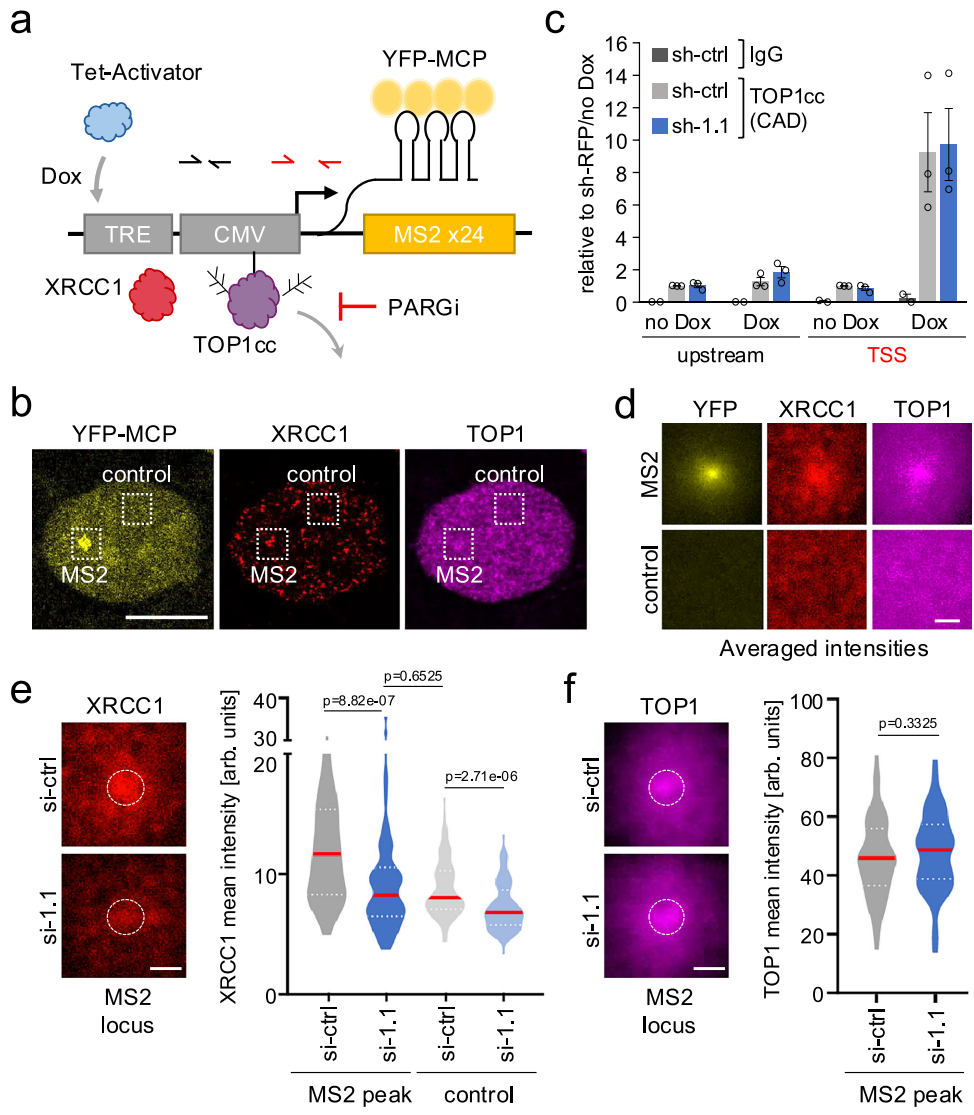
研究发现macroH2A1.1通过其PAR结合能力,促进XRCC1和TDP1等修复因子在损伤位点的募集。免疫荧光显示,CPT诱导的XRCC1焦点形成在macroH2A1.1缺失细胞中显著减少,而这一过程在非S期细胞中尤为明显。
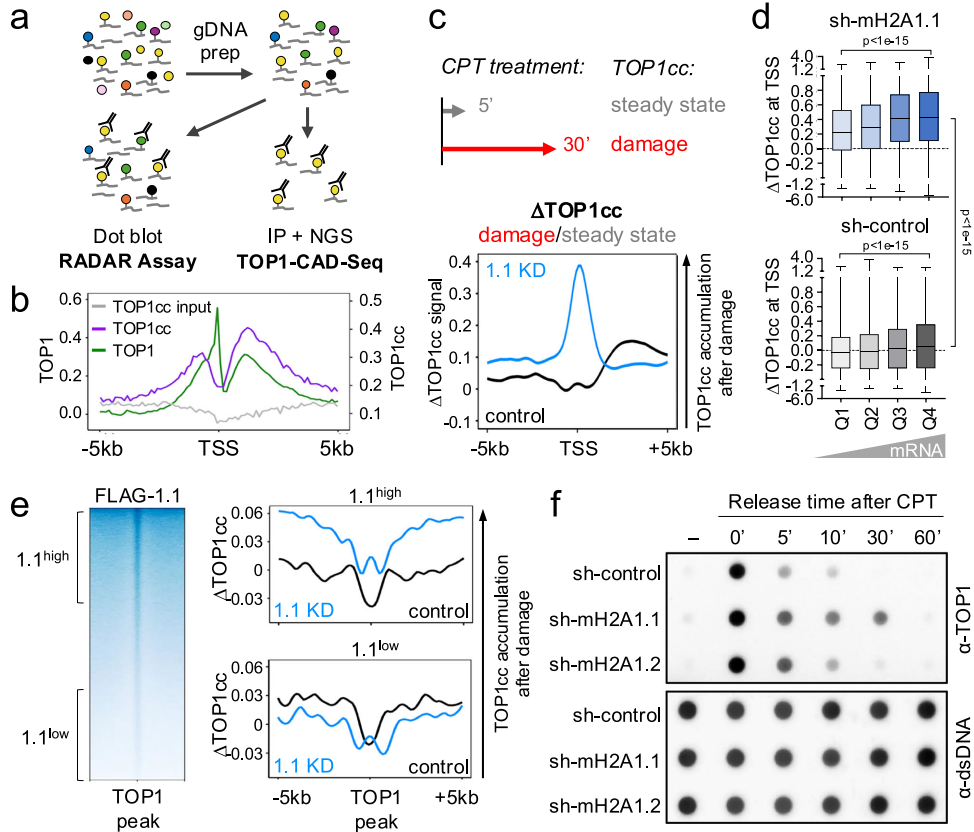
macroH2A1.1在拓扑应力位点促进修复
利用MS2转录报告系统,研究人员首次实现了对转录相关TOP1cc修复的实时观测。发现macroH2A1.1缺失会特异性减弱XRCC1在新生转录位点的募集,而不影响TOP1cc的形成本身。
macroH2A1.1防止TOP1诱导的DNA断裂
碱性彗星实验证实,macroH2A1.1缺失细胞对CPT诱导的单链断裂更为敏感。γH2AX分析进一步显示,这些细胞在复制非依赖途径中更易将未修复的TOP1cc转化为双链断裂。
macroH2A1剪接作为癌细胞TOP1i敏感性的标志
通过对NCI60乳腺癌细胞系的药物敏感性分析,发现macroH2A1.1表达水平与72种TOP1抑制剂的敏感性呈显著负相关。临床数据分析显示,macroH2A1.1低表达的卵巢癌患者对拓扑替康治疗反应更好。
这项研究确立了macroH2A1.1作为TOP1活性的表观遗传调节因子,揭示了其通过PAR结合能力协调TOP1cc修复的分子机制。研究首次证明:1)染色质环境特别是macroH2A1.1结构域可调控细胞对拓扑应力的响应;2)macroH2A1.1选择性剪接异常通过破坏PAR依赖的修复通路,创造了可被TOP1抑制剂靶向的癌症脆弱性。这些发现不仅深化了对转录相关基因组不稳定性的理解,更重要的是为预测TOP1抑制剂反应和开发PARP抑制剂联合治疗方案提供了新的分子标志物和治疗策略。该研究将表观遗传调控、DNA损伤修复和癌症治疗三个重要领域有机连接,为精准医学时代的癌症治疗开辟了新思路。
 生物通微信公众号
生物通微信公众号
知名企业招聘