
-

生物通官微
陪你抓住生命科技
跳动的脉搏
NLRP12通过抑制TRIM25介导的HK2降解促进胃癌糖酵解和H3K18乳酸化的分子机制研究
【字体: 大 中 小 】 时间:2025年08月14日 来源:Cell Death & Disease 9.6
编辑推荐:
本研究揭示了NLRP12在胃癌中的促癌新机制:通过竞争性结合TRIM25抑制HK2的K63泛素化降解,维持HK2蛋白稳定性从而增强糖酵解,促进乳酸介导的H3K18la表观遗传修饰并激活Myc转录。该发现为胃癌代谢重编程治疗提供了新靶点。
胃癌作为消化系统最常见的恶性肿瘤,其早期症状隐匿且治疗手段有限,患者预后较差。近年来,肿瘤细胞代谢重编程成为癌症治疗的关键策略,其中Warburg效应(即有氧糖酵解)是胃癌细胞的显著特征。然而,调控这一过程的分子机制尚未完全阐明。盐城临床学院(徐州医科大学附属医院)的研究团队在《Cell Death and Disease》发表的重要研究,揭示了先天免疫受体NLRP12通过调控糖酵解关键酶HK2的蛋白稳定性,促进胃癌进展的新机制。
研究人员采用TCGA数据库分析、临床样本验证(68对胃癌/癌旁组织)及多种胃癌细胞系(SNU-216/AGS/HGC-27等),结合裸鼠移植瘤模型,通过代谢流分析、泛素化检测、染色质免疫共沉淀等技术,系统阐明了NLRP12-HK2-H3K18la-Myc信号轴的作用机制。
研究结果:
NLRP12在胃癌中高表达且与不良预后相关
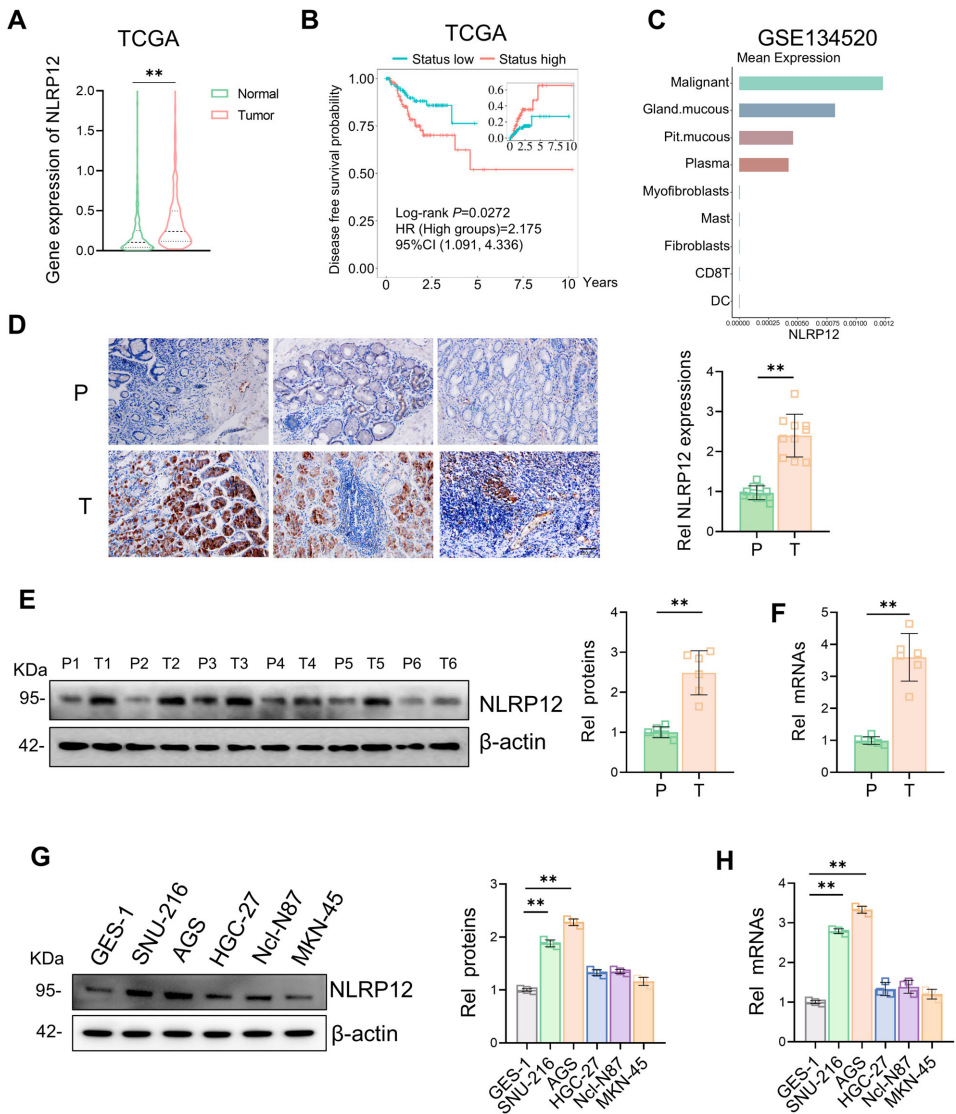
通过TCGA数据库和单细胞测序数据(GSE134520)分析发现,NLRP12在胃癌组织中显著高表达,且与临床分期(P=0.006)和转移(P=0.020)显著相关。免疫组化和Western blot验证显示,NLRP12在胃癌组织的表达水平是癌旁的2.3倍(P<0.01)。
NLRP12促进胃癌细胞增殖
体外实验显示,敲低NLRP12使AGS细胞增殖率降低47%(CCK-8检测),而过表达使MKN-45细胞克隆形成数增加2.1倍(P<0.01)。裸鼠模型中,NLRP12过表达组肿瘤体积达1287±156 mm3,显著高于对照组的682±89 mm3。
NLRP12通过糖酵解-H3K18la-Myc轴驱动肿瘤进展
Seahorse分析显示NLRP12使糖酵解能力提升2.4倍(P<0.01),乳酸产量增加3.1倍。特别值得注意的是,NLRP12特异性促进组蛋白H3第18位赖氨酸乳酸化(H3K18la),通过ChIP-qPCR证实该修饰使Myc基因转录水平提升2.8倍。
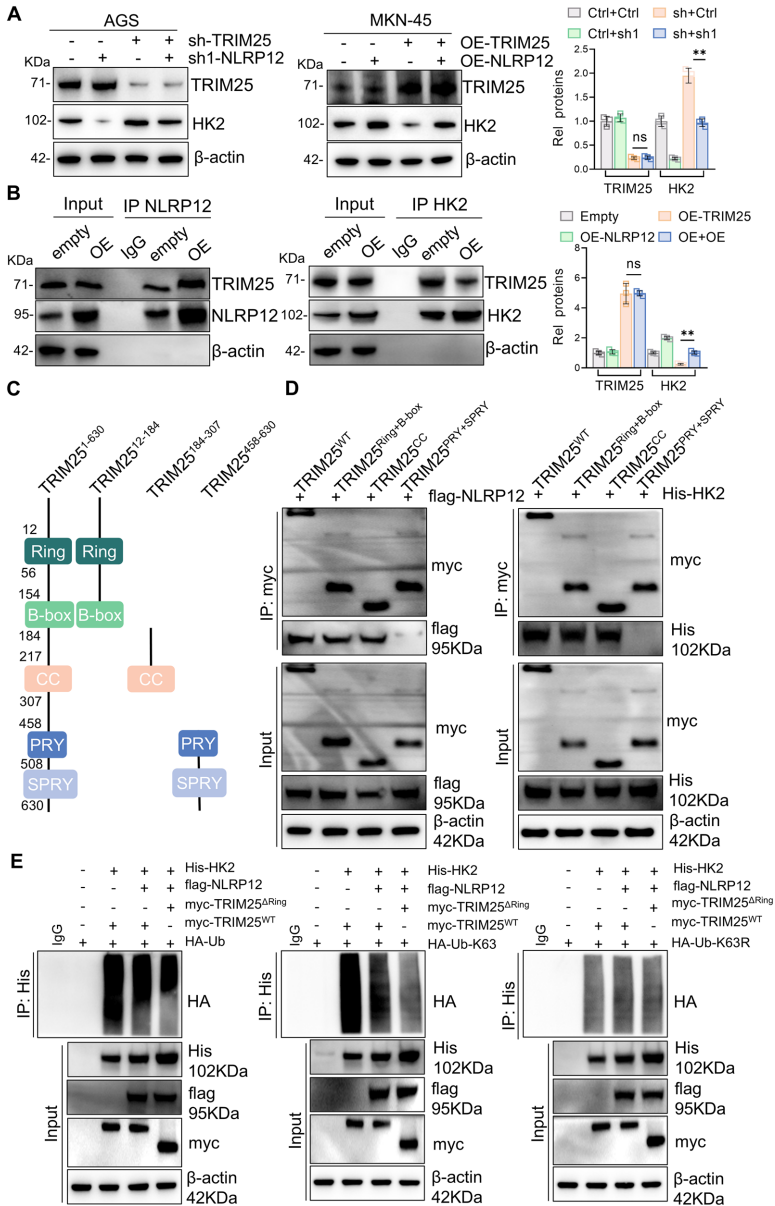
分子机制:NLRP12竞争性抑制TRIM25介导的HK2降解
研究发现NLRP12不改变HK2 mRNA水平,但通过阻断E3连接酶TRIM25与HK2的结合(KD=3.64×10-7 M),抑制HK2的K63泛素化。溶酶体IP实验证实,NLRP12敲低使溶酶体中HK2含量增加3.2倍(P<0.01),表明其通过阻断自噬-溶酶体途径维持HK2稳定。
这项研究首次揭示了NLRP12在胃癌代谢重编程中的关键作用,阐明了"NLRP12-TRIM25-HK2-H3K18la-Myc"的全新信号轴。该发现不仅为理解胃癌发生发展提供了新视角,更提示靶向NLRP12/HK2通路可能成为胃癌治疗的新策略。特别是研究中发现的代谢-表观遗传交叉调控机制,为开发联合代谢抑制剂和表观遗传药物的治疗方案提供了理论依据。值得注意的是,2-DG(2-脱氧葡萄糖)在实验中显示出逆转NLRP12促癌效应的潜力,这为临床转化提供了直接线索。
 生物通微信公众号
生物通微信公众号
知名企业招聘