
-

生物通官微
陪你抓住生命科技
跳动的脉搏
阴道微生态中细菌性阴道病相关菌群与阴道毛滴虫的互作机制:增强寄生虫致病性及宿主免疫应答的新发现
《Parasites & Vectors》:Interactions between bacterial vaginosis-associated microbiota and Trichomonas vaginalis modulate parasite-induced pathogenicity and host immune responses
【字体: 大 中 小 】 时间:2025年08月15日 来源:Parasites & Vectors 3.5
编辑推荐:
本研究针对阴道毛滴虫(Tv)与细菌性阴道病(BV)相关菌群(BVB)的协同致病机制展开深入探索。研究人员通过建立体外共培养模型,首次揭示特定BVB(如普雷沃菌P. bivia)能显著增强Tv的黏附蛋白ap65基因表达,促进寄生虫对宿主细胞的黏附与细胞毒性,并激活PI3K/ERK/p38 MAPK信号通路及上皮-间质转化(EMT)过程。该研究为理解阴道微环境中宿主-细菌-寄生虫的复杂互作提供了关键证据,对开发混合感染的新型干预策略具有重要临床意义。
在女性生殖健康领域,阴道毛滴虫(Tv)感染和细菌性阴道病(BV)如同"狼狈为奸"的致病组合。全球每年有1.56亿例Tv感染病例,而BV影响着近30%的育龄女性。这两种疾病不仅常同时出现,更会相互加重症状――增加HIV感染风险、引发妇科并发症甚至与宫颈癌相关。但长期以来,科学家们对这两种病原体如何在阴道微环境中"暗中勾结"增强致病力的机制知之甚少。
为解开这个谜团,台湾国防医学院(Host-Parasite Interactions Laboratory, National Defense Medical Center)的研究团队开展了一项开创性研究。他们发现特定BV相关细菌竟会"教唆"Tv变得更危险:普雷沃菌(P. bivia)能显著增强Tv的"武器库"(黏附蛋白AP65),使其更易攻击宿主细胞;还会"煽动"Tv激活宿主细胞的炎症信号通路,引发"细胞叛变"(EMT过程)。这项发表在《Parasites》的研究,首次揭示了阴道菌群如何成为Tv的"帮凶",为混合感染的精准治疗提供了新靶点。
研究团队运用多学科技术手段:建立Tv与四种阴道细菌(L. crispatus、E. coli、P. bivia、L. iners)的共培养系统;通过RT-PCR检测Tv毒力基因表达;采用荧光标记法量化寄生虫黏附率;结合ELISA和Western blot分析炎症因子分泌及信号通路激活。
Tv与特定BVB互作影响寄生虫生长和毒力
研究发现P. bivia如同Tv的"生长激素",能持续促进寄生虫增殖。更惊人的是,这种细菌还上调了Tv的"攻击武器"ap65基因表达,而健康菌L. crispatus则表现出抑制作用。
细菌预处理的Tv增强宿主细胞损伤
当Tv"吸收"了P. bivia的特性后,对宿主细胞Ect1的黏附率提高50%,并造成更严重的细胞损伤。这种"狼狈为奸"的效果在共培养120分钟后尤为明显。
炎症风暴的引发
P. bivia预处理的Tv诱导宿主细胞分泌IL-6、IL-8等炎症因子达到峰值,特别是CXCL1分泌量增加2倍。这种"细胞求救信号"可能解释临床观察到的混合感染严重炎症反应。
信号通路与EMT的激活
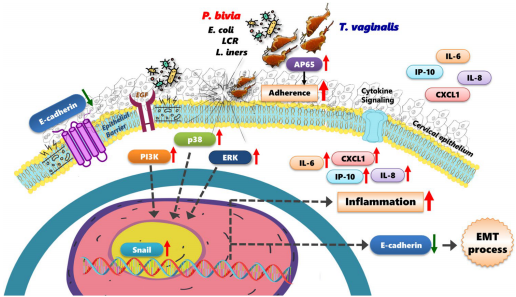
研究揭示P. bivia-Tv组合能同时激活PI3K、ERK和p38 MAPK三条"炎症信号高速公路",并诱发上皮细胞"叛变"(E-cadherin下调、Snail上调的EMT过程),这可能是混合感染导致组织长期损伤的关键机制。
这项研究首次绘制了阴道微环境中"细菌-寄生虫-宿主"三方对话的分子图谱。P. bivia作为"病原体帮凶"的发现尤其重要,它通过多重机制增强Tv致病性:既提供生长优势,又增强毒力武器,还"教唆"Tv扰乱宿主防御系统。这些发现为开发针对混合感染的联合疗法提供了理论依据――未来或许可以通过调节阴道菌群来削弱Tv的战斗力。更重要的是,该研究提示临床诊治需关注阴道微生态整体平衡,而非单一病原体,这对降低HIV感染风险、预防妇科肿瘤等并发症具有深远意义。
 生物通微信公众号
生物通微信公众号