
-

生物通官微
陪你抓住生命科技
跳动的脉搏
综述:质粒拷贝数作为细菌致病性和抗生素耐药性的调控因子
【字体: 大 中 小 】 时间:2025年08月19日 来源:npj Antimicrobials and Resistance
编辑推荐:
这篇综述深入探讨了质粒拷贝数(PCN)的动态调控机制及其在平衡细菌适应性、毒力基因剂量和抗生素耐药性中的核心作用。文章系统梳理了PCN的分子调控网络(包括iteron重复序列、反义RNA和毒素-抗毒素系统),揭示了PCN如何通过基因剂量效应影响T3SS毒力系统表达和β-内酰胺酶耐药性,为理解细菌进化及临床耐药防控提供了新视角。
作为细菌适应性进化的关键载体,质粒通过精确的拷贝数控制平衡其代谢负担与功能收益。低拷贝数质粒(LCP,1-5拷贝/细胞)依赖ParABS等主动分配系统确保稳定遗传,而高拷贝数质粒(HCP,50-100拷贝/细胞)则通过随机分配维持。复制控制的核心在于三类分子开关:
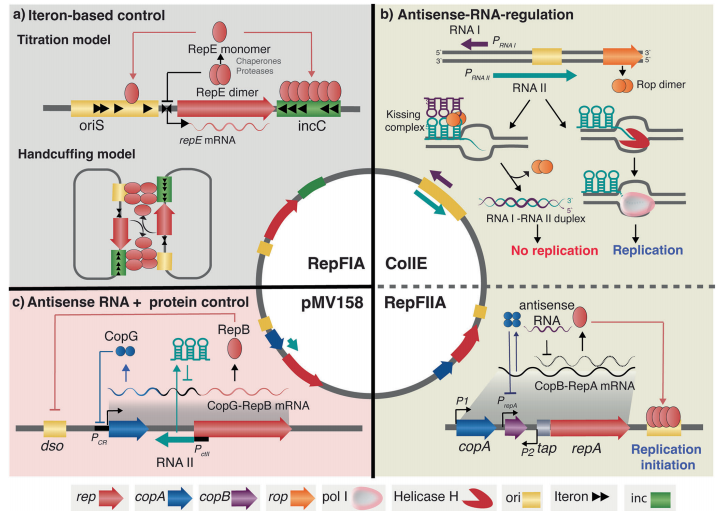
Iteron介导的调控:如沙门氏菌R1质粒通过Rep蛋白与ori位点的iteron重复序列结合,过量Rep会形成"分子手铐"抑制复制起始;
反义RNA调控:ColE1型质粒利用RNA I/II配对阻碍引物形成,而R1质粒的CopA/CopT系统则阻断RepA翻译;
蛋白复合物调控:链球菌pMV158同时采用CopG阻遏蛋白和RNAII实现双反馈调节。
质粒携带必然带来代谢成本,但环境压力可驱动PCN动态调整。耶尔森菌的毒力质粒在宿主体温(37°C)下PCN提升3倍,通过增加T3SS效应蛋白YopD的剂量增强侵袭力。相反,当ParE毒素胁迫时,大肠杆菌会主动降低PCN以维持生存。这种权衡在进化中催生了"隐形质粒"――删除代价高昂的耐药基因(AMR)但保留高PCN的变异体,揭示了基因剂量与功能选择的微妙平衡。
PCN直接决定blaNDM等耐药基因的剂量效应。美罗培南压力下,IncX3质粒的repA突变使PCN和接合转移频率同步增加;而pOXA-48质粒在患者肠道中通过ori区突变获得高拷贝特性。更值得注意的是,抗生素可诱导RecA介导的质粒多聚化,产生172拷贝的"超级质粒",导致血流感染菌株出现显著异质性耐药(HR)。这种可逆的基因剂量扩增,比染色体突变更能快速响应抗生素压力。
高PCN通过两种途径塑造长期进化:一方面增加突变供给(如copA突变解除复制抑制),另一方面增强分离漂变――等位基因在质粒群体中的随机分配延缓了优势变异的固定。沙门氏菌pSLT质粒在血清中表现出1-8拷贝的细胞间差异,形成具有不同毒力表达水平的亚群。宿主染色体补偿突变(如DNA聚合酶I变异)则能稳定这种多态性,使质粒成为细菌适应新生态位的"基因试验场"。
PCN动态调控网络为遏制耐药传播提供了新靶点:干扰Rep-iteron相互作用可阻断质粒扩增,而抑制PcnB poly(A)聚合酶能 destabilize毒力质粒。单细胞PCN监测技术的进步,将有助于预测耐药爆发和优化联合用药策略。理解PCN如何协调水平基因转移与宿主适应性,将是应对超级细菌威胁的关键突破口。
 生物通微信公众号
生物通微信公众号
知名企业招聘