
-

生物通官微
陪你抓住生命科技
跳动的脉搏
地塞米松缓释人工耳蜗通过抑制炎症和异物反应改善耳蜗植入效果
【字体: 大 中 小 】 时间:2025年08月21日 来源:Scientific Reports 3.9
编辑推荐:
为解决人工耳蜗(CI)植入后炎症性异物反应(FBR)导致的电极阻抗升高和听力损失问题,研究人员通过小鼠模型和人类临床试验,证实地塞米松缓释电极(Dex-CI)可长期抑制CX3CR1+巨噬细胞浸润、减少α-SMA+纤维化,并显著降低电极阻抗。该研究为优化CI功能提供了新策略,成果发表于《Scientific Reports》。
背景与挑战
全球约4.66亿人受听力损失困扰,人工耳蜗(CI)是重度感音神经性聋的主要治疗手段。然而,CI植入后引发的炎症性异物反应(FBR)会导致电极阻抗升高、残余听力丧失和言语识别率下降。尽管临床常用局部地塞米松(Dex-local)缓解炎症,但其长期效果有限。更棘手的是,FBR涉及巨噬细胞(CX3CR1+)、T/B淋巴细胞等多类免疫细胞浸润,以及α-平滑肌肌动蛋白(α-SMA)介导的纤维化,但目前缺乏针对性干预方案。
研究设计与方法
美国爱荷华大学团队联合美国国立卫生研究院等机构,采用CX3CR1+/GFP Thy1+/YFP双报告基因小鼠模型,对比标准CI、地塞米松缓释CI(Dex-CI)和Dex-local的长期效果。通过超高效液相色谱-质谱(UPLC-MS)检测药物释放,结合三维免疫荧光定量分析巨噬细胞密度、纤维化程度和螺旋神经节神经元(SGN)存活。人类受试者接受632D型Dex-CI植入,远程监测电极阻抗变化。单细胞RNA测序(scRNA-seq)解析了植入耳蜗的免疫细胞亚群特征。
研究结果
1. Dex-CI实现长期药物缓释
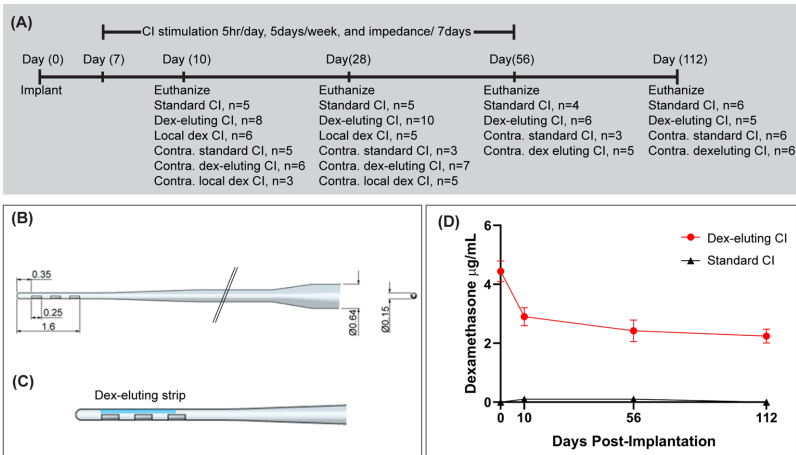
植入小鼠体内的Dex-CI在112天内持续释放地塞米松(p=0.0008),而UPLC-MS显示药物含量随时间显著下降。
2. Dex-CI显著抑制炎症反应
在耳蜗底转:
巨噬细胞浸润:Dex-CI使CX3CR1+细胞密度在56天内降低99%(p=0.0001),而Dex-local仅短期有效(10天,p=0.0181)。
纤维化抑制:α-SMA+纤维组织占比从标准CI组的15%降至Dex-CI组的2%(p=0.0021)。
3. 电极阻抗与临床转化
小鼠模型:Dex-CI组阻抗较标准CI降低40%(p=0.0001),而Dex-local无显著差异(p=0.99)。
人类数据:632D型Dex-CI使用者基底电极阻抗降低30%,且极化阻抗改善更明显(图6B)。
4. 免疫微环境解析
scRNA-seq发现植入耳蜗中存在促炎性单核细胞(高表达Ccl4、Il1b)和纤维化相关巨噬细胞亚群,Dex-CI可下调这些细胞的活化标志物MHC II。
结论与意义
该研究首次证实:
Dex-CI通过持续释放地塞米松,形成"药物缓释-抑制炎症-减少纤维化-降低阻抗"的良性循环,效果远超当前临床Dex-local方案;
电极阻抗降低与耳蜗底转纤维化程度直接相关,为临床监测提供生物标志物;
单细胞数据揭示了FBR的细胞多样性,为开发靶向疗法(如阻断Ccl4/CX3CR1通路)奠定基础。
研究团队指出,Dex-CI已进入多项临床试验(NCT04750642),未来或可推广至其他植入式神经假体。这一突破不仅提升CI性能,更为解决生物材料异物反应这一共性难题提供了范本。

 生物通微信公众号
生物通微信公众号
知名企业招聘