
-

生物通官微
陪你抓住生命科技
跳动的脉搏
综述:基于聚乳酸-羟基乙酸共聚物(PLGA)的药物递送系统在帕金森病治疗中的革新应用
【字体: 大 中 小 】 时间:2025年08月21日 来源:npj Parkinson's Disease 6.7
编辑推荐:
这篇综述系统阐述了PLGA纳米载体在帕金森病(PD)治疗中的突破性进展。通过克服血脑屏障(BBB)穿透难题,PLGA纳米系统实现了多巴胺能药物(如左旋多巴、罗匹尼罗)和植物活性成分(如白藜芦醇、姜黄素)的靶向递送,显著提升了药物稳定性、生物利用度及神经保护效果。文章详细解析了PD的α-突触核蛋白(α-synuclein)聚集、线粒体功能障碍等病理机制,并论证了PLGA载体在改善运动症状和延缓疾病进展方面的双重优势。
帕金森病治疗的纳米革命
病理机制的多维挑战
帕金森病(PD)作为第二大神经退行性疾病,全球影响着700-1000万患者。其核心病理表现为黑质多巴胺能神经元退化,伴随纹状体多巴胺水平下降。超越传统认知的是,PD还涉及α-突触核蛋白(α-synuclein)异常聚集形成路易小体、线粒体自噬障碍(PINK1/Parkin通路异常)、以及神经炎症级联反应。这些机制共同构成"病理三角",加速神经元死亡。
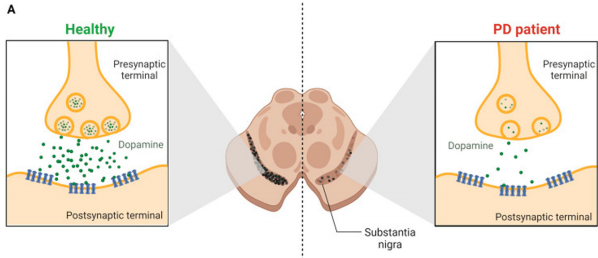
现有疗法的局限性
尽管左旋多巴仍是PD治疗的"金标准",但长期使用会导致剂末现象和异动症。MAO-B抑制剂(如司来吉兰)和COMT抑制剂(如恩他卡朋)虽能延缓多巴胺降解,却面临中枢渗透率低和肝毒性等问题。更令人遗憾的是,具有疾病修饰潜力的HDAC6抑制剂(如CAY10603)和二甲双胍等代谢调节剂,因水溶性差和快速清除而难以发挥疗效。
PLGA纳米载体的突破优势
聚乳酸-羟基乙酸共聚物(PLGA)凭借其可降解为无毒单体(乳酸和乙醇酸)、载药灵活性(可包封亲水/疏水药物)、以及表面可功能化等特点脱颖而出。通过乳铁蛋白修饰或PEG化,PLGA纳米粒能通过受体介导转运(RMT)穿越BBB,如乳铁蛋白修饰的纳米粒在纹状体的富集度比未修饰组提高1.5倍。
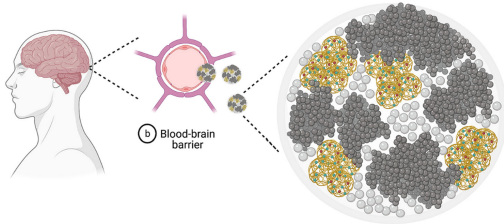
药物递送创新实践
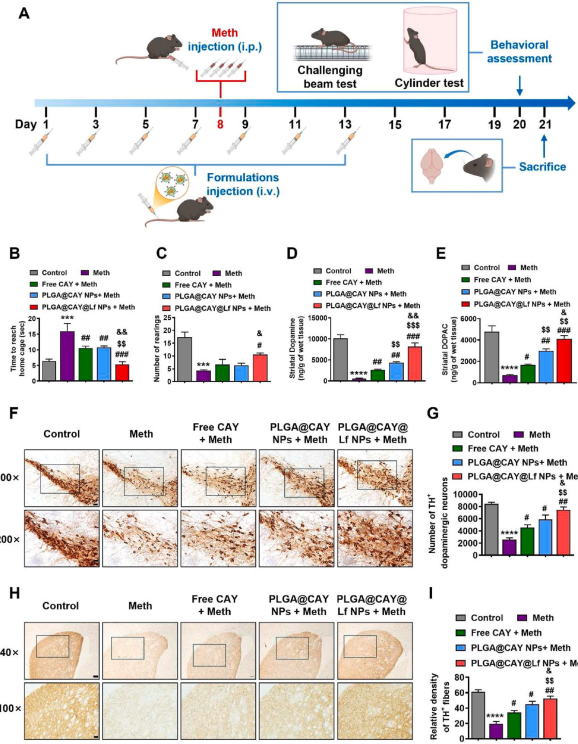
多巴胺激动剂普拉克索与金纳米球共载的PLGA微粒(粒径24μm)在近红外光控释下,使PD模型鼠在旋转棒测试中的跌落潜伏期从66秒提升至291秒。更巧妙的是,左旋多巴/苄丝肼PLGA微球通过上调β-arrestin2蛋白,使异动症评分降低60%。而乳铁蛋白-CAY10603-PLGA纳米粒则使乙酰化α-微管蛋白水平提升11.9倍,显著减少α-突触核蛋白聚集。
植物活性成分的华丽转身
针对姜黄素生物利用度低的问题,PLGA纳米粒联合低频聚焦超声(LIFU)使其脑部递送效率提升1.45倍。白藜芦醇-PLGA纳米粒则通过降低TNF-α/β-肌动蛋白比值14.1倍,展现强大抗炎效果。值得注意的是,橙皮素-PLGA纳米粒(粒径162nm)使PD大鼠的SOD活性提升至225.12 U/mgprot,同时MDA水平降低51%。
临床转化里程碑
罗替高汀PLGA微球(LY03003)已完成III期临床试验,药效可持续28天。毒理学研究显示,食蟹猴在360mg/kg剂量下仍保持良好耐受性,仅出现可逆的注射部位结节。这为每月一次给药的PD治疗方案铺平了道路。
未来挑战与机遇
尽管PLGA载体取得突破,但酸性降解产物引发的局部炎症、大规模生产的质量控制、以及多药共递送系统的开发仍需突破。微流控技术等新型制备工艺,或将成为实现GMP标准生产的关键。
这项技术革新不仅为PD治疗提供新范式,更启示我们:当材料科学与神经病学碰撞,纳米载体将成为打通血脑屏障的"特洛伊木马",为神经退行性疾病的治疗开启全新篇章。
 生物通微信公众号
生物通微信公众号
知名企业招聘