
-

生物通官微
陪你抓住生命科技
跳动的脉搏
神经母细胞瘤化疗后免疫功能变化及潜在免疫靶点预测研究
【字体: 大 中 小 】 时间:2025年08月22日 来源:BMC Medical Genomics 2
编辑推荐:
本研究针对儿童神经母细胞瘤化疗耐受性强、疗效难以评估的临床难题,通过尿液蛋白质组学分析联合生物信息学方法,揭示了化疗后CD8+ T细胞介导的免疫抑制状态与mTOR信号通路激活的关联,首次发现SEMA7A蛋白表达抑制与CD8+ T细胞浸润的正相关性,并预测了四氯二苯并二噁英等靶向SEMA7A的化合物,为神经母细胞瘤协同化疗的免疫治疗提供了新靶点。
神经母细胞瘤作为儿童最常见的颅外实体肿瘤,其治疗困境始终牵动着医学界的心弦。尽管多模式联合疗法显著改善了高危患者的生存期,但5年生存率仍低于50%,而化疗带来的骨髓抑制等副作用更让患儿雪上加霜。更令人担忧的是,即便近年来广泛应用的抗GD2免疫疗法,在复发或难治性病例中的应答率仍不尽如人意。这种"疗效天花板"现象促使科学家们思考:是否存在更精准的免疫靶点能与化疗产生协同效应?
北京儿童医院Ma Yunfei团队在《BMC Medical Genomics》发表的研究给出了突破性答案。研究人员创新性地采用尿液蛋白质组学技术,对12例接受CVP方案(顺铂+依托泊苷)化疗的患儿进行动态监测,结合20例健康儿童对照,通过LC-MS/MS质谱分析鉴定出1935种蛋白质。运用ESTIMATE算法和ssGSEA分析揭示化疗后免疫微环境特征,并采用Mfuzz动态表达模型锁定关键靶点。
研究结果呈现三大发现:首先,免疫分析显示化疗7天后免疫评分(ImmuneScore)显著降低,21天后逐渐恢复,其中CD8+ T细胞减少是免疫抑制的关键因素。其次,通过差异表达分析和动态聚类,筛选出112个化疗相关差异蛋白,其中mTOR信号通路相关蛋白(如ATP6V1G1、KRAS等)的异常激活尤为突出。最后,研究发现神经母细胞瘤化疗显著抑制SEMA7A表达,该蛋白与CD8+ T细胞浸润呈正相关(r=0.62),并通过CTD数据库预测四氯二苯并二噁英等化合物可能靶向调控SEMA7A。
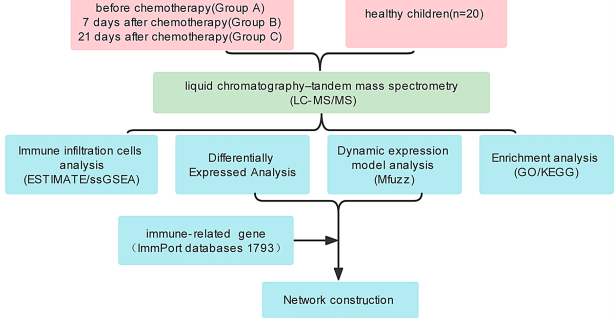
技术方法上,研究团队建立了标准化样本处理流程:采用10,000xg离心去除细胞碎片,25mm硝酸纤维素膜富集蛋白,改良FASP方法消化后,使用Orbitrap Exploris 480质谱仪进行DIA模式检测。数据分析采用Spectronaut Pulsar软件,设置Q值<0.01的严格阈值,并通过KNN算法填补缺失值。免疫分析将3483个免疫相关基因(IRGs)映射至蛋白质组数据,采用GeneMANIA构建蛋白互作网络。
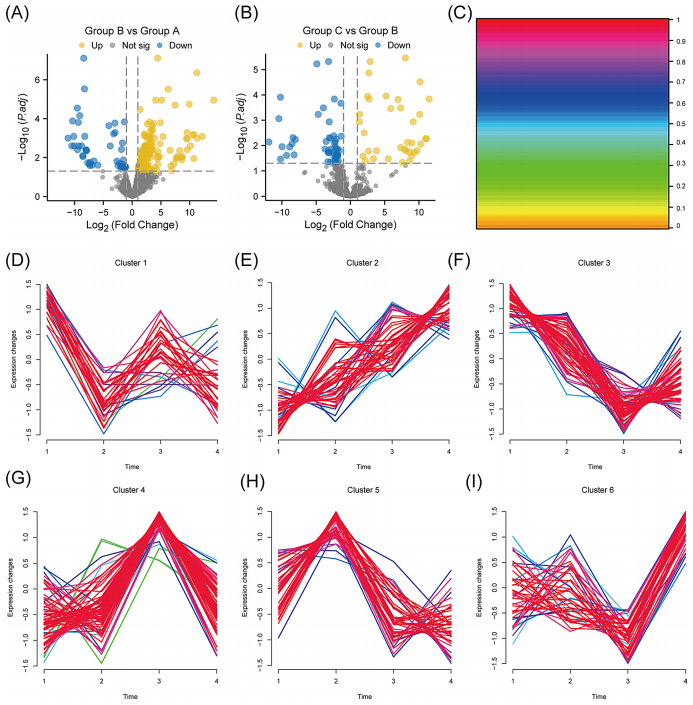
具体研究结果可分为四个维度:
免疫特征演变:ESTIMATE算法显示化疗7天后免疫评分骤降(P<0.01),21天组部分恢复。CIBERSORT分析证实CD8+ T细胞是主要变化亚群。
通路激活模式:差异蛋白显著富集于mTOR通路(Padj<0.05),其中ATP6V1系列蛋白介导的自噬保护与KRAS驱动的免疫抑制形成"双刃剑"效应。
关键靶点鉴定:19个差异表达免疫相关蛋白(DEIRPs)中,SEMA7A在化疗后呈现"V型"动态变化,与CD8+ T细胞浸润程度显著相关。
药物预测:CTD数据库筛选出四氯二苯并二噁英等7种可能作用于SEMA7A的化合物,为后续实验提供候选分子。

讨论部分指出,该研究首次建立神经母细胞瘤化疗后尿液蛋白质组图谱,提出mTOR通路双重调控机制假说:化疗早期mTORC1通过ATP6V1促进肿瘤细胞存活,而mTORC2则通过KRAS介导免疫逃逸。SEMA7A的发现尤为关键,既往研究显示其在头颈鳞癌中通过异常糖基化诱导CD8+ T细胞耗竭,本研究则揭示其在神经母细胞瘤化疗免疫调控中的新角色。预测化合物四氯二苯并二噁英已知可通过芳香烃受体(AHR)激活调节性T细胞,这为开发联合治疗方案提供思路。
这项研究的创新价值体现在三方面:方法学上开创尿液蛋白质组监测化疗反应的新范式;理论上阐明mTOR通路时空特异性激活机制;临床上为GD2疗法无效患者提供替代靶点。尽管存在样本量有限等局限,但研究提出的"SEMA7A-CD8+ T细胞-mTOR"调控轴为神经母细胞瘤精准免疫治疗开辟了新路径,未来可通过类器官模型和多中心队列进一步验证。
 生物通微信公众号
生物通微信公众号
知名企业招聘