
-

生物通官微
陪你抓住生命科技
跳动的脉搏
SPIDER算法:基于空间转录组解析配体-受体互作空间变异与功能支持的新方法
【字体: 大 中 小 】 时间:2025年08月22日 来源:Nature Communications 15.7
编辑推荐:
本研究针对空间转录组(ST)数据中配体-受体相互作用(LRIs)空间异质性识别难题,开发了SPIDER算法。通过构建容量约束的细胞互作界面,整合集体最优运输(COT)与共表达分析,结合下游转录因子(svTFs)功能验证,实现了空间变异相互作用(SVIs)的精准识别。该方法在PDAC和DLPFC等数据集验证中展现出优越性能,为揭示组织微环境细胞通讯提供了新工具。
在生命科学领域,细胞间的"对话"机制一直是研究的核心问题。就像人类社会需要语言交流,细胞也通过配体-受体相互作用(LRIs)传递信息,这些分子对话影响着胚胎发育、组织稳态和疾病进程。然而,传统技术如同"雾里看花",难以捕捉这些相互作用在复杂组织中的空间分布规律。随着空间转录组学(ST)技术的突破,科学家们终于获得了细胞通讯的"空间地图",但如何从中识别真正具有功能活性的空间变异相互作用(SVIs),仍是悬而未决的挑战。
这项发表在《Nature Communications》的研究提出了创新解决方案。研究人员意识到,现有的空间变异基因(SVG)分析方法无法直接应用于LRIs研究,主要面临两大障碍:一是LRIs信号产生于细胞间而非特定位置;二是随着ST数据分辨率提升,计算复杂度呈指数增长。更关键的是,缺乏功能验证会导致大量假阳性结果,如同没有"质检报告"的通讯记录,可靠性存疑。
为解决这些难题,Shiying Li等开发了SPIDER算法。该方法通过三个关键技术突破实现了SVIs的精准识别:首先采用功率图算法构建容量约束的细胞互作界面,反映细胞的实际通讯能力;其次整合集体最优运输(COT)和共表达分析来量化LRIs强度;最后引入下游转录因子(svTFs)的功能验证,确保发现的SVIs具有生物学意义。研究团队在胰腺导管腺癌(PDAC)和背外侧前额叶皮层(DLPFC)等多个数据集上验证了SPIDER的优越性能。
关键技术方法包括:1)基于功率图的容量约束界面建模;2)整合COT和共表达的LRIs评分;3)自组织映射(SOM)的界面抽象化;4)六种概率模型联合检测空间变异;5)基于知识图谱的svTFs功能验证。样本来源于公开的ST数据集,涵盖10x Visium、Slide-seq V2、seqFISH和Stereo-seq等多种平台。
研究结果部分,通过多个维度验证了SPIDER的创新价值:
"SPIDER在模拟数据集上的性能评估"显示,在99%相互作用强度下,SPIDER的AUC值达0.84,显著优于SpatialDM(0.701)和SpaTalk(0.697)。在特异性测试中,SPIDER平均值为0.848,远高于其他方法。这些数据证实了SPIDER在准确识别svTF支持的SVIs方面的优势。

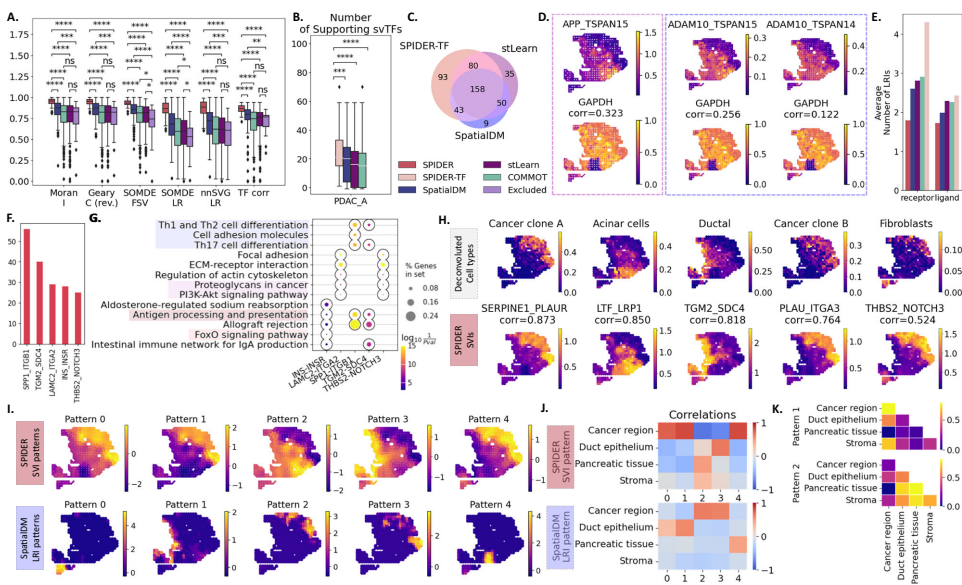
"真实PDAC数据集的分析"揭示,SPIDER识别的SVIs具有更高的空间自相关分数。例如TSPAN14/15信号通路中,只有APP-TSPAN15获得下游GAPDH的支持,而其他方法错误报告了无svTF支持的互作。GO分析显示SPIDER发现的SVIs显著富集癌症相关通路,如蛋白聚糖在癌症中(hsa05205)和PI3K-Akt信号通路(hsa04151)。
"单细胞分辨率样本的验证"部分,在seqFISH小鼠胚胎数据中,SPIDER成功识别了器官发育关键SVIs,如Kitt-Epor与红细胞生成(相关系数0.917),Bmp7-Acvr1与心肌细胞发育相关。更令人振奋的是,SPIDER揭示了大脑区域内Fgf15-Fgfr1和Sfrp1-Fzd2的空间特异性分布,为神经发育研究提供了新线索。
"空间互作模式的发现"方面,在Slide-seq V2小鼠海马数据中,SPIDER将SVIs聚类为7种空间模式。例如模式2与少突胶质细胞强相关(r=0.760),模式1富集神经营养因子信号,这些发现为理解神经环路的空间组织提供了新视角。
在"大块组织样本的应用"中,SPIDER在乳腺癌数据中区分了原位癌和浸润癌的特征SVIs,如HSP90AA1-ERBB2(原位癌标志,r=0.824)和THBS2-ITGB1(浸润癌标志,r=0.697)。值得注意的是,基于SVIs构建的伪时间轨迹比基因表达具有更高相关性(0.5752 vs 0.3967),展现了其在肿瘤进化研究中的独特价值。
研究结论部分强调,SPIDER的创新在于首次实现了空间变异与功能验证的结合,解决了现有方法假阳性率高的问题。通过容量约束界面建模和多模型集成,SPIDER能够适应不同分辨率的ST数据,从小鼠胚胎到人类癌症样本均表现出强大鲁棒性。特别值得关注的是,该方法揭示了64%的SVIs属于异型信号,为理解肿瘤微环境中细胞互作提供了新视角。
讨论部分指出,SPIDER的灵活框架允许用户自定义界面评分和空间变异检测方法,这种模块化设计使其能够整合未来更先进的CCI分析方法。研究者也坦诚指出界面抽象化在提升计算效率的同时,可能弱化微弱但重要的信号,这是未来需要优化
 生物通微信公众号
生物通微信公众号
知名企业招聘