
-

生物通官微
陪你抓住生命科技
跳动的脉搏
人类泛基因组揭示NPIP基因家族的结构变异、选择压力与功能分化
【字体: 大 中 小 】 时间:2025年08月23日 来源:Cell Genomics 9
编辑推荐:
研究人员针对人类核孔互作蛋白(NPIP)基因家族的功能未知但存在强烈正选择信号的特点,利用长读长测序技术解析了169个人类单倍型的结构变异,发现56%的NPIP蛋白模型未被报道,揭示了该家族通过基因转换和大规模倒位多态性驱动遗传不稳定性,同时通过组织特异性表达实现功能分化,为理解人类特异性基因家族的进化与疾病关联提供了新视角。
在灵长类进化过程中,NPIP(核孔互作蛋白)基因家族展现出惊人的扩张现象,尤其在人类和非洲猿类中表现出极强的正选择信号。这个神秘的基因家族不仅与核孔复合体存在潜在相互作用,更因其所在的LCR16a重复序列介导了人类16号染色体短臂10%区域的重复扩增,成为导致自闭症、发育迟缓等神经精神疾病的热点区域。然而,由于该家族成员间高度相似的序列特征,传统短读长测序技术难以准确解析其变异谱系,使得这个在进化上备受"青睐"的基因家族的功能机制长期成谜。
为破解这一难题,Dishuck等研究团队在《Cell Genomics》发表最新成果,首次基于169个人类单倍型的长读长组装数据,结合1.4亿条全长转录本测序,绘制了NPIP家族在人类群体中的完整变异图谱。研究主要采用三大技术手段:一是利用PacBio HiFi和ONT超长读长测序完成高精度单倍型组装;二是通过多序列比对和最大似然法构建NPIP系统发育树;三是整合384个Iso-seq文库的转录组数据解析组织特异性表达模式。
结构变异与进化动力学
研究揭示NPIP拷贝数在人类群体中存在显著差异(21-33拷贝),非洲人群显著高于其他群体。通过构建包含4665个NPIP位点的系统发育树,鉴定出28个亚型,其中NPIPB2、B11和B14为拷贝数恒定位点。研究发现NPIP通过基因转换(IGC)维持序列同质性,且转换方向呈现明显偏倚――祖先位点NPIPA1仅作为供体向远端16p位点转移序列。更引人注目的是,NPIP介导了4个常见倒位多态性(350kb-1.6Mb),其中16p13.11位点的545kb倒位在人群中占比达69%。
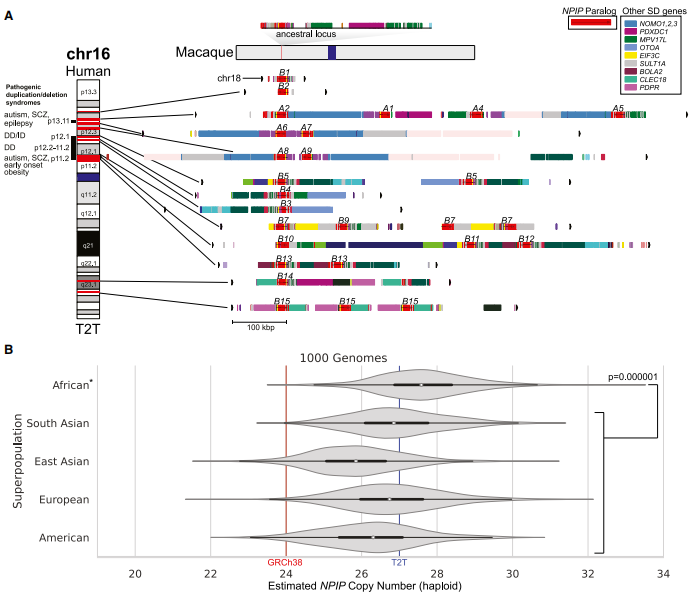
持续的正选择信号
群体遗传学分析显示,NPIPB9和B15在Tajima's D和nSL检验中均位列染色体16正向选择信号前1%,另有9个位点进入前5%。值得注意的是,这些选择信号在排除基因转换区域后仍然显著,提示其可能反映真实的适应性进化。位于倒位边界附近的NPIPB3-B9可能通过抑制重组维持了优势单倍型。
基因模型与功能分化
研究重构出55个主要异构体,其中56%为首次报道。关键发现包括:1)人类特异的NPIPB亚群获得ACSM1基因衍生的"MVKL"起始序列;2)B6-B15亚型含有预测的信号肽和跨膜结构域;3)NPIPB3-B5等亚型携带可形成β螺旋的可变数目串联重复(VNTR),其拷贝数在个体间存在差异;4)发现10种PKD1-NPIP融合转录本,最长编码843个氨基酸。表达谱分析揭示NPIPA5、B12/B13等亚型在脑组织中特异性高表达,而B1、B2等则保留睾丸特异性表达模式。
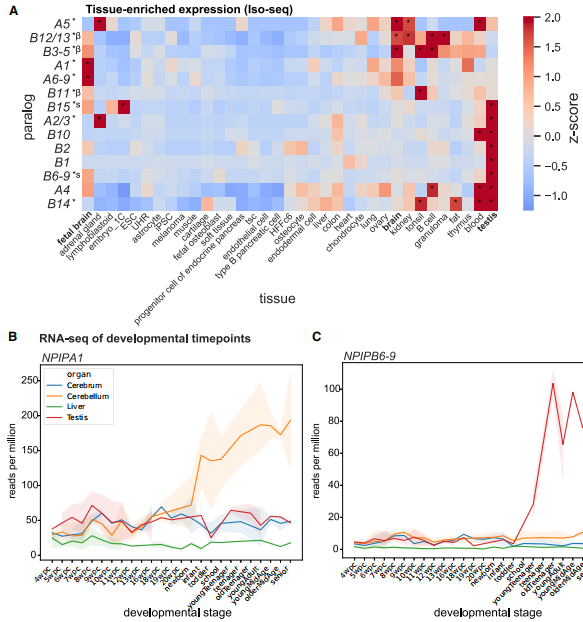
这项研究首次系统揭示了NPIP基因家族在人类群体中的动态进化格局,阐明了结构变异与正选择的相互作用机制。特别值得注意的是,尽管NPIP相关重排导致多种疾病风险,但自然选择仍维持其高度多态性,暗示该家族可能在人类特有性状(如脑发育)中发挥重要作用。发现的β螺旋结构域、组织特异性异构体等分子特征,为后续功能研究提供了明确靶点。该成果不仅为理解人类基因组"暗物质"的进化意义树立了新范式,更为神经发育疾病的精准诊断提供了结构变异参考图谱。
 生物通微信公众号
生物通微信公众号
知名企业招聘