
-

生物通官微
陪你抓住生命科技
跳动的脉搏
综述:提高精准医学中致病性胚系变异诊断率的当前最佳实践与未来机遇
《Human Genomics》:Increasing pathogenic germline variant diagnosis rates in precision medicine: current best practices and future opportunities
【字体: 大 中 小 】 时间:2025年08月24日 来源:Human Genomics 4.3
编辑推荐:
这篇综述系统探讨了提高精准医学(precision medicine)中致病性变异诊断率的最新技术与策略,涵盖测序技术(WGS/WES/scRNA-Seq)、变异注释工具(VEP/ANNOVAR)、家系分析(segregation analysis)及机器学习(ML/LLM)应用,为构建模块化、可扩展的多组学分析框架提供了关键设计原则。
现代精准医学依赖多样化的测序技术,从靶向基因面板到全基因组测序(WGS),每种方法各具优劣。靶向测序成本低且适用于已知致病基因的疾病,但无法检测新变异或大片段变异。全外显子测序(WES)覆盖85%的致病突变区域,而WGS凭借全面检测小变异、拷贝数变异(CNV)和结构变异的能力,逐渐成为临床首选。新兴的单细胞测序(scRNA-Seq/scDNA-Seq)和长读长测序技术(如PacBio/ONT)进一步解决了细胞异质性和复杂重复序列的检测难题,但数据稀疏性和高错误率仍是技术瓶颈。
高效的变异筛选需结合样本选择、家系分析和多层级注释。极端表型患者分组或家系测序可显著缩小候选变异范围,例如通过人类表型本体(HPO)术语标准化表型描述。家系分析中,符合孟德尔遗传规律的共分离变异(如ACMG分类中的PP1证据)能强化致病性判定,而健康携带者则提示不完全外显率。
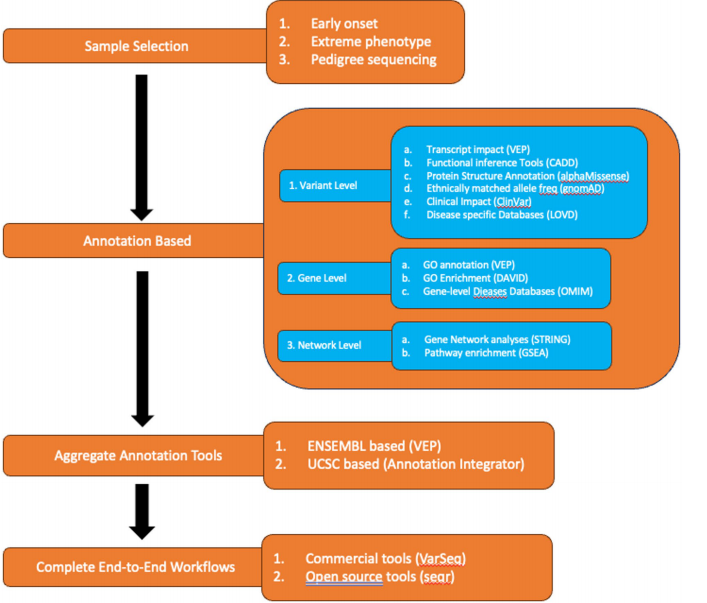
变异注释工具(如VEP/AlphaMissense)通过整合基因组坐标、蛋白结构预测(AlphaFold2)和群体频率数据库(gnomAD),区分良性多态性与致病突变。临床数据库ClinVar和HGMD提供致病性证据,但需警惕文献来源的假阳性记录。
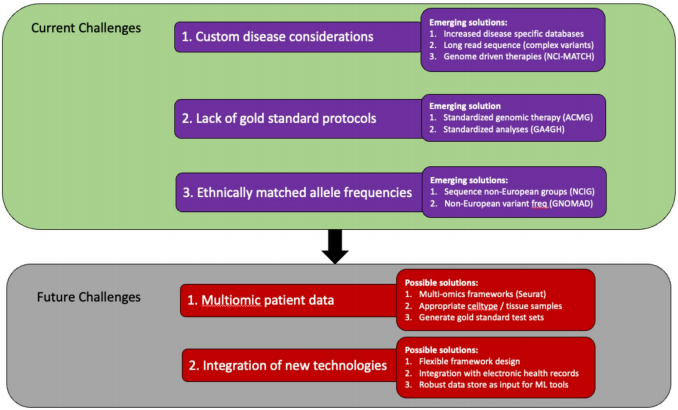
机器学习模型(如REVEL/DeepVariant)在变异致病性预测中表现突出,但“黑箱”决策机制和训练数据偏差限制临床转化。大语言模型(LLM)如EvAgg可加速文献挖掘,却难以处理复杂遗传互作。当前挑战包括多组学数据整合(如微生物组与宿主基因组互作)、电子健康记录(EHR)的动态关联,以及伦理敏感的种族多样性数据库建设(如All of Us计划)。
成功的精准医学系统需具备模块化、可扩展性和安全性,支持实时更新ACMG标准与新兴数据流。临床报告需平衡自动化与人工审核,例如通过NextFlow实现流程可重复性。未来,跨平台标准化和实时变异重分类将推动个性化医疗从理论迈向实践。
 生物通微信公众号
生物通微信公众号