
-

…˙ŒÔÕ®πŸŒ¢
≈„ƒ„◊•◊°…˙√¸ø∆ºº
ï∂صƒ¬ˆ≤´
ª˘”⁄∑¥œÚ“þ√Á—ßµƒ∂ý“©ƒÕ“©…À∫Æ…≥√≈ œæ˙√‚“þ‘≠–‘ƒ§µ∞∞◊∞–µ„º¯∂®”κ∆À„ª˙∏®÷˙“þ√Á…˺∆
°æ◊÷ã∫ ¥Û ÷– –° °ø ±º‰£∫2025ƒÍ08‘¬24»’ ¿¥‘¥£∫BMC Microbiology 4.2
±ýº≠Õ∆ºˆ£∫
°°°°±æ—–æø’Î∂‘∂ý“©ƒÕ“©(MDR)…À∫Æ…≥√≈ œæ˙(S. Typhimurium)»±∑¶”––ß“þ√Áµƒœ÷◊¥£¨≤…”√∑¥œÚ“þ√Á—ß(Reverse vaccinology)Ω·∫œº∆À„ª˙ƒ£ƒ‚ºº ı£¨¥”4,446∏ˆµ∞∞◊÷–…∏—°≥ˆ9÷÷∏þ√‚“þ‘≠–‘ƒ§µ∞∞◊∞–µ„(Q7CQX2/Q7CQW9µ»)£¨Õ®π˝øπ‘≠–‘(°ð0.9)°¢∑«π˝√Ù‘≠–‘°¢±ÌŒª‘§≤‚(ABCpred/IEDB)º∞√‚“þƒ£ƒ‚(C-ImmSim)—È÷§£¨Œ™ø™∑¢π„∆◊∂ý±ÌŒª“þ√ÁÃ·π©–¬≤þ¬‘°£
‘⁄»´«Úπ´π≤Œ¿…˙¡Ï”Ú£¨…À∫Æ…≥√≈ œæ˙(Salmonella Typhimurium) º÷’ «ª”÷Æ≤ª»•µƒÕ˛–≤°£’‚÷÷∏Ô¿º“ı–‘∏Àæ˙Õ®π˝Œ€»æ ≥ŒÔ∫ÕÀÆ‘¥¥´≤•£¨√øƒÍµº÷¬≥¨π˝50ÕÚ¿˝«÷œÆ–‘∑«…À∫Æ…≥√≈æ˙≤°(iNTS)£¨‘⁄∂˘ÕØ∫Õ√‚“þ»±œð»À»∫÷–À¿Õˆ¬ æ”∏þ≤ªœ¬°£∏¸º¨ ÷µƒ «£¨∏√≤°‘≠Ó—Ω¯ªØ≥ˆ∂ý÷ÿƒÕ“©(MDR)ƒÐ¡¶£¨∂‘∞±Ð–Œ˜¡÷°¢¬»√πÀÿµ»“ªœþøπ…˙Àÿ≤˙…˙ƒÕ“©–‘£¨Õ¨ ±Õ®π˝–Œ≥……≥√≈æ˙∫¨æ˙ø’≈ð(SCV)∫Õº§ªÓPhoP-PhoQœµÕ≥µ»ª˙÷∆Ô±Ð√‚“þ«Â≥˝°£æ°πÐ∂،ԓþ√Á»ÁPoulvac ST“—Õ∂»Î π”√£¨»À¿ý“þ√Á—–∑¢»¥≥§∆⁄Õ£÷Õ°™°™¥´Õ≥∞–œÚ±Þ√´µ∞∞◊∫Õ÷¨∂ýë(LPS)µƒ“þ√Á¥Ê‘⁄—™«Â–ÕÃÿ“Ï–‘«ø°¢§ƒ§√‚“þ≥÷æ√–‘≤ª◊„µ»»±œð°£
Œ™Õª∆∆’‚“ª¿ßæ÷£¨Tooba Umeµ»—–æø’þ¡Ì±ŸıËæ∂£¨≤…”√∑¥œÚ“þ√Á—ß’‚“ª∏Ô√¸–‘≤þ¬‘°£∏√ºº ı≤ª“¿¿µ≤°‘≠ÃÂ≈ý—¯£¨÷±Ω”¥”ª˘“Ú◊È÷–Õ⁄æÚ«±‘⁄“þ√Á∞–µ„°£Õ≈∂”—°‘ÒÕÍ»´≤‚–ÚµƒLT2æ˙÷Í◊˜Œ™ƒ£–Õ£¨Õ®π˝Àƒº∂…∏—°ÃÂœµ£∫ ◊œ»”√SOSUI∑˛ŒÒ∆˜¥”4,446∏ˆµ∞∞◊÷–À¯∂®1,228∏ˆƒ§µ∞∞◊£ªΩ”◊≈“‘VaxiJen v2.0(„–÷µ°ð0.9)…∏—°≥ˆ15∏ˆ∏þøπ‘≠–‘µ∞∞◊£ª‘Ÿæ≠AllerTOP∫ÕToxinPredÃÞ≥˝3∏ˆπ˝√Ù/∂æ–‘µ∞∞◊£ª◊Ó∫ÛÕ®π˝C-ImmSim√‚“þƒ£ƒ‚ÑÃ≠3∏ˆµÕœÏ”¶µ∞∞◊°£πÿº¸ µ—Ⱥº ı∞¸¿®£∫1) ª˘”⁄SOSUIµƒƒ§µ∞∞◊‘§≤‚£ª2) VaxiJenøπ‘≠–‘∆¿∑÷£ª3) ABCpred/IEDB±ÌŒª‘§≤‚£ª4) C-ImmSim√‚“þœÏ”¶ƒ£ƒ‚£ª5) ProtParam/TMHMM¿ÌªØ–‘÷ ∑÷Œˆ°£
øπ‘≠–‘∆¿π¿
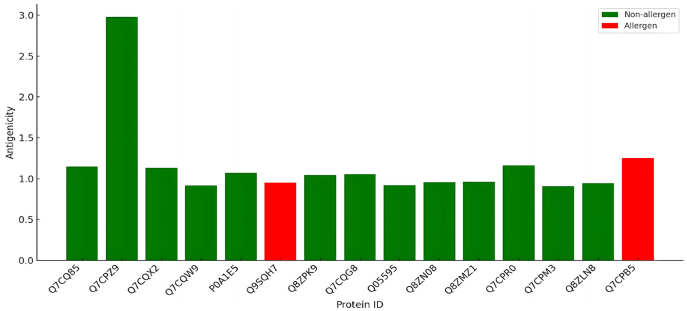
Õ®π˝VaxiJen∑÷ŒˆªÒµ√15∏ˆøπ‘≠÷µ£æ0.9µƒƒ§µ∞∞◊£¨∆‰÷–P0A1E5(curli÷˜“™—«ª˘)øπ‘≠÷µ¥Ô2.25£¨œ‘÷¯∏þ”⁄¥´Õ≥∞–µ„OmpA(0.7-0.8)°£
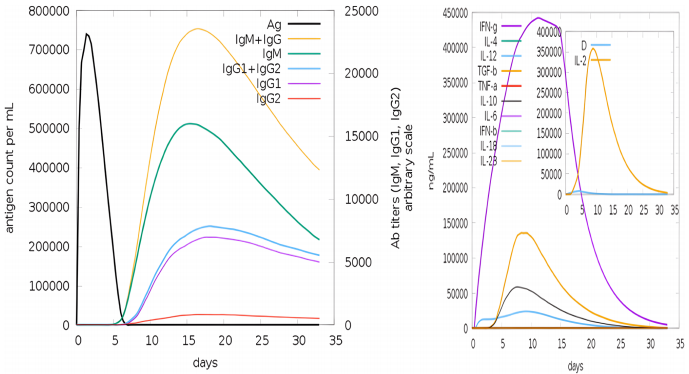
√‚“þƒ£ƒ‚∑÷Œˆ
Q7CQG8( …æ˙ÖðøÀµ∞∞◊B)‘⁄ƒ£ƒ‚÷–“˝∑¢œ‘÷¯IgG/IgM∑¥”¶∫ÕIFN-¶√∑÷√⁄°£
±ÌŒª‘§≤‚
ABCpredº¯∂®≥ˆQ7CQW9(΃æ€Ã«œýπÿ÷¨µ∞∞◊)∫¨6∏ˆBœ∏∞˚±ÌŒª£¨◊Ó∏þ∑÷0.86°£∆‰MHC-I±ÌŒªFLRSNPSYKVΩ·∫œ¡¶¥Ô3.57nM£¨
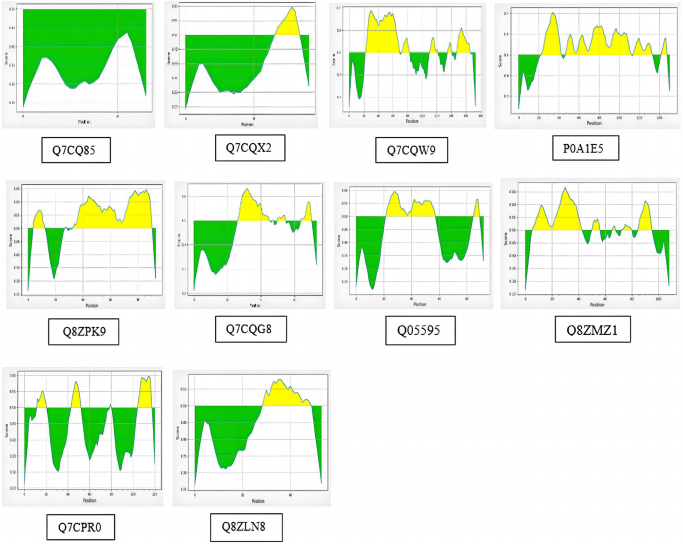
±£ ÿ–‘—È÷§
À˘”–∫Ú—°µ∞∞◊‘⁄MDRæ˙÷ÍDT104÷–±£≥÷100%–Ú¡–Õ¨“ª–‘£¨∆‰÷–Q7CPR0(ƒ⁄ƒ§µ∞∞◊)∫¨3∏ˆøÁƒ§¬ð–˝£¨

’‚œÓ∑¢±Ì”⁄°∂BMC Microbiology°∑µƒ—–æøø™¥¥–‘µÿº¯∂®≥ˆ9∏ˆ–¬–Õ“þ√Á∞–µ„£¨∆‰“‚“‘⁄”⁄£∫1) ◊¥ŒœµÕ≥∆¿π¿ƒ§µ∞∞◊◊˜Œ™…À∫Æ…≥√≈ œæ˙“þ√Á∞–±Íµƒ«±¡¶£ª2) ∑¢œ÷΃æ€Ã«œýπÿ÷¨µ∞∞◊(Q7CQW9)ºÊæþTLR2º§∂غ¡π¶ƒÐ£¨ø…‘ˆ«ø◊Ùº¡–ß”¶£ª3) ±ÌŒª…˺∆πʱСÀ»À¿ýÕ¨‘¥–Ú¡–£¨ΩµµÕ◊‘…Ì√‚“þ∑Áœ’°£Ãÿ±÷µµ√◊¢“‚µƒ «£¨±£ ÿ–‘∑÷Œˆ÷§ µ’‚–©∞–µ„‘⁄MDRæ˙÷Í÷–∏þ∂»±£ ÿ£¨Œ™”¶∂‘øπ…˙ÀÿŒ£ª˙÷π©¡À–¬Àº¬∑°£Œ¥¿¥—–æø–Ë‘⁄∂،ԃ£–Õ÷–—È÷§’‚–©º∆À„ª˙‘§≤‚Ω·π˚£¨≤¢ÃΩÀ˜∂ý±ÌŒª“þ√Á”΃…√◊‘ÿúº ıµƒΩ·∫œ”¶”√°£
 …˙ŒÔÕ®Œ¢–≈π´÷⁄∫≈
…˙ŒÔÕ®Œ¢–≈π´÷⁄∫≈
÷™√˚∆Û“µ’–∆∏
ΩÒ»’∂Øè | »À≤≈ –≥° | –¬ºº ı◊®¿∏ | ÷–π˙ø∆—ß»À | ‘∆’πî | BioHot | ‘∆Ω≤Ã√÷±≤• | ª·’π÷––ƒ | Ãÿº€◊®¿∏ | ºº ıøÏ—∂ | √‚∑— ‘”√
∞Ê»®À˘”– …˙ŒÔÕ®
Copyright© eBiotrade.com, All Rights Reserved
¡™œµ–≈œ‰£∫
‘¡ICP±∏09063491∫≈