
-

生物通官微
陪你抓住生命科技
跳动的脉搏
靶向EGFR突变的新型诊疗一体化探针OSA-Cy7的构建及其在非小细胞肺癌中的应用研究
【字体: 大 中 小 】 时间:2025年08月27日 来源:BMC Biotechnology 3.4
编辑推荐:
本研究针对EGFR-TKIs(酪氨酸激酶抑制剂)疗效预测的临床难题,开发了基于第三代EGFR-TKI奥希替尼(Osimertinib)的近红外荧光探针OSA-Cy7。该探针通过特异性识别EGFR激活突变(19del/L858R/T790M),实现了对非小细胞肺癌(NSCLC)的分子影像诊断与靶向治疗同步进行,为EGFR突变患者的精准诊疗提供了新型theranostic(诊疗一体化)策略。
肺癌是全球癌症死亡的首要原因,其中非小细胞肺癌(NSCLC)占比超过85%。表皮生长因子受体(EGFR)作为NSCLC的关键驱动基因,其酪氨酸激酶域突变(如19号外显子缺失/19del和L858R)患者对EGFR酪氨酸激酶抑制剂(TKI)治疗敏感。然而临床面临两大困境:一是传统基因检测存在样本获取困难、灵敏度不足等问题;二是约10%携带敏感突变患者对TKI无应答,而部分无突变患者反而获益。更棘手的是,50%以上患者使用第一/二代TKI后会产生T790M耐药突变。第三代TKI奥希替尼虽能克服T790M耐药,但仍缺乏配套的疗效预测工具。
针对这些挑战,Dong Ying团队在《BMC Biotechnology》发表研究,创新性地将奥希替尼与近红外荧光染料Cy7偶联,构建了首个基于第三代TKI的诊疗一体化探针OSA-Cy7。该探针兼具分子影像与靶向治疗双重功能:通过近红外荧光成像可视化EGFR突变状态,同时保留奥希替尼的抗肿瘤活性。
研究采用三步关键技术:1)通过丙烯酸连接臂合成奥希替尼-Cy7偶联物;2)采用CCK-8和克隆形成实验评估抗增殖效应;3)结合Western blot和流式细胞术验证靶向性。实验选用PC9(19del)、H1975(L858R/T790M)和A549(野生型)三种NSCLC细胞系。
选择性靶向突变EGFR细胞系
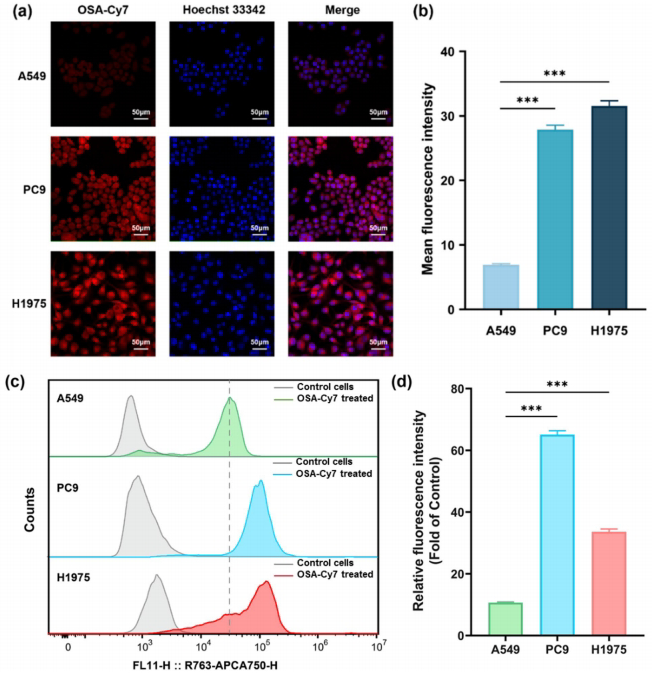
荧光成像显示,OSA-Cy7在突变型PC9和H1975细胞的摄取量分别是野生型A549细胞的4.3倍和3.8倍(P<0.001)。流式数据证实,突变细胞的平均荧光强度(MFI)较对照组提升5-7倍,而游离Cy7无此选择性。
抗增殖与EGFR磷酸化抑制
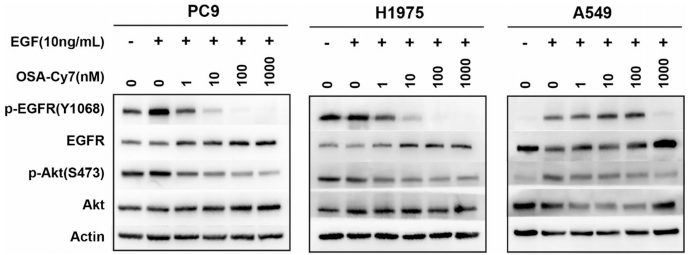
CCK-8实验显示OSA-Cy7对突变细胞的IC50与奥希替尼相当(均<1μM),克隆形成率降低70%-85%。Western blot揭示其可剂量依赖性抑制EGFR和AKT磷酸化,但对野生型EGFR无显著影响。
这项研究突破性地实现了第三代TKI疗效预测与治疗的同步化。OSA-Cy7的创新性体现在:1)首次将奥希替尼改造为分子影像探针;2)近红外成像(750/780nm)具备深层组织穿透优势;3)保留不可逆结合Cys797的特性,可监测T790M/C797S耐药突变。尽管需进一步验证体内稳定性,该研究为NSCLC精准医疗提供了新型工具,未来或可应用于术中导航、耐药监测等临床场景。
 生物通微信公众号
生物通微信公众号
知名企业招聘