
-

生物通官微
陪你抓住生命科技
跳动的脉搏
综述:肿瘤转移中的中性粒细胞胞外诱捕网:机制与治疗意义
【字体: 大 中 小 】 时间:2025年08月28日 来源:Discover Oncology 2.9
编辑推荐:
这篇综述系统阐述了中性粒细胞胞外诱捕网(NETs)在肿瘤微环境中的形成机制及其双重作用。作者详细解析了NETs通过整合素(integrins)、Toll样受体(TLR4/9)、活性氧(ROS)等通路促进肿瘤转移、血管生成和免疫逃逸的分子机制,同时探讨了DNase I、PAD4抑制剂等靶向治疗策略的临床转化潜力。文中特别强调了NETs与CD8+T细胞耗竭、血小板活化间的复杂互作,为肿瘤免疫治疗提供了新视角。
中性粒细胞胞外诱捕网在肿瘤转移中的多维调控机制
NETs的形成与调控
中性粒细胞胞外诱捕网(NETs)是由DNA骨架、组蛋白和抗菌蛋白组成的网状结构。其形成受NADPH氧化酶依赖和非依赖两条通路调控:前者通过ROS激活肽酰精氨酸脱亚胺酶4(PAD4)促进组蛋白瓜氨酸化;后者则通过钙离子内流和TLR信号触发。肿瘤微环境中,粒细胞集落刺激因子(G-CSF)和IL-8通过CXCR1/2受体激活Src-p38-ERK通路,显著促进NETs释放。
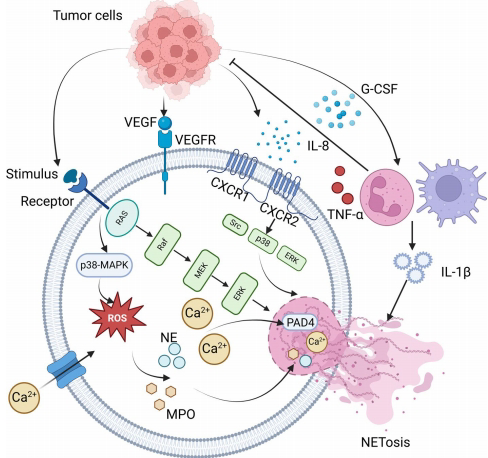
NETs与肿瘤微环境互作
NETs通过αvβ3、α5β1等整合素捕获循环肿瘤细胞(CTCs),并激活β1-整合素/IL-17A通路促进转移灶形成。在胰腺癌中,NETs通过PAD4依赖途径形成纤维化屏障保护肿瘤细胞;而乳腺癌转移则与NETs激活HMGB1/TLR9信号密切相关。值得注意的是,NETs表面携带的PD-L1可通过代谢重编程诱导CD8+T细胞耗竭,这种免疫抑制效应在放疗后微环境中尤为显著。
NETs的促转移作用
• 血管生成:NETs中的髓过氧化物酶(MPO)和中性粒细胞弹性蛋白酶(NE)通过降解细胞外基质,暴露出层粘连蛋白新表位,激活α3β1整合素信号唤醒休眠肿瘤细胞
• 血栓形成:肿瘤源性外泌体诱导的NETs可作为凝血因子支架,在胰腺癌患者中与静脉血栓栓塞风险正相关
• 代谢重编程:NETs释放的脂质被肿瘤细胞摄取后,上调线粒体生物合成基因并增强ATP合成
靶向治疗策略
临床前研究显示:
DNase I降解NETs的DNA骨架可减少CTC捕获,在乳腺癌肝转移模型中降低67%转移负荷
PAD4抑制剂GSK484通过阻断组蛋白瓜氨酸化,使胰腺癌纤维化屏障厚度减少40%
抗IL-8抗体联合CXCR1/2抑制剂Reparixin可逆转NETs介导的PD-1抑制剂耐药
传统中药成分如丹参酮IIA通过抑制MMP-9减少NETs形成,而黄连汤则下调PAD4表达。这些发现为开发基于NETs的肿瘤分级诊疗策略提供了理论依据。
展望
尽管NETs在抗感染中具有保护作用,但其在肿瘤中的双重效应仍需精准调控。未来研究需明确不同肿瘤发展阶段NETs的功能异质性,并探索靶向NETs联合免疫检查点抑制剂的协同治疗方案。
 生物通微信公众号
生物通微信公众号
知名企业招聘