
-

生物通官微
陪你抓住生命科技
跳动的脉搏
Shh信号通过拮抗Wnt通路调控小鼠颅底软骨发育的分子机制研究
【字体: 大 中 小 】 时间:2025年08月28日 来源:BMC Biology 4.5
编辑推荐:
本研究针对颅底软骨过早闭合的发育机制难题,通过Vismodegib部分抑制Sonic hedgehog(Shh)信号,首次建立颅底早闭小鼠模型。研究发现E10.5时期Shh与Wnt信号在颅底原基共激活,Shh通过拮抗Wnt/β-catenin信号维持颅底软骨正常发育节奏,该机制为颅面畸形治疗提供新靶点。论文发表于《BMC Biology》。
颅底作为连接颅脑与躯干的关键结构,其发育异常会导致颅面畸形综合征。虽然已知Indian hedgehog(Ihh)通过PTHrP途径调控软骨细胞分化,但Sonic hedgehog(Shh)在颅底早期发育中的作用仍不清楚。传统基因敲除方法因导致胚胎早期死亡而受限,这成为研究颅底发育分子机制的瓶颈。
为突破这一限制,Jiangping Chen等研究人员创新性地采用小分子抑制剂Vismodegib建立条件性Shh信号干扰模型。通过不同剂量(50-200 mg/kg)的E10.5阶段性干预,发现150 mg/kg剂量组在维持胚胎存活的同时,能诱导E17.5小鼠出现颅底软骨过早闭合的典型表型。研究运用micro-CT三维重建、免疫荧光染色、RNAscope原位杂交等技术,系统揭示了Shh-Wnt信号对话在颅底发育中的时空调控规律。
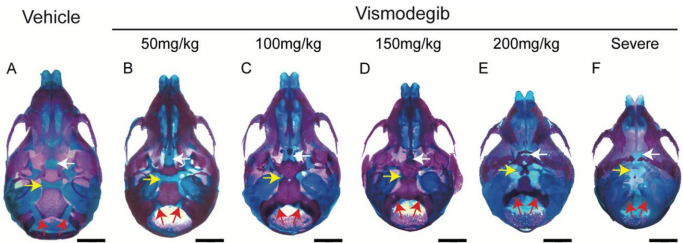
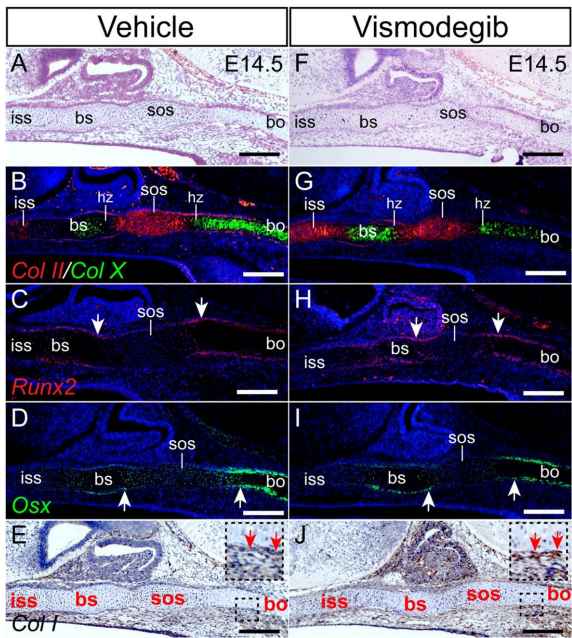
剂量依赖性表型分析显示,50 mg/kg仅引起基枕软骨(IOS)部分融合,而200 mg/kg则导致颅底中央结构缺失,重现Shh基因敲除表型。这种梯度效应首次证明Shh信号强度与颅底发育存在剂量依赖关系。通过Alcian blue/alizarin red染色时序分析发现,Vismodegib处理组在E14.5前颅底模式正常,但E15.5开始出现IOS过早骨化,E16.5-E17.5时蝶枕软骨(SOS)和蝶间软骨(ISS)出现加速肥大分化,表现为ColX表达区域扩展和ColII区域缩短。
与Ihh缺陷模型不同,Vismodegib处理组的Ptch1、Gli1和PTHrP表达未受抑制,软骨细胞增殖标记Phh3反而增强。关键发现出现在E10.5-E12.5发育窗口期:RNAscope检测显示E10.5颅底原基中Shh与Wnt通路共激活而Bmp信号静默;E11.5短暂抑制Shh后,E12.5颅底软骨腹侧间充质细胞出现β-catenin核转位及Lef1/Runx2异位表达。这种Wnt信号异常激活先于软骨分化加速现象,提示腹侧软骨膜细胞命运改变可能是颅底早闭的始动因素。
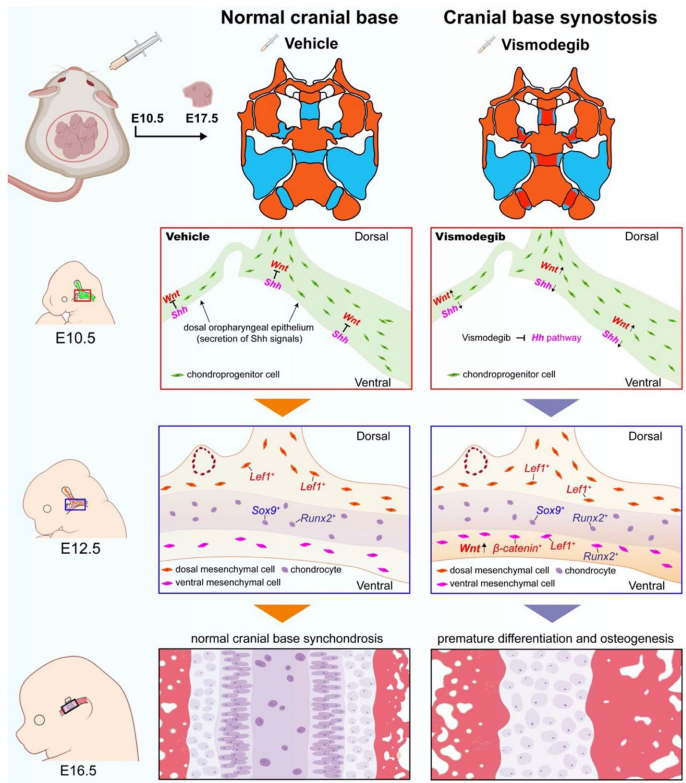
研究结论创新性提出"Shh-Wnt拮抗"调控模式:背侧口咽上皮分泌的Shh通过抑制腹侧Wnt/β-catenin信号,维持颅底软骨膜前体细胞的稳态。这种时空特异性调控机制解释了临床观察到的颅底发育异常谱系――从部分软骨早闭到完全性颅底缺失都可能源于Shh信号梯度变化。该发现为Apert综合征等颅缝早闭疾病的分子分型提供了理论依据,并提示靶向信号通路串扰可能是未来治疗方向。
这项研究的技术亮点在于:建立可调控的Shh信号干扰动物模型;采用多组学方法(组织学染色、三维成像、分子标记检测)进行表型-机制关联分析;首次揭示颅底腹侧软骨膜细胞的命运决定机制。论文通过精巧的实验设计,解决了传统基因敲除方法无法研究的发育生物学问题,为颅面畸形发病机制研究开辟了新途径。
 生物通微信公众号
生物通微信公众号
知名企业招聘