
-

生物通官微
陪你抓住生命科技
跳动的脉搏
光生物调节疗法逆转唑来膦酸对牙周膜间充质干细胞存活与分化的抑制作用及其机制研究
【字体: 大 中 小 】 时间:2025年08月30日 来源:Scientific Reports 3.9
编辑推荐:
本研究针对双膦酸盐类药物(如唑来膦酸ZA)导致的颌骨坏死(MRONJ)临床难题,创新性探讨了980 nm与635 nm波长光生物调节疗法(PBMT)对ZA暴露下牙周膜间充质干细胞(PDLMSCs)的干预效果。通过MTT法、ALP活性检测及实时PCR等技术,首次证实980 nm激光(4 J/cm2)可显著提升细胞存活率(P<0.001),促进矿化结节形成(P<0.001),并上调OCN、OPN、RUNX2等成骨基因表达,为MRONJ的临床防治提供了新型非侵入性治疗策略。
在口腔医学领域,双膦酸盐类药物(如唑来膦酸ZA)虽能有效治疗骨质疏松和骨转移癌,但其引发的药物相关性颌骨坏死(MRONJ)却成为临床棘手难题。这种病症表现为颌骨暴露坏死,常规治疗收效甚微。究其根源,ZA会直接损伤牙周膜间充质干细胞(PDLMSCs)――这些细胞是牙周组织再生和骨修复的关键"种子细胞"。当PDLMSCs的存活和成骨分化能力被ZA抑制,颌骨的自我修复机制便陷入瘫痪。面对这一困境,研究者将目光投向了光生物调节疗法(PBMT),这种利用特定波长激光调控细胞行为的无创技术,能否成为逆转ZA毒性的"光之钥匙"?
为验证这一设想,研究团队设计了一套严密的实验体系。关键技术包括:采用MTT法检测24/72小时细胞活力,通过Alizarin red染色定量矿化结节形成,使用实时PCR分析OCN、OPN、RUNX2等成骨标志基因表达,并测定碱性磷酸酶(ALP)活性评估早期分化。所有实验均使用人源PDLMSCs(IBRC C11326细胞系),在5 μM ZA暴露条件下比较635 nm与980 nm激光(2/4 J/cm2)的干预效果。
细胞存活结果显示:ZA使PDLMSCs存活率显著降低,而980 nm激光展现出惊人挽救效果。24小时时,4 J/cm2组存活率甚至超越对照组(P<0.001);72小时时,980 nm各剂量组及635 nm高剂量组均显著逆转ZA毒性(P<0.05)。
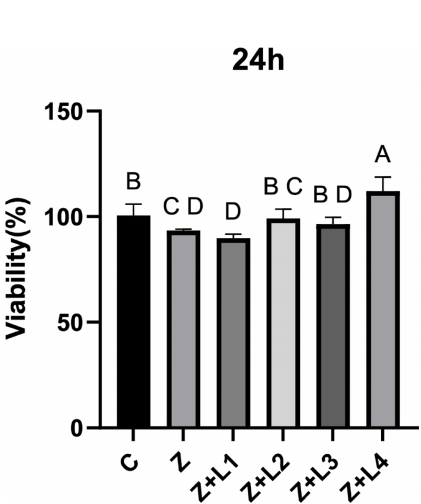
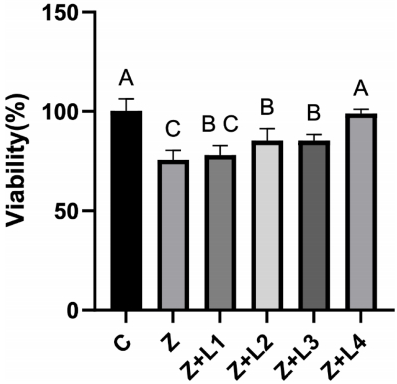
矿化能力分析中,980 nm激光组的表现尤为亮眼。Alizarin red染色显示,其矿化结节形成量较ZA组增加近27%(P<0.001),且呈现剂量依赖性。
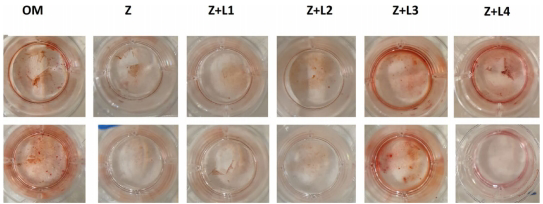
分子机制探索揭示了更深入的发现:980 nm激光能同时上调OCN(成熟期标志)、OPN(基质矿化调控因子)和RUNX2(成骨分化主调控因子)的表达(P<0.001),形成完整的成骨分化调控网络。而635 nm激光则呈现"双刃剑"效应:2 J/cm2促进OPN但4 J/cm2抑制OCN,说明红光波长存在能量密度依赖的复杂调控。
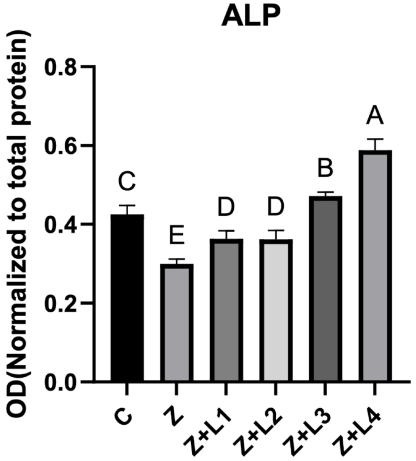
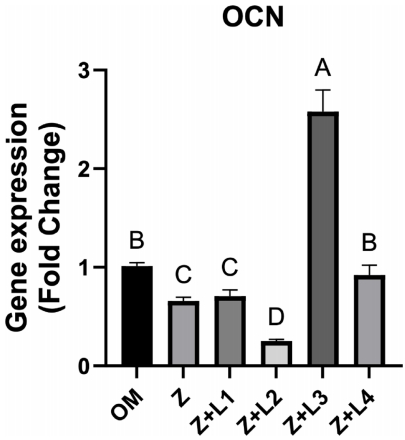
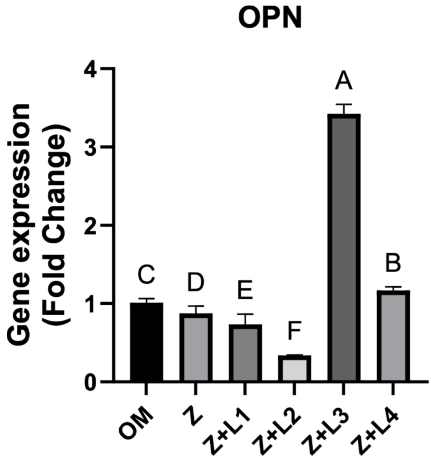
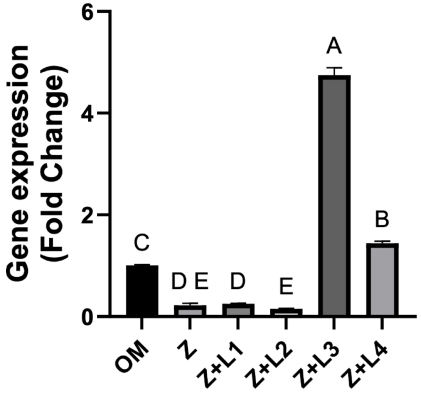
这项发表于《Scientific Reports》的研究首次系统比较了不同波长PBMT对ZA毒性干预的差异,证实980 nm激光(4 J/cm2)能通过多重机制协同作用:既保护PDLMSCs免受ZA诱导的凋亡,又激活RUNX2-OPN-OCN信号轴促进成骨分化。这为临床MRONJ防治提供了精准的光疗参数――相较于传统660 nm波长,980 nm激光具有更深组织穿透性,能更好作用于颌骨深部干细胞。研究者特别指出,该技术可整合到拔牙创照射、牙周治疗等临床场景,在ZA用药患者中建立"光保护屏障"。未来研究需进一步探索PBMT与现有治疗方案(如PRF、抗生素)的协同效应,并开展动物模型验证。这项成果不仅为MRONJ治疗开辟新途径,更为干细胞光调控研究提供了重要范式。
 生物通微信公众号
生物通微信公众号
知名企业招聘