
-

生物通官微
陪你抓住生命科技
跳动的脉搏
基于深度学习的CBCT合成CT在鼻咽癌自适应放疗中的自动分割精度与剂量计算一致性研究
【字体: 大 中 小 】 时间:2025年08月30日 来源:Radiation Oncology 3.2
编辑推荐:
本研究针对鼻咽癌(NPC)自适应放疗(ART)中人工依赖度高的问题,开发了基于Cycle-GAN的CBCT合成CT(sCT)技术,结合深度学习自动分割和GPU加速蒙特卡洛剂量计算,实现了靶区与危及器官(OAR)的高精度分割(DSC>0.85)和剂量评估。结果显示该方法能准确捕捉解剖结构变化(如腮腺体积减少26.5%),剂量差异控制在临床可接受范围(GTVn D99偏差-1.44Gy),为常规直线加速器实现高效ART提供了新思路。
鼻咽癌(NPC)作为头颈部常见恶性肿瘤,调强放疗(IMRT)虽已显著提升疗效,但治疗过程中肿瘤退缩、体重下降等解剖变化常导致剂量偏差,引发口干等副作用。传统自适应放疗(ART)依赖频繁CT扫描和人工勾画,耗时耗力;而在线ART需专用磁共振直线加速器(MR-Linac),基层医院难以普及。锥形束CT(CBCT)虽广泛配备,却因散射伪影等问题无法直接用于精确剂量计算。如何利用现有设备实现高效ART,成为临床亟待解决的难题。
为解决这一瓶颈,Weijie Lei团队在《Radiation Oncology》发表研究,创新性地将深度学习与常规直线加速器相结合。通过16例接受两阶段离线ART的NPC患者数据,采用独立数据集训练的Cycle-GAN生成合成CT(sCT),结合改进的2D Unet和3D nnUNet模型实现自动分割,并利用GPU加速蒙特卡洛算法进行剂量重计算。研究通过Dice相似系数(DSC)和95%豪斯多夫距离(HD95)评估几何精度,并分析剂量体积参数差异。
关键技术方法
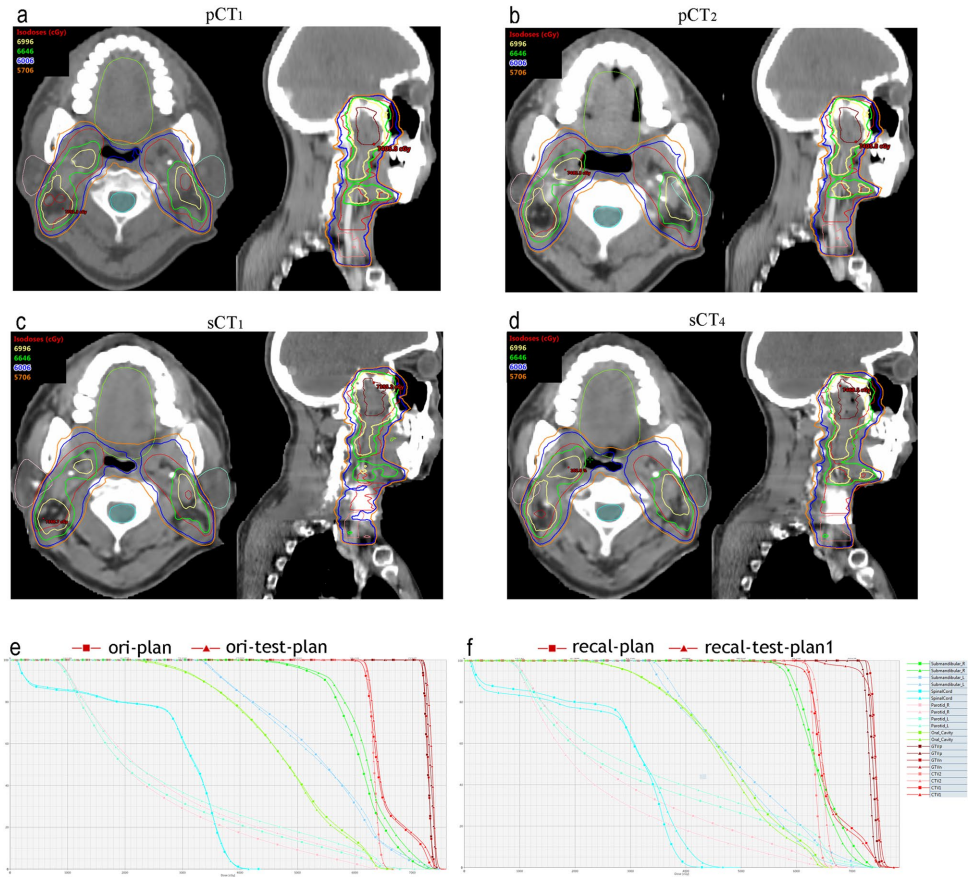
研究纳入16例II-III期NPC患者,采集初始(pCT1)和自适应(pCT2)计划CT及每周CBCT。采用ArcherQA平台实现三大核心步骤:(1)基于Cycle-GAN生成sCT;(2)改进神经网络自动分割靶区(GTVp/GTVn)和危及器官(腮腺/颌下腺);(3)GPU蒙特卡洛剂量重计算。对比分析sCT与金标准pCT的剂量差异,并通过Spearman相关性评估体积变化与计划调整的关联。
自动分割精度
靶区结构中CTV1/CTV2表现最优(DSC>0.91),GTVn因软组织对比度不足精度最低(DSC=0.43)。腮腺(PG)分割一致性最高(DSC>0.88),颌下腺(SG)次之(DSC=0.64-0.73)。值得注意的是,基于pCT2-CBCT4配对的sCT4*在GTVp分割中显著优于非配对组(ΔDSC=0.06),证实时间相近的影像配对可提升精度。
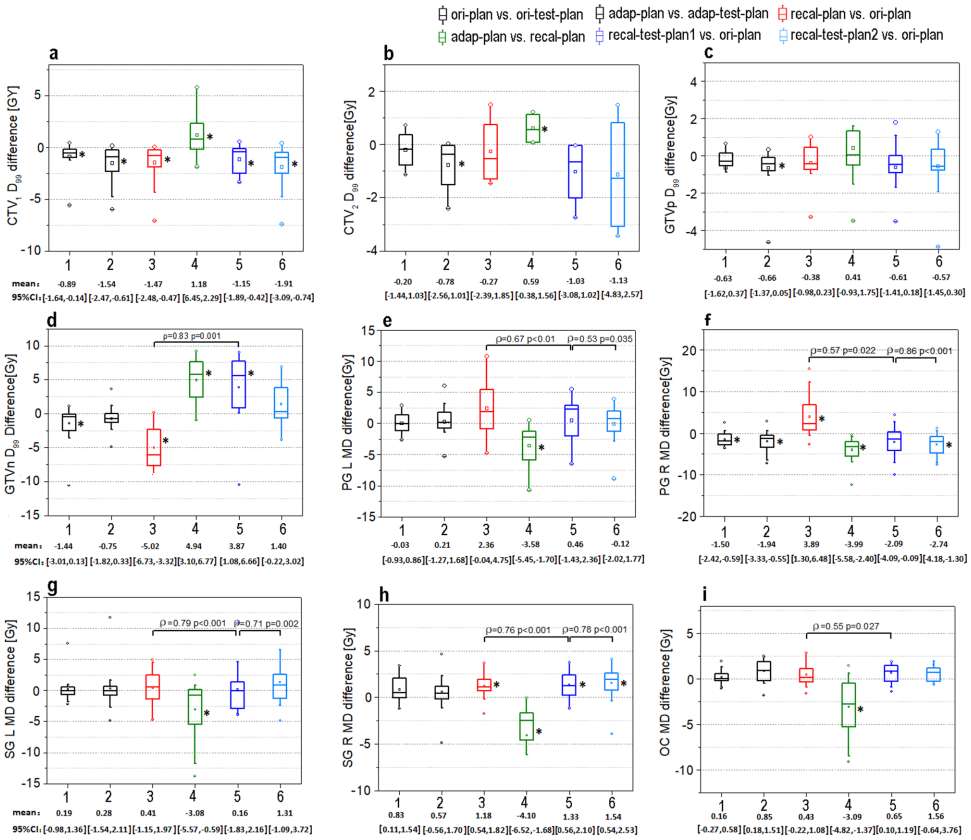
剂量计算一致性
sCT剂量差异具有结构特异性:CTV1 D99偏差-1.54Gy,GTVn D99偏差-1.44Gy。右侧腮腺平均剂量差异达-1.94Gy(p<0.05),与体积变化显著相关(r=0.72)。自适应计划(adap-plan)较非调整计划(recal-plan)显著降低OAR剂量,如左侧腮腺MD减少3.58Gy(p<0.05),验证了sCT指导ART的临床价值。
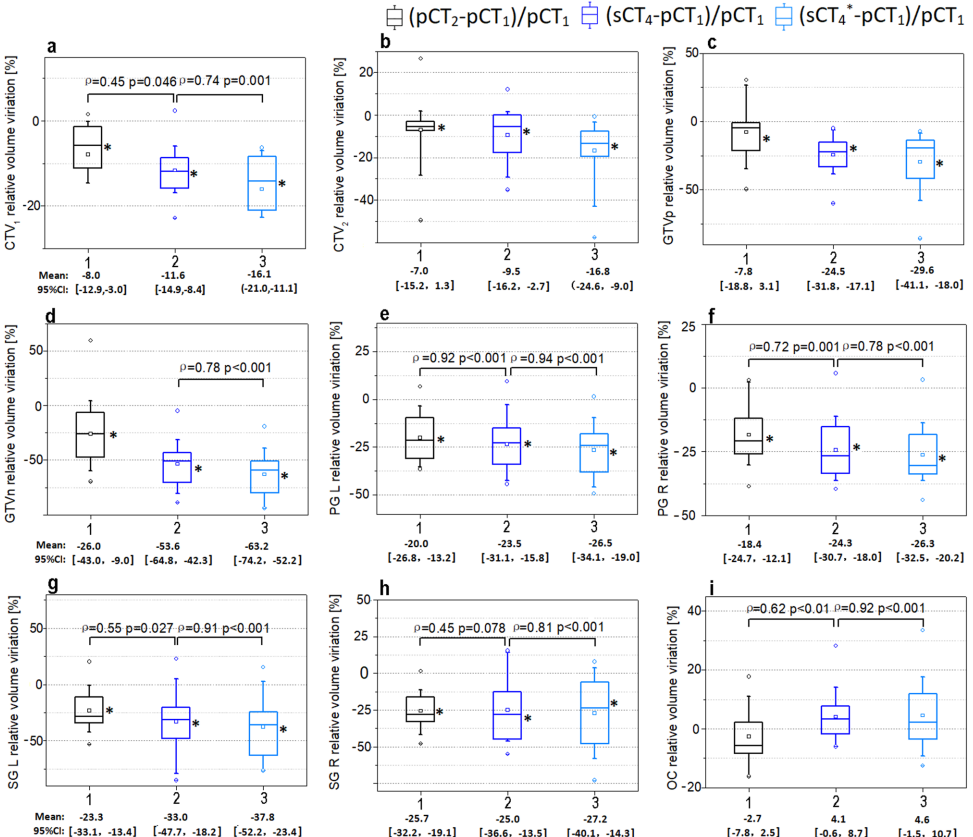
解剖变化监测
sCT成功捕捉到治疗中关键变化:CTV1体积缩减16.1%,GTVn缩减63.2%,右侧腮腺体积减少26.3%。这些变化与离线ART计划调整高度相关(r>0.78),证实sCT可替代CT监测解剖演变。
结论与意义
该研究首次在常规C臂直线加速器上实现NPC全流程自动化ART评估,将单次评估时间压缩至秒级。虽然GTVn等小靶区仍需人工复核,但该方法显著降低了ART对硬件和人力资源的依赖。尤为重要的是,研究揭示了sCT衍生的体积变化与剂量偏差的定量关系,为建立标准化ART触发阈值提供了理论依据。未来通过扩大训练数据集、优化网络架构,有望进一步提升小靶区和低对比度组织的分割精度,推动精准放疗在基层医院的普及。
 生物通微信公众号
生物通微信公众号
知名企业招聘