
-

生物通官微
陪你抓住生命科技
跳动的脉搏
胶原结构紊乱特征(CoDA)在结肠癌临床分子分型及预后预测中的多组学关联研究
【字体: 大 中 小 】 时间:2025年08月30日 来源:npj Precision Oncology 8
编辑推荐:
本研究针对结肠癌(CC)肿瘤微环境(TME)中胶原结构量化评估的临床需求,开发了基于全切片图像(WSI)的计算病理学流程,从2212例多中心患者中提取胶原紊乱架构(CoDA)特征。研究通过随机森林分类和LASSO-Cox模型证实,CF Fragmentation等5个特征可有效区分临床分期、CMS分子亚型(CMS1-4)及KRAS/BRAF突变状态(AUC≥0.7),其风险评分对总生存期(OS)和无病生存期(DFS)具有独立预测价值(HR=1.45-1.65)。该成果为结肠癌精准诊疗提供了新型数字化生物标志物。
在全球范围内,结肠癌(Colon Cancer, CC)长期占据癌症发病率和死亡率的前三位,其五年生存率在转移阶段骤降至13%。尽管AJCC TNM分期系统仍是临床决策的基石,但越来越多的证据表明,肿瘤微环境(TME)中细胞外基质(ECM)的重塑――尤其是胶原纤维(Collagen Fiber, CF)的结构变化,深刻影响着肿瘤的侵袭转移和药物抵抗。然而,传统病理评估难以量化这些微妙的结构特征,且CMS分子分型、RAS突变状态等关键指标依赖耗时昂贵的基因检测。这种技术瓶颈在医疗资源匮乏地区尤为突出,亟需开发可替代的数字化评估工具。
针对这一挑战,研究团队在《npj Precision Oncology》发表了突破性成果。该研究创新性地构建了胶原紊乱架构(Collagen Disorder Architecture, CoDA)分析框架,从常规H&E染色切片中提取CF Fragmentation(碎片化)、Bundling(成束)、Anisotropy(各向异性)、Density(密度)和Rigidity(刚性)五大特征。研究纳入了PLCO、TCGA等四大数据库共2212例患者数据,采用基于导数高斯模型(DtG)的CF检测算法,结合随机森林分类和LASSO-Cox回归等机器学习方法,系统评估了CoDA特征的临床关联性与预后价值。
关键技术方法
研究团队首先通过QuPath软件手动标注训练集(TCGA 81例+UH 50例)的肿瘤区域,采用ResNet18卷积神经网络实现全自动肿瘤分割。利用HistoQC工具剔除脂肪组织和伪影区域后,从600×600像素的肿瘤-间质区域提取图像块,应用导数高斯(DtG)模型识别线性胶原结构。最终通过五种定量算法计算患者水平的CoDA特征值,并在PLCO队列训练预后模型,于TCGA、UH和Emory数据集进行独立验证。
CoDA特征与临床病理参数的关联
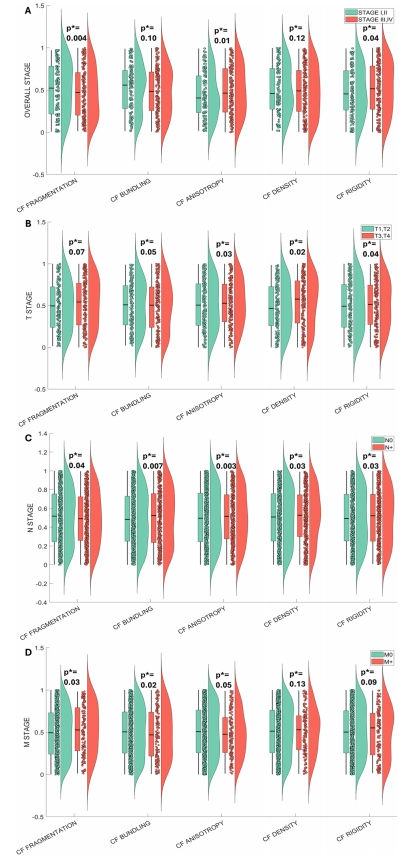
通过Mann-Whitney U检验发现,所有CoDA特征均与AJCC分期显著相关(p<0.05),其中CF Anisotropy在N分期中差异最显著(p=0.003)。分子层面,CMS1亚型显示更高的CF Fragmentation(p=0.006),而CMS3则与CF Bundling密切关联(p=0.02)。基因突变分析揭示,BRAF突变组在所有CoDA特征上均呈现显著差异,KRAS突变组则特异性影响CF Bundling(p=0.007)。随机森林模型验证了这些特征的判别力,对BRAF突变状态的分类AUC高达0.85±0.10。
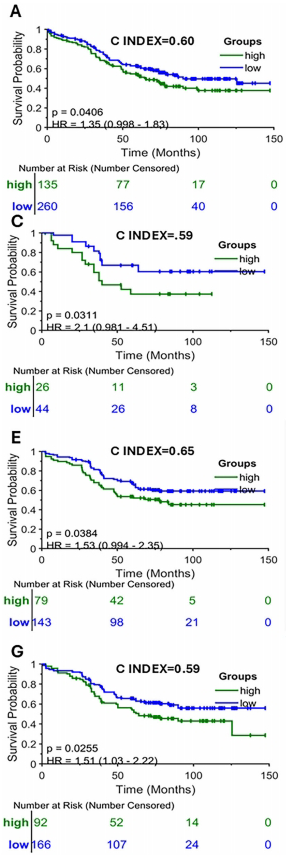
预后风险分层效能
LASSO-Cox模型生成的CoDA风险评分在验证集中展现出强劲的预后预测能力。对于III-IV期患者,高风险组的总生存期显著缩短(HR=1.45, 95%CI:1.10-1.91),且该指标独立于CMS分型和KRAS状态存在。值得注意的是,CMS4患者虽然临床预后较差,但CoDA低风险组仍显示出生存优势(HR=0.56, p=0.014),提示胶原结构可能反映独特的TME生物学特性。在DFS预测中,CF Rigidity对KRAS突变患者的风险分层效果尤为突出(p=0.015)。
多变量分析验证
在调整年龄、种族等混杂因素后,CoDA风险评分仍保持独立预后价值(OS: p=0.008; DFS: p=0.0006)。与其他生物标志物相比,其预测效能超越了单个分子特征,如KRAS突变(HR=2.05)或CMS4分型(HR=0.56)。种族差异分析显示,黑人患者虽然总体预后较差(DFS: HR=1.33),但CoDA模型在此亚群中仍保持稳定预测性能。
这项研究开创性地建立了胶原结构量化与结肠癌精准医疗的桥梁。其技术突破在于:首次实现H&E切片中CF架构的自动化定量,克服了Masson染色非标准化的局限;开发的CoDA特征不仅与COL1A1等促转移基因表达谱相呼应,还能通过常规病理切片预测RAS突变状态,为资源有限地区提供了替代检测方案。临床转化方面,该模型可识别MEK/SRC抑制剂潜在获益人群,特别是CMS4和KRAS突变亚型。未来研究可探索CoDA特征与免疫治疗响应的关联,或结合其他TME组分构建综合预测系统。这项成果标志着计算病理学在结直肠癌领域迈入三维微环境建模的新纪元。
 生物通微信公众号
生物通微信公众号
知名企业招聘