
-

生物通官微
陪你抓住生命科技
跳动的脉搏
全基因组转录分析揭示抗氧化防御系统、氨基酸代谢和抗原呈递在乳糜泻发病机制中的关键作用
【字体: 大 中 小 】 时间:2025年08月31日 来源:BMC Medicine 8.3
编辑推荐:
本研究通过全基因组RNA测序技术,对283例肠道黏膜和外周血样本进行多表型分析,揭示了乳糜泻(CD)患者中7565个肠道差异表达基因和542个血液差异表达基因。研究发现免疫球蛋白重链可变区5-51(IGHV5-51)和组织转谷氨酰胺酶(TGM2)在肠道活检中显著上调,同时鉴定出Nrf2通路、谷胱甘肽代谢、mTORC1信号等关键通路在CD发病中的调控作用,为理解该疾病的分子机制提供了新视角。
乳糜泻(CD)是一种由麸质触发、具有遗传易感性的自身免疫性疾病,其特征是肠道绒毛萎缩和针对组织转谷氨酰胺酶(TG2)的自身抗体产生。尽管HLA-DQ2/DQ8单倍型被确认为主要遗传风险因素,但非HLA基因和环境因素在疾病发生中的作用机制仍不清楚。现有研究多聚焦于活动期CD的肠道病变特征,而对潜在CD(血清学阳性但无肠道损伤)和治疗后CD的分子特征缺乏系统认识,这限制了对疾病发生发展全过程的理解。
为全面解析CD的分子机制,?sa Torinsson Naluai团队在《BMC Medicine》发表了突破性研究。该研究创新性地整合了72例CD患者(包括活动期、潜在期和治疗后)和73例对照的283份肠道活检及外周血样本,采用全基因组RNA测序技术进行多组学分析。通过limma-voom和edgeR包进行差异表达分析,结合Enrichr通路富集方法,系统绘制了CD不同临床阶段的分子图谱。
研究发现活动期CD患者肠道中IGHV5-51(p=1.05×10-14)和TGM2(p=5.29×10-10)表达显著上调,外周血中HLA-DQB1、HLA-DQB2和GSTM1差异最显著。研究首次揭示:1)Nrf2(核因子E2相关因子2)通路与谷胱甘肽代谢紊乱在氧化应激调控中的核心作用;2)SLC22A4基因编码的麦角硫因转运体下调可能影响抗氧化防御;3)mTORC1(哺乳动物雷帕霉素靶蛋白复合体1)信号与氨基酸代谢重编程的关联;4)MHC I类抗原呈递缺陷与CD8+T细胞反应的异常激活。
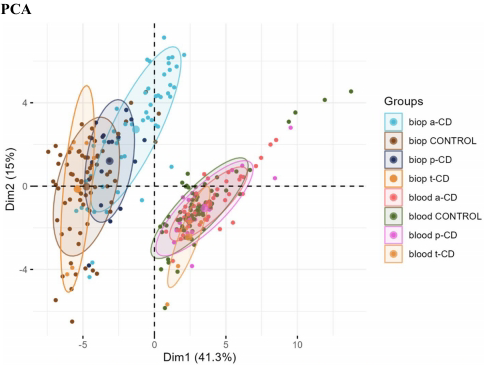
关键技术方法包括:1)从瑞典四家儿科诊所收集经内镜确诊的CD患者样本,严格按ESPGHAN标准分组;2)使用Illumina Stranded Total RNA建库试剂盒进行全转录组测序;3)采用GRCh38/hg38参考基因组进行序列比对;4)运用limma-voom算法进行差异表达分析;5)通过Enrichr进行通路富集分析。
主要研究结果
差异表达特征:活动期CD患者肠道中鉴定出7565个差异基因(5244个经多重检验校正),LPL基因表达上调最显著(log2FC=3.6)。治疗后CD患者MAP3K20-AS基因表达异常升高4.79倍。
氧化应激通路:Nrf2通路相关基因(HMOX1、GCLC、GCLM)显著下调,而谷胱甘肽S-转移酶GSTM1在血液中上调4.32倍。麦角硫因转运体SLC22A4表达降低1.32倍。
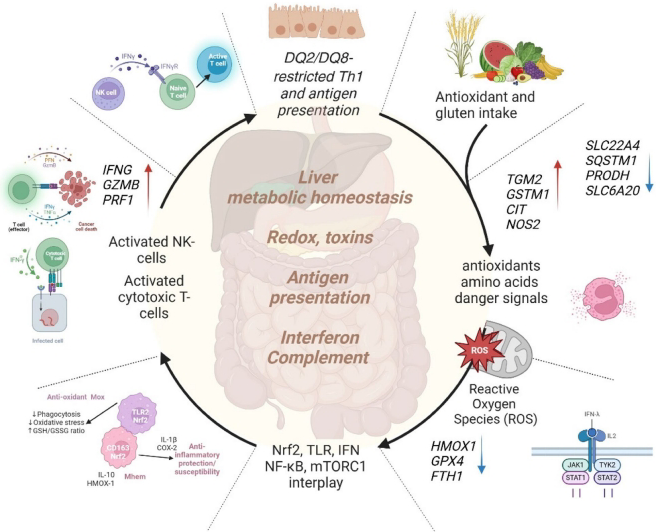
免疫调控机制:抗原加工基因TAP1/TAP2和蛋白酶体亚基PSMB8/9显著上调。NLRC5基因表达在治疗后CD仍维持高水平,提示持续CD8+T细胞活化。BTN3A家族基因在肠道中特异性高表达。
多表型比较:潜在CD患者苦味受体TAS2R基因家族表达独特,可能通过激活Nrf2维持黏膜完整性。治疗后CD仍保留HLA-DQB2等基因异常表达模式。
该研究首次系统阐明了CD不同临床阶段的分子特征,提出氧化应激-代谢重编程-免疫激活的三维发病模型。发现麦角硫因转运障碍、mTORC1信号异常等新机制,为开发靶向抗氧化通路(如Nrf2激活剂)和代谢干预策略提供了理论依据。临床价值在于:1)建立基于多组织基因表达谱的疾病分型标准;2)鉴定潜在CD的生物标志物;3)为无麸质饮食疗效监测提供分子指标。研究局限性包括样本量较小(尤其治疗后CD仅6例),未来需开展蛋白质组学验证。
这项多中心研究通过创新性的实验设计和生物信息学分析,深化了对CD发病机制的理解,为开发新型诊疗策略奠定了重要基础。特别值得注意的是,研究发现即使在黏膜愈合状态下,某些分子异常仍然持续存在,这为解释CD患者长期并发症风险提供了新视角,对临床管理具有重要指导意义。
 生物通微信公众号
生物通微信公众号
知名企业招聘