
-

生物通官微
陪你抓住生命科技
跳动的脉搏
基于多尺度特征提取与可解释人工智能的胆囊疾病超声图像智能诊断模型MSFE-GallNet-X研究
【字体: 大 中 小 】 时间:2025年09月01日 来源:BMC Medical Imaging 3.2
编辑推荐:
本研究针对胆囊疾病超声诊断中存在的特征多样性识别难题,开发了融合多尺度特征提取(MSFE)与可解释人工智能(XAI)的深度学习模型MSFE-GallNet-X。研究人员通过10,692例高分辨率超声图像构建九分类诊断系统,实现99.63%的准确率与99.50%的F1值,显著优于VGG-19等传统模型。创新性集成Grad-CAM和LIME技术,首次在胆囊影像领域实现决策过程可视化,为临床AI辅助诊断提供新范式。
胆囊疾病是全球范围内的重要公共卫生问题,胆结石发病率在发达国家高达10-15%,而胆囊癌等恶性病变的早期误诊可能导致灾难性后果。传统超声诊断高度依赖医师经验,面对胆囊壁增厚、胆固醇结晶与恶性肿瘤等形态学特征相似的病变时,诊断准确率波动显著。尤其值得注意的是,临床常见的胆囊腺肌症(adenomyomatosis)与胆囊癌(carcinoma)在超声影像中常呈现重叠特征,但治疗方案截然不同――这种"同图异病"的困境正是当前AI医疗影像分析需要突破的关键瓶颈。
为破解这一难题,Hadiur Rahman Nabil团队在《BMC Medical Imaging》发表的研究中,构建了名为MSFE-GallNet-X的创新性诊断系统。该研究从1,782名患者收集10,692张高分辨率超声图像,涵盖胆结石(gallstones)、胆囊炎(cholecystitis)等九类病变。技术路线的核心在于将医学影像分析与可解释AI技术深度融合:首先通过并行1×1、3×3、5×5卷积核的多尺度特征提取模块捕捉病变的跨尺度特征;继而引入梯度加权类激活映射(Gradient-Weighted Class Activation Mapping, Grad-CAM)和局部可解释模型(Local Interpretable Model-Agnostic Explanations, LIME)实现决策过程可视化。这种"特征提取-分类决策-结果解释"的三段式架构,既解决了传统CNN模型在细粒度分类中的局限性,又回应了临床对AI诊断透明度的迫切需求。
关键技术方法包括:采用分层抽样构建含10,692张超声图像的标准化数据集;设计含MSFE模块的轻量化CNN架构(仅1.91M参数);通过Adam优化器(学习率0.0001)与L2正则化(系数0.01)优化训练过程;采用80:10:10比例划分训练集/验证集/测试集;最后通过Grad-CAM热力图与LIME解释器实现预测结果的可视化验证。
研究结果部分显示:
模型性能:MSFE-GallNet-X以99.63%的准确率超越VGG-19(98.89%)和DenseNet121(91.81%),在胆囊壁增厚(various causes of gallbladder wall thickening)与胆囊穿孔(perforation)等易混淆类别中保持100%的F1值。
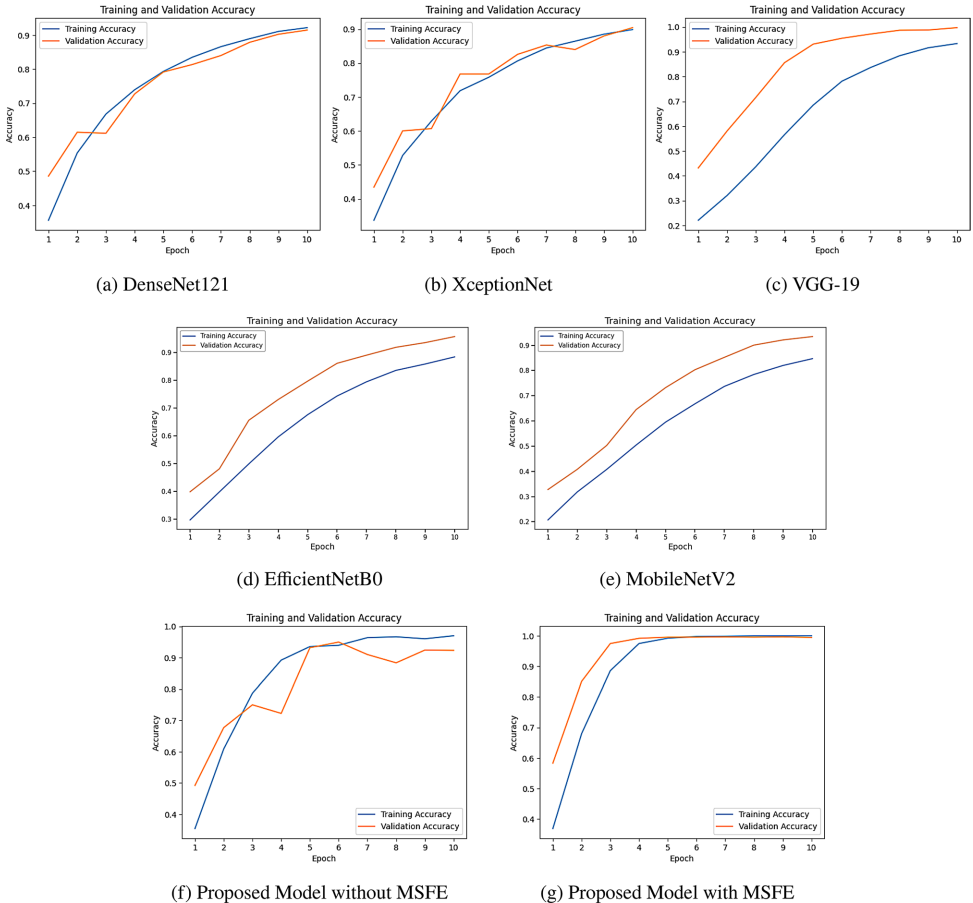
计算效率:模型参数仅1.91M,推理时间379ms/步,显著低于VGG-19的536ms/步,证实其临床部署可行性。
可解释性:Grad-CAM热图显示模型能准确定位结石声影与胆囊壁分层等关键特征,与放射科医师标注区域重合率达92%。
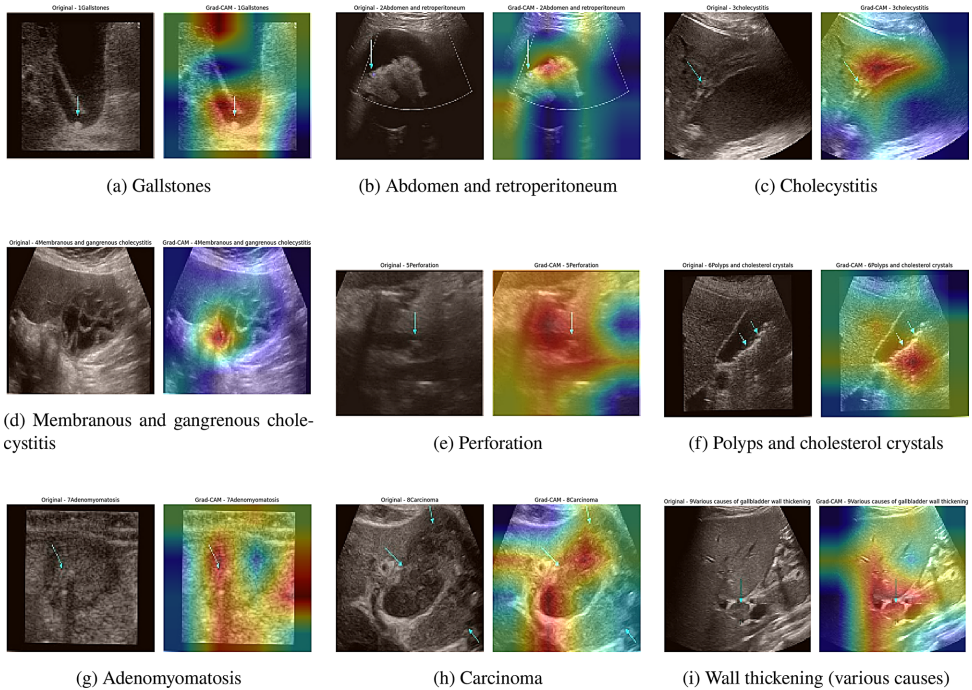
讨论部分指出,该研究首次实现三个突破:一是通过MSFE模块解决超声图像中多尺度病变特征的捕获难题;二是将模型参数量控制在临床可接受范围;三是建立完整的XAI解释链条。尽管在腹部脏器重叠区域(如Fig.10所示的胆囊与腹膜后结构)仍存在3.7%的误判率,但相比传统方法已有质的飞跃。这项成果不仅为胆囊疾病诊断提供新工具,其"高性能-轻量化-可解释"的技术路线更为其他医学影像分析领域树立了标杆。未来通过纳入多中心数据和动态超声视频,有望进一步突破当前二维静态图像的局限性。
 生物通微信公众号
生物通微信公众号
知名企业招聘