
-

生物通官微
陪你抓住生命科技
跳动的脉搏
基于印刷电解质门控聚合物场效应晶体管的心肌细胞动作电位无创记录技术
【字体: 大 中 小 】 时间:2025年09月01日 来源:Nature Communications 15.7
编辑推荐:
研究人员针对传统膜片钳技术侵入性强、通量低的问题,开发了基于喷墨印刷P3HT(聚3-己基噻吩)的电解质门控有机场效应晶体管(EGOFET),实现了人源诱导多能干细胞分化心肌细胞(hiPSC-CMs)动作电位(AP)的高保真无创记录,成功检测药物诱导的早后除极(EADs)等心律失常信号,为心脏疾病模型构建和药物筛选提供了高通量新工具。
在心脏疾病研究和药物开发中,准确记录心肌细胞动作电位(Action Potential, AP)至关重要。传统膜片钳技术虽能精确测量AP,但存在侵入性强、细胞存活率低、通量受限等问题。尽管微电极阵列(MEAs)和三维纳米器件等替代方案不断涌现,它们仍需膜穿孔操作或面临信号保真度不足的挑战。如何实现非侵入、高通量且高保真的AP记录,成为领域内亟待突破的技术瓶颈。
这项发表于《Nature Communications》的研究提出创新解决方案:利用喷墨印刷的有机半导体聚合物聚3-己基噻吩(P3HT)构建电解质门控场效应晶体管(EGOFET),成功实现人源诱导多能干细胞分化心肌细胞(hiPSC-CMs)AP的无创记录。研究团队通过优化器件结构与细胞界面耦合,使AP信号幅度达50 mV,成功率超90%,且能灵敏捕捉药物诱导的早后除极(EADs)等病理特征。该技术兼具膜片钳的信号质量与MEAs的高通量潜力,为心脏安全药理学和疾病建模提供了变革性工具。
关键技术方法包括:1)喷墨印刷制备P3HT半导体通道(30 nm厚度,粗糙度1 nm);2)hiPSC-CMs在纤维连接蛋白包被的EGOFET上形成单层培养;3)电解质门控配置(细胞培养基作为电解质,铂电极作栅极);4)多电极阵列(MEAs)和膜片钳技术平行验证;5)扫描电镜-聚焦离子束(SEM-FIB)表征细胞/晶体管界面结构。
结果部分
Action potential recordings
EGOFET在VGS=-0.8 V、VDS=-0.5 V工作点时,跨导gm=40 μS,信噪比-60 dB。与膜片钳相比,APD20、APD50和APD90(动作电位复极化20%/50%/90%时长)无显著差异(p>0.05),且搏动频率与MEAs结果一致。
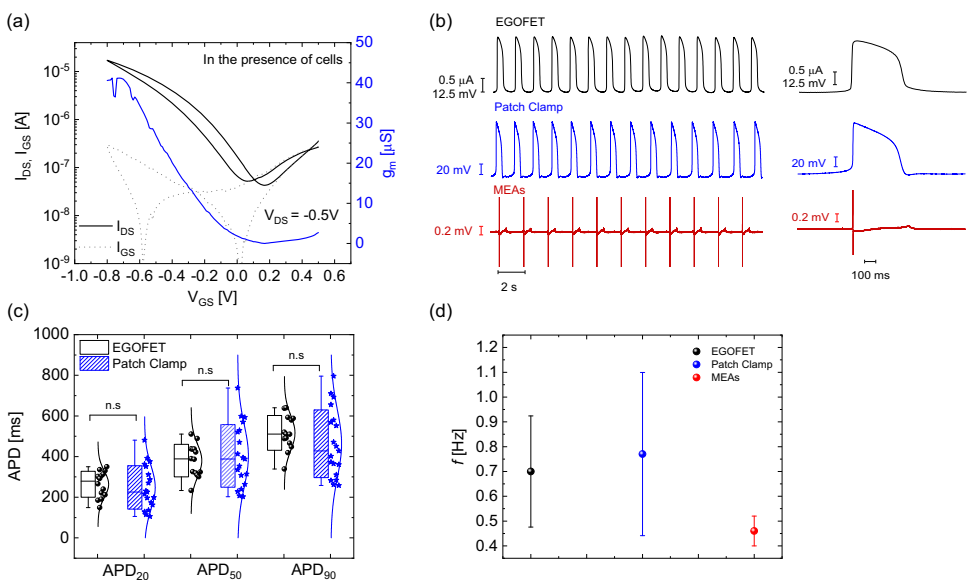
Transduction mechanism
理论计算表明,细胞膜与晶体管通道间自发形成高阻抗密封(>1 GΩ),使跨膜AP能通过离子重分布调控局部电化学势,从而调制P3HT沟道电导。当VGS<-0.2 V时,信号形态从AP转变为微分形态,证实双栅极调控机制。
Drug tests
应用钙通道阻滞剂硝苯地平(NIFE)后,APD缩短并出现舒张期振荡;hERG阻滞剂E-4031则诱发APD延长和EADs交替现象。EGOFET可持续监测30分钟,优于膜片钳的10分钟极限。
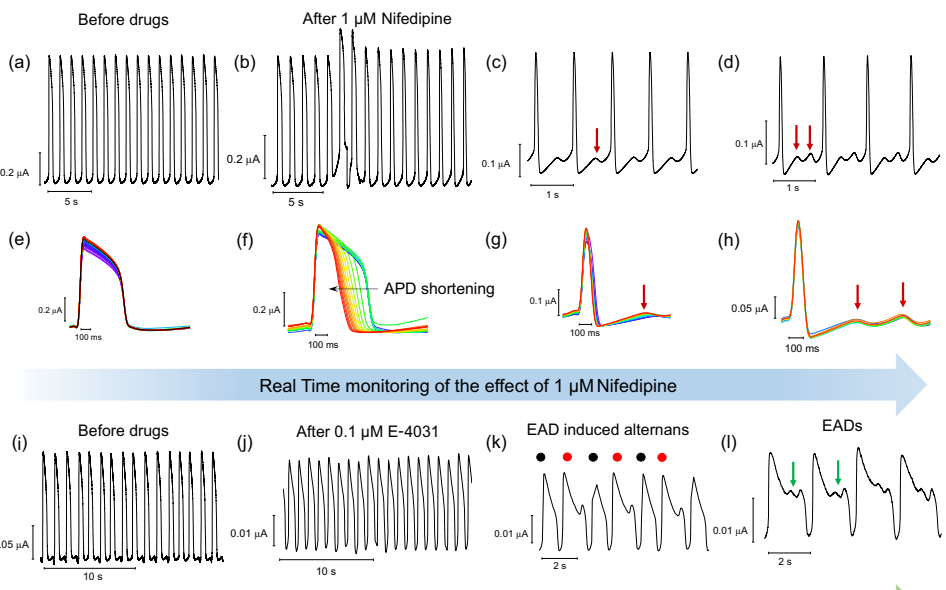
这项研究通过印刷电子学与电生理学的交叉创新,建立了首个无需膜穿孔即可记录完整AP波形的晶体管平台。其核心突破在于:1)P3HT薄膜与细胞膜形成类紧密连接的高阻界面;2)离子门控机制实现AP信号直接转换;3)可扩展的喷墨印刷工艺。该技术不仅满足FDA现代化法案2.0对非动物模型的需求,更为研究心肌细胞、神经元等兴奋性细胞提供了新范式。未来通过优化工作电压窗口(避免膜损伤)和集成多通道阵列,有望推动心脏芯片和神经接口领域的发展。
 生物通微信公众号
生物通微信公众号
知名企业招聘