
-

生物通官微
陪你抓住生命科技
跳动的脉搏
综述:Wnt-NAD+轴在癌症、衰老和组织再生中的作用
【字体: 大 中 小 】 时间:2025年09月01日 来源:TRENDS IN Cell Biology 18.1
编辑推荐:
这篇综述系统阐述了Wnt信号通路与烟酰胺腺嘌呤二核苷酸(NAD+)代谢的交叉调控机制,揭示了二者通过Sirtuins(SIRT1-7)、PARPs等NAD+依赖性酶形成的分子网络如何影响干细胞功能、组织稳态和衰老相关疾病(如癌症、骨质疏松)。作者提出靶向Wnt-NAD+轴(如NAD+前体NMN、CD38抑制剂)可能成为抗衰老和再生医学的新策略。
细胞能量代谢的核心分子NAD+作为氧化还原反应的辅因子,通过糖酵解和三羧酸循环等保守途径维持生命活动。其合成依赖三种路径:从头合成(色氨酸)、补救途径(NMN)和Preiss-Handler途径(烟酸)。NAD+可磷酸化为NADP+,前者主导分解代谢,后者促进合成代谢。这两种分子还作为底物参与DNA修复、基因表达调控等过程。
随着单细胞生物向多细胞生物的进化,Wnt信号通路(由小鼠Int1和果蝇Wingless基因融合命名)应运而生,协调细胞通讯和组织稳态。该网络包含经典Wnt/β-catenin通路(调控增殖分化基因)和两种非经典通路:平面细胞极性(PCP)通路调控细胞极性,Wnt/Ca2+通路调节细胞迁移。衰老过程中NAD+水平下降与Wnt信号紊乱共同导致再生能力衰退。
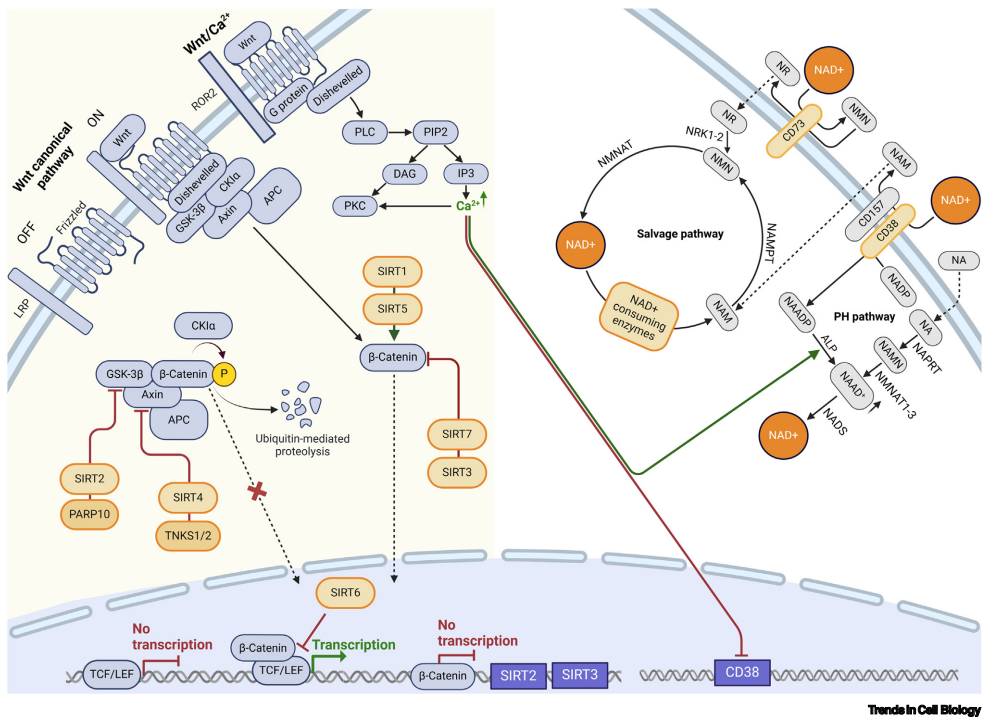
NAD+代谢与Wnt信号呈现区室化分布特征。胞质、线粒体和细胞核内的NAD+池依赖局部酶系统,而Wnt/β-catenin通路从细胞外延伸至核内。这种区室化创造了两者的交互节点:
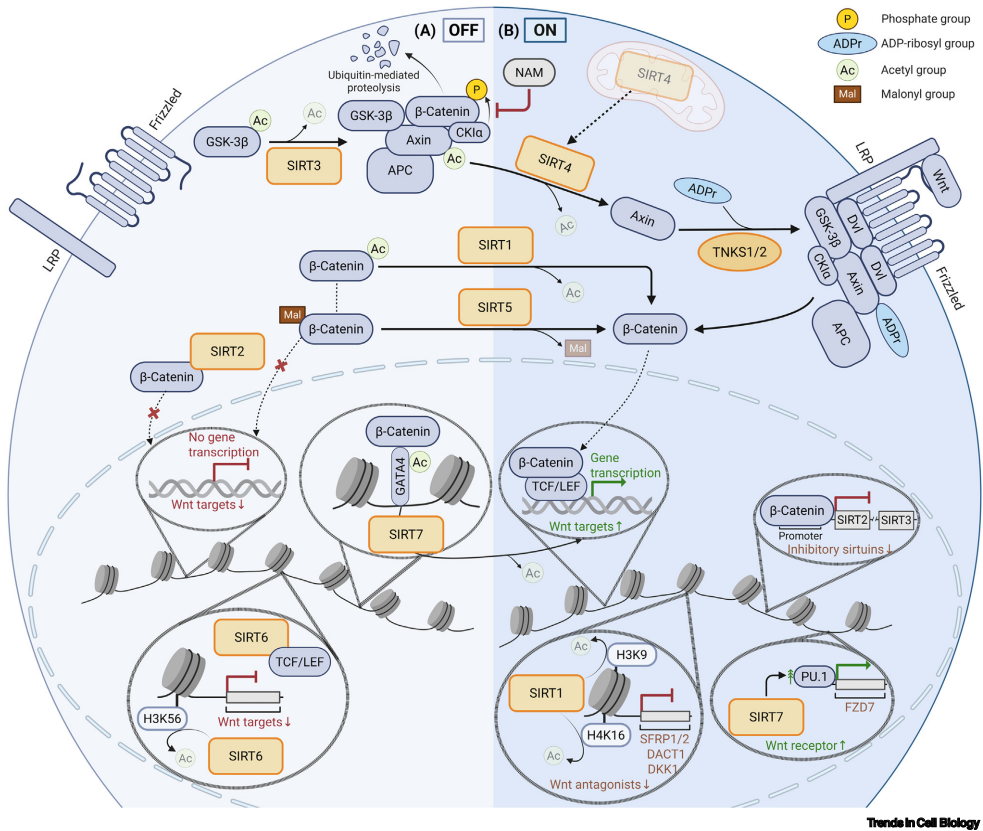
Sirtuins的双向调控
SIRT1在间充质干细胞中通过β-catenin去乙酰化促进其核转位,同时表观沉默Wnt拮抗剂DKK1/SFRP1/2
SIRT2在结肠癌细胞中结合β-catenin阻断其核转位
SIRT3通过激活GSK-3β促进β-catenin降解,但在前列腺癌中β-catenin又可抑制SIRT3启动子
PARPs的桥梁作用
坦克蛋白(TNKS1/2)通过ADP-核糖基化修饰Axin:一方面标记Axin经RNF146泛素化降解,另一方面增强Axin与磷酸化LRP6的结合,形成Wnt信号的正反馈循环。
衰老伴随NAD+水平下降,主要由于CD38表达上调和PARP1过度激活。炎症微环境加剧这一过程,例如巨噬细胞中NAD+耗竭会激活NLRP3炎症小体。在钙化性主动脉瓣疾病(CAVD)中,CD38驱动的NAD+降解无法通过前体补充逆转,提示组织特异性机制。
Wnt/β-catenin通路随年龄呈现复杂变化:在肠道干细胞中活性降低导致再生障碍,但在肌肉前体细胞中过度激活则促使纤维化。端粒维护是二者交汇的典型场景――β-catenin直接上调端粒酶TERT和端粒保护蛋白TRF2的表达,而端粒损伤激活的p53/miR-34a轴又可抑制SIRT1和Wnt信号。
NAD+提升策略
前体补充:NMN通过SLC12A8转运体吸收,在小鼠中改善血管功能和线粒体动力学
酶抑制剂:CD38抑制剂78c延长小鼠寿命;PARP抑制剂PJ34维持造血干细胞功能
微生物干预:阿克曼菌(Akkermansia muciniphila)模拟NMN的促修复效应
Wnt靶向技术
离子调节:锂离子通过抑制GSK-3β稳定β-catenin
配体递送: immobilized Wnt3a("Wnt-bandage")使老年小鼠骨修复能力年轻化
小分子干预:XAV939纳米脂质体在眼病模型中抑制异常血管生成
这些突破性发现为理解代谢-发育信号整合提供了新范式,但组织特异性效应(如SIRT7在骨分化与肝癌中的相反作用)和长期安全性仍是未来研究的重点。
 生物通微信公众号
生物通微信公众号
知名企业招聘