
-

生物通官微
陪你抓住生命科技
跳动的脉搏
综述:TREK-1与癫痫:星形胶质细胞-神经元相互作用中K+平衡和谷氨酸释放的调控
【字体: 大 中 小 】 时间:2025年09月02日 来源:Behavioral and Brain Functions 3.3
编辑推荐:
(推荐语)本综述系统探讨了双孔钾通道TREK-1通过调控星形胶质细胞的K+缓冲(Kir4.1/TWIK-1异源二聚体)和谷氨酸释放(GLT-1/mGluR3通路),在癫痫病理机制中的双重作用,为靶向神经胶质网络的抗癫痫药物开发提供了新视角。
作为双孔域钾通道(K2P)家族的"背景泄漏通道",TREK-1通过四跨膜螺旋结构(M1-M4)和GFG基序维持静息膜电位。其C末端可响应机械张力、pH、多不饱和脂肪酸(PUFAs)等刺激,而调节口袋"cap"结构是麻醉剂的作用靶点。与TWIK-1形成的异源二聚体是功能关键。
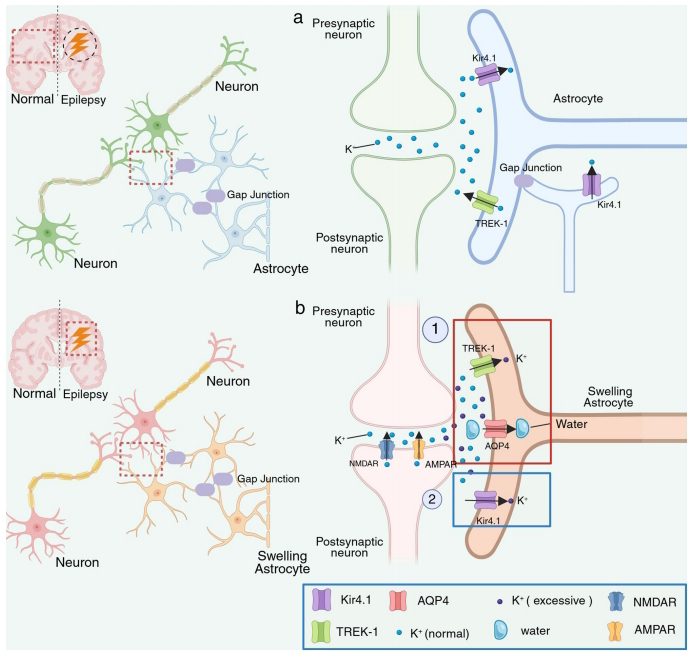
在急性神经元活动中,TREK-1(而非Kir4.1)通过AQP4介导的水转运驱动瞬时K+摄取,导致星形胶质细胞肿胀。而TWIK-1/TREK-1异源二聚体维持的"被动电导"特性,通过NHERF-1调控影响癫痫易感性。实验显示,TREK-1突变体TREK-M可增强K+电流并减少癫痫发作时长。
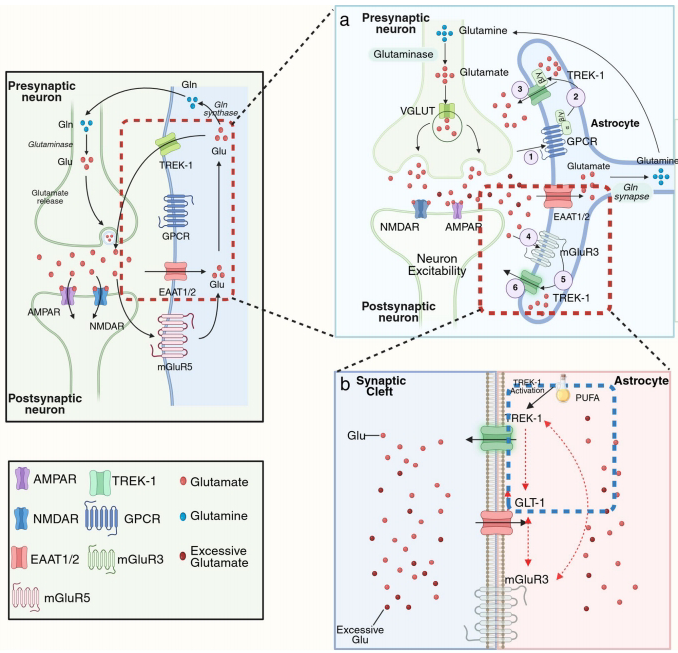
TREK-1通过双重机制参与突触谷氨酸调控:
快速释放:Gi蛋白偶联受体(如GABABR)激活后,Gβγ亚基与TREK-1结合形成谷氨酸渗透通道;
清除增强:PUFAs激活TREK-1可上调谷氨酸转运体GLT-1表达,而mGluR3持续激活也能通过GLT-1促进谷氨酸再摄取。
TREK-1激活剂(如DCPIB、ALA)通过调节K+稳态和GLT-1功能展现神经保护作用,但其在时空特异性调控中的精确机制仍需通过条件性敲除模型验证。星形胶质细胞体积变化与TREK-1活性的关联,为理解癫痫中的突触微环境重塑提供了新思路。
(注:全文严格依据原文数据,未添加非文献支持内容)
 生物通微信公众号
生物通微信公众号
知名企业招聘