
-

ЩњЮяЭЈЙйЮЂ
ХуФузЅзЁЩњУќПЦММ
ЬјЖЏЕФТіВЋ
ОоЪЩЯИАћЬњЫРЭіЧ§ЖЏGCN2ШБЯнгеЕМЗЮОВТіЖЏТіЛЏаТЛњжЦМААаЯђИЩдЄВпТд
ЁОзжЬхЃК Дѓ жа аЁ ЁП ЪБМфЃК2025Фъ09дТ23Ше РДдДЃКNature Communications 15.7
БрМЭЦМіЃК
ЁЁЁЁБОЦкЭЦМіЃКЮЊНтОіЗЮОВТіБеШћадМВВЁ(PVOD)жаGCN2(EIF2AK4)ШБЯнЕМжТЗЮОВТіжиЫмЕФЛњжЦФбЬтЃЌбаОПШЫдБЭЈЙ§ЕЅЯИАћВтађЁЂПеМфзЊТМзщКЭЛљвђБрМаЁЪѓФЃаЭЃЌЪзДЮЗЂЯжОоЪЩЯИАћЬњЫРЭіЪЧЧ§ЖЏОВТіФкЦЄЖЏТіЛЏЕФЙиМќЛЗНкЃЌжЄЪЕЬњЫРЭівжжЦМСFerrostatin-1ПЩФцзЊМВВЁБэаЭЃЌЮЊPVODжЮСЦЬсЙЉСЫаТАаЕуЁЃ
дкЗЮЖЏТіИпбЙМВВЁЦзжаЃЌЗЮОВТіБеШћадМВВЁ(Pulmonary Veno-Occlusive Disease, PVOD)ЪЧвЛжжКБМћШДжТУќЕФбЧаЭЃЌЦфЬиеїЮЊЗЮаЁОВТіНјааадБеШћКЭКЌЬњбЊЛЦЫидкОоЪЩЯИАћжаЕФвьГЃГСЛ§ЁЃЫфШЛМШЭљбаОПЗЂЯждкМвзхадКЭЩЂЗЂадPVODЛМепжаДцдкGeneral Control Nonderepressible 2(GCN2, гЩEIF2AK4ЛљвђБрТы)ЕФЫЋЕШЮЛЛљвђЭЛБфЃЌЕЋGCN2ШБЯнШчКЮгАЯьЗЮОВТіЯИАћМАЦфЮЂЛЗОГЕФОпЬхЛњжЦШдВЛУїШЗЁЃИќбЯОўЕФЪЧЃЌФПЧАГ§ЗЮвЦжВЭтЩаЮогааЇжЮСЦЗНЗЈЃЌЛМепеяЖЯКѓжаЮЛЩњДцЦкВЛзуСНФъЃЌетЭЙЯдСЫНвЪОЦфЗжзгЛњжЦВЂПЊЗЂАаЯђСЦЗЈЕФНєЦШадЁЃ
еыЖдетвЛЬєеНЃЌгЩеХОИдЖЁЂУЋХхЁЂжмЬкЗЩЕШбаОПШЫдБзщГЩЕФбаОПЭХЖгдкЁЖNature CommunicationsЁЗЩЯЗЂБэСЫзюаТбаОПГЩЙћЁЃЫћУЧЭЈЙ§ећКЯСйДВбљБОЗжЮіЁЂЕЅЯИАћЖрзщбЇММЪѕЁЂЛљвђЙЄГЬЖЏЮяФЃаЭКЭЗжзгЩњЮябЇЪЕбщЃЌЯЕЭГВћУїСЫGCN2ШБЯнЭЈЙ§геЕМОоЪЩЯИАћЬњЫРЭіЃЈferroptosisЃЉНјЖјЧ§ЖЏЗЮОВТіЖЏТіЛЏЕФШЋаТЛњжЦЃЌВЂбщжЄСЫАаЯђЬњЫРЭіЕФжЮСЦЧБСІЁЃ
баОПжївЊВЩгУСЫвдЯТЙиМќММЪѕЗНЗЈЃК1) ЖдPVODЛМепКЭЖдеезщЗЮзщжЏНјааЕЅЯИАћRNAВтађ(scRNA-seq)КЭПеМфзЊТМзщбЇ(10x Visium)ЗжЮіЃЛ2) ЙЙНЈаЏДјШЫРржТВЁЭЛБфEif2ak4
баОПНсЙћ
PVODЛМепЗЮОоЪЩЯИАћЬњЫРЭіЯрЙиЛљвђБэДяЩЯЕї
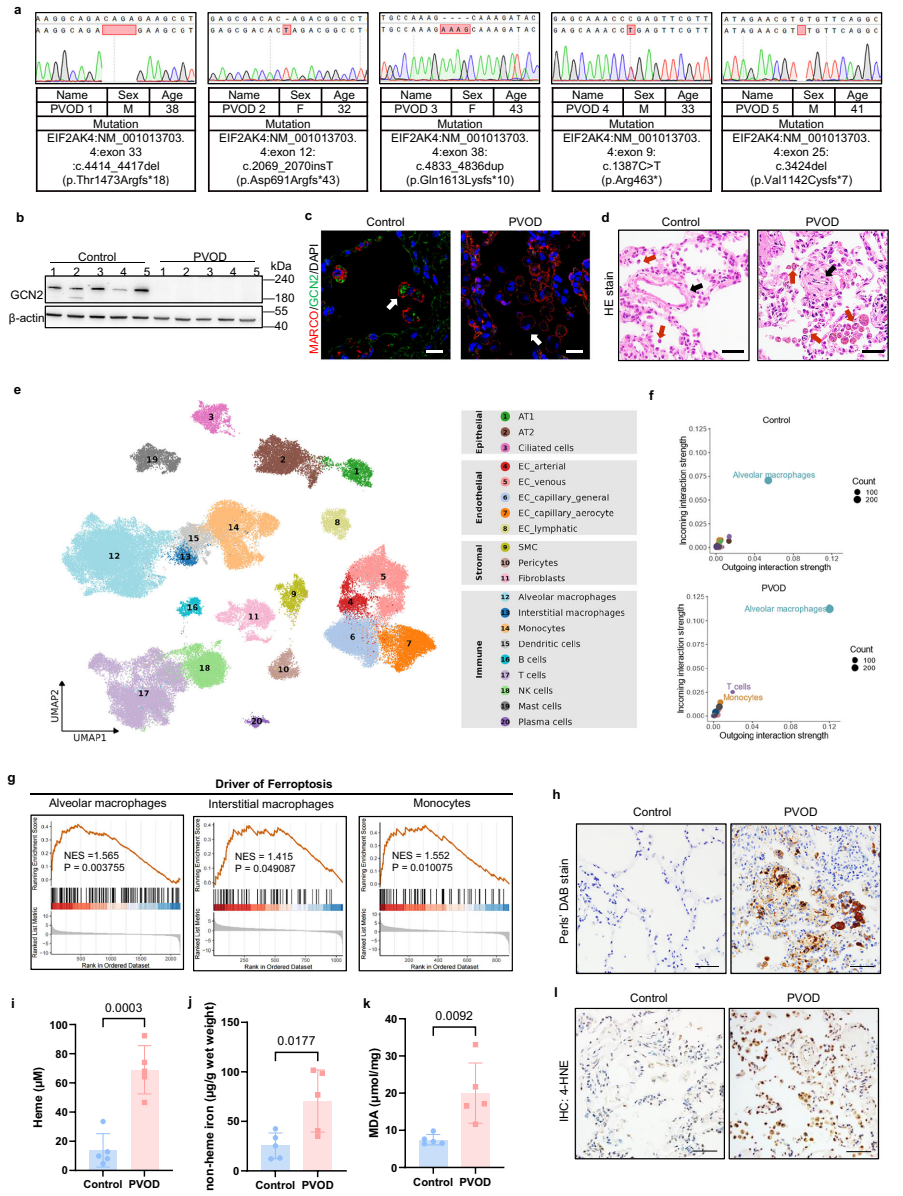
ЭЈЙ§ЖдPVODЛМепЗЮзщжЏЕФУтвпзщЛЏКЭscRNA-seqЗжЮіЃЌЗЂЯжGCN2ЕААзБэДяШБЪЇЃЌЧвОоЪЩЯИАћЪЧжївЊЪмРлЯИАћШКЁЃЛљвђМЏИЛМЏЗжЮіЯдЪОЃЌОоЪЩЯИАћжаЬњЫРЭіЭЈТЗЛљвђЯджјЩЯЕїЁЃЦеТГЪПРЖШОЩЋжЄЪЕЛМепЗЮзщжЏЬњГСЛ§діМгЃЌжЌжЪЙ§бѕЛЏВњЮяMDAКЭ4-HNEЫЎЦНЩ§ИпЃЌЬсЪОЬњЫРЭіМЄЛюЁЃ
Eif2ak4
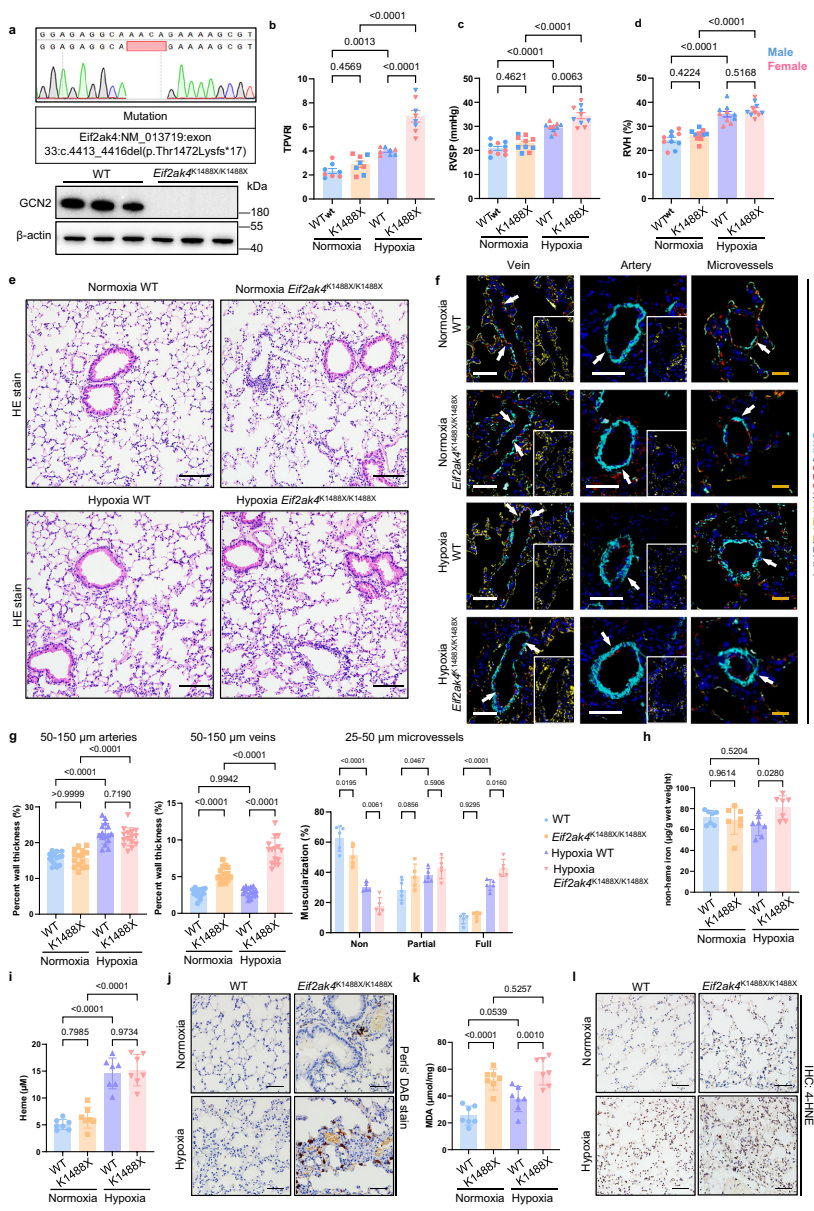
баОПЭХЖгЙЙНЈСЫаЏДјШЫРржТВЁЭЛБфЕФаЁЪѓФЃаЭЁЃШБбѕ6жмКѓЃЌЭЛБфаЁЪѓГіЯжЯджјЕФЗЮбЊЙмзшСІжИЪ§(TPVRI)КЭгваФЪвЪеЫѕбЙ(RVSP)Щ§ИпЃЌВЁРэМьВщЗЂЯжЗЮОВТіМЁЛЏМАбзжЂЯИАћНўШѓЁЃЭЛБфаЁЪѓЗЮзщжЏЬњГСЛ§ЁЂMDAКЭ4-HNEЫЎЦНЯджјдіМгЃЌжЄЪЕЬњЫРЭіЗЂЩњЁЃ
Fer-1ФцзЊвХДЋадКЭвЉЮягеЕМадPVODФЃаЭБэаЭ
ЪЙгУЬњЫРЭівжжЦМСFer-1НјааИЩдЄЃЌЮоТлдкдЄЗРЛЙЪЧжЮСЦФЃЪНЯТЃЌОљФмЯджјНЕЕЭEif2ak4
GCN2ШБЯнЭЈЙ§ЩЯЕїHMOX1діЧПОоЪЩЯИАћЬњЫРЭіУєИаад
ЛњжЦЩЯЃЌGCN2ШБЯнЕФОоЪЩЯИАћКЭHT1080ЯИАћжабЊКьЫиМгбѕУИ1(HMOX1)БэДяЯджјЩ§ИпЃЌЕМжТЬњЪЭЗХдіМгЁЃЬњДІРэЯджјНЕЕЭGCN2ШБЯнЯИАћЕФЛюСІЃЌдіМгжЌжЪЙ§бѕЛЏКЭЯИАћФкЬњГСЛ§ЃЌжЄЪЕGCN2ШБЯнЭЈЙ§HMOX1ЭООЖМгОчЬњЫРЭіЁЃ
GCN2ШБЯндіЧПОВТіФкЦЄЯИАћЖЏТіЛЏКЭЦНЛЌМЁЯИАћеаФМ
scRNA-seqЗжЮіЗЂЯжЃЌPVODЛМепОВТіФкЦЄЯИАћ(VECs)жаЖЏТіБъжОЮяNRP1ЁЂKDRЁЂEFNB2вдМАNOTCH4ЁЂJAG2ЁЂCXCL12БэДяЩЯЕїЃЌЖјОВТіБъжОЮяTEKЁЂACKR1БэДяЯТНЕЃЌЬсЪООВТіЯђЖЏТіЕФУќдЫзЊБфЁЃПеМфзЊТМзщНјвЛВНжЄЪЕбЊЙмЧјгђЖЏТіЬиеїдіЧПЁЃ
ETS1зЊТМвђзгЕїПиNRP1/KDR/EFNB2БэДяЧ§ЖЏОВТіЖЏТіЛЏ
ЭЈЙ§ПеМфзЊТМзщКЭзЊТМвђзгЛюадЗжЮіЃЌЗЂЯжETS1ЪЧPVODбЊЙмжазюЯджјЩЯЕїЕФзЊТМвђзгЃЌжБНгЕїПиNRP1КЭKDRЕФБэДяЁЃЬхЭтЪЕбщжЄЪЕЃЌЬњДІРэПЩгеЕМGCN2ШБЯнЕФШЫЦъОВТіФкЦЄЯИАћ(hUVECs)жаNRP1ЁЂEFNB2БэДяКЭERKСзЫсЛЏЫЎЦНЩ§ИпЁЃ
баОПНсТлгывтвх
БОбаОПЪзДЮНвЪОСЫGCN2ШБЯнЕМжТPVODЕФШЋаТЛњжЦЃКGCN2ШБЪЇЭЈЙ§ЩЯЕїОоЪЩЯИАћжаHMOX1БэДяЃЌДйНјЬњЫРЭіЗЂЩњКЭЬњРызгЪЭЗХЃЛЮЂЛЗОГжаЕФЬњРызгЭЈЙ§МЄЛюETS1зЊТМвђзгЃЌЩЯЕїОВТіФкЦЄЯИАћжаNRP1ЁЂKDRЁЂEFNB2ЕШЖЏТіБъжОЮяЕФБэДяЃЌЧ§ЖЏОВТіФкЦЄЯђЖЏТіБэаЭзЊЛЏЃЌзюжеЕМжТЗЮОВТіБеШћадВЁБфЁЃ
етвЛЗЂЯжВЛНіЮЊРэНтPVODЕФЗЂВЁЛњжЦЬсЙЉСЫШЋаТЪгНЧЃЌИќживЊЕФЪЧЬсГіСЫАаЯђЬњЫРЭіЕФжЮСЦаТВпТдЁЃбаОПБэУїЬњЫРЭівжжЦМСFerrostatin-1ФмЙЛгааЇФцзЊЖЏЮяФЃаЭЕФМВВЁБэаЭЃЌетЮЊПЊЗЂPVODЕФАаЯђжЮСЦЬсЙЉСЫжБНгЪЕбщвРОнЁЃДЫЭтЃЌбаОПМјЖЈЕФNRP1/KDR/EFNB2аХКХжсзїЮЊОВТіЖЏТіЛЏЕФЬивьадБъжОЮяМЏКЯЃЌПЩгУгкPVODЕФСйДВеяЖЯКЭСЦаЇЦРЙРЁЃ
ИУбаОПЕФДДаТаддкгкЃКЪзДЮНЈСЂСЫФЃФтШЫРрPVODЕФвХДЋЙЄГЬаЁЪѓФЃаЭЃЛЭЈЙ§ЖрзщбЇММЪѕНвЪОСЫОоЪЩЯИАћ-ФкЦЄЯИАћЛЅзїЕФаТЛњжЦЃЛНЋЬњЫРЭігыбЊЙмжиЫмЯрСЊЯЕЃЌЭиеЙСЫЯИАћЫРЭіЗНЪНдкбЊЙмМВВЁжаЕФзїгУЃЛЬсГіСЫПЩзЊЛЏЕФжЮСЦВпТдЃЌОпгаживЊЕФСйДВвтвхЁЃетаЉЗЂЯжВЛНіЪЪгУгкPVODЃЌвВПЩФмЮЊЦфЫћРраЭЕФЗЮЖЏТіИпбЙКЭбЊЙмжиЫмадМВВЁЬсЙЉаТЕФжЮСЦЫМТЗЁЃ
 ЩњЮяЭЈЮЂаХЙЋжкКХ
ЩњЮяЭЈЮЂаХЙЋжкКХ
жЊУћЦѓвЕеаЦИ
НёШеЖЏЬЌ | ШЫВХЪаГЁ | аТММЪѕзЈРИ | жаЙњПЦбЇШЫ | дЦеЙЬЈ | BioHot | дЦНВЬУжБВЅ | ЛсеЙжааФ | ЬиМлзЈРИ | ММЪѕПьбЖ | УтЗбЪдгУ
АцШЈЫљга ЩњЮяЭЈ
Copyright© eBiotrade.com, All Rights Reserved
СЊЯЕаХЯфЃК
дСICPБИ09063491КХ