
-

生物通官微
陪你抓住生命科技
跳动的脉搏
基于酿酒酵母表达系统的新型重组ROP6蛋白疫苗显著诱导免疫应答并提供抗弓形虫病保护效果
【字体: 大 中 小 】 时间:2025年09月27日 来源:Scientific Reports 3.9
编辑推荐:
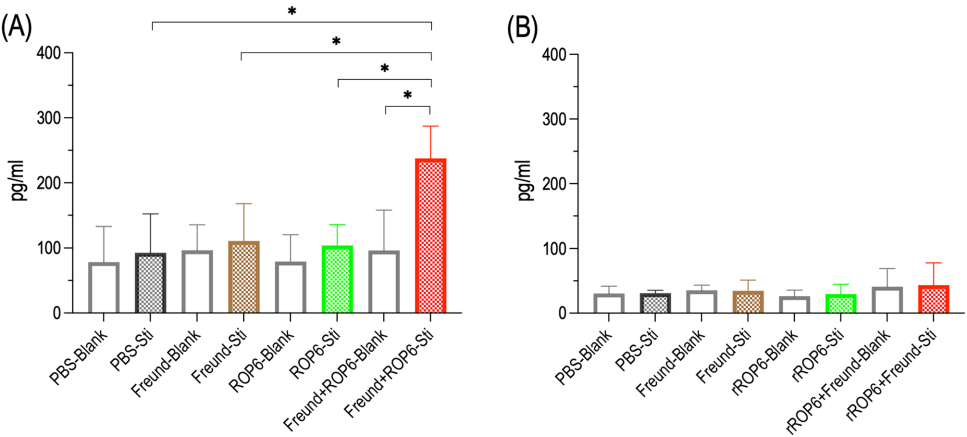
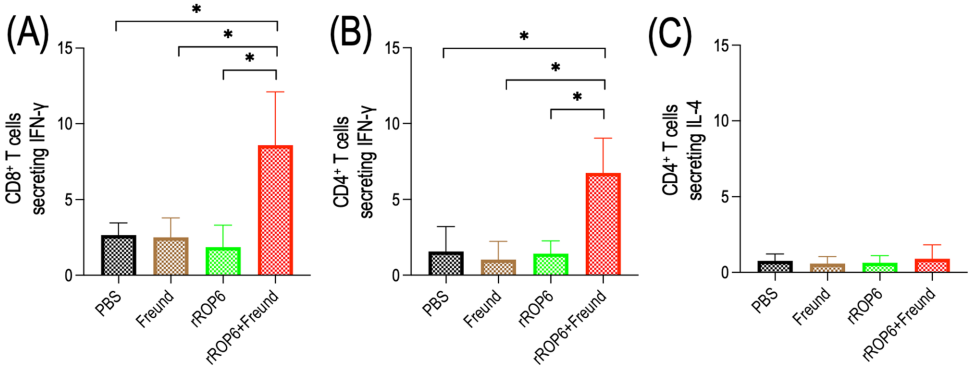
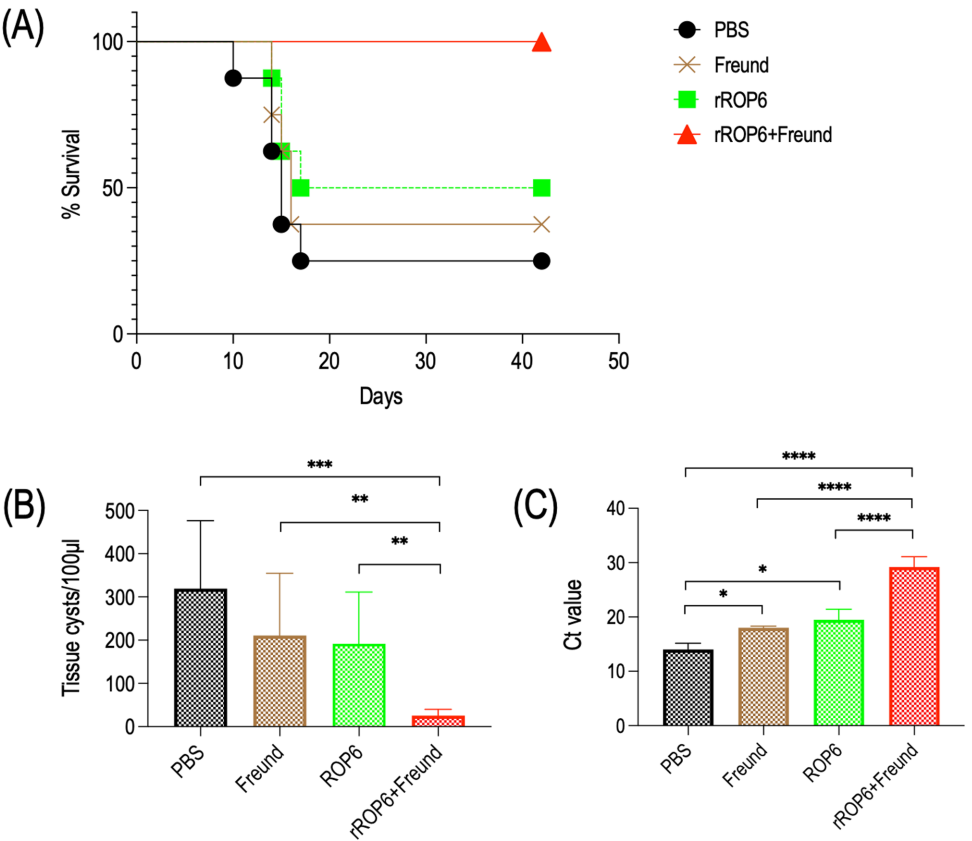
本研究针对慢性弓形虫病缺乏有效防治手段的难题,开发了基于弓形虫棒状体蛋白ROP6的重组亚单位疫苗。研究人员通过酿酒酵母INVSc1细胞表达系统成功制备重组rROP6蛋白,并联合弗氏佐剂免疫BALB/c小鼠。实验结果表明,该疫苗能激发强烈的IgG抗体反应和CD8+ T细胞免疫应答,攻毒实验显示免疫组小鼠全部存活,脑组织内包囊数量和虫体DNA载量显著降低(P<0.0001)。该研究为开发安全有效的人畜共患弓形虫病疫苗提供了重要实验依据。

 生物通微信公众号
生物通微信公众号
知名企业招聘