《Molecular Biomedicine》:Targeting ferroptosis in cancer: from mechanistic insights to therapeutic approaches
编辑推荐:
这是一篇关于铁死亡在癌症治疗中应用的前沿综述。文章系统阐述了这种铁依赖、脂质过氧化驱动的程序性细胞死亡方式的分子机制,包括铁代谢、脂质代谢和抗氧化系统(如Xc?-GSH-GPX4轴、FSP1-CoQ10和GCH1-BH4通路)。作者探讨了铁死亡与铜死亡、双硫死亡及自噬等其他细胞死亡形式的互作,及其在塑造肿瘤免疫微环境中的作用。综述重点总结了通过化疗、放疗、免疫治疗及纳米药物递送策略诱导铁死亡的临床潜力,并指出了在临床转化中面临的挑战,为开发基于铁死亡的新型抗癌疗法连接了机制认知与可行的干预节点。
引言:对抗癌症治疗耐药的新武器
癌症治疗的进步日新月异,靶向治疗、免疫疗法、细胞疗法和纳米医学等创新方案层出不穷。然而,化疗依然是临床治疗的基石。遗憾的是,肿瘤细胞常常对传统疗法产生耐药性,导致治疗失败。主流化疗药物很大程度上依赖细胞凋亡来杀死肿瘤细胞,因此,发现新型的非凋亡性细胞死亡方式来抑制恶性肿瘤生长具有重要的临床意义。铁死亡,作为一种铁依赖性的、由脂质过氧化驱动的非凋亡性程序性细胞死亡方式,正是在此背景下进入了科学家们的视野,并展现出对抗癌症,特别是耐药癌症的巨大潜力。
机制认知一:铁代谢与铁死亡
顾名思义,铁死亡是一个铁依赖的过程。与正常细胞不同,恶性细胞对铁表现出更高的依赖性,这被称为“铁成瘾”,这在一定程度上解释了癌细胞对铁死亡的敏感性。铁过载可诱导多种恶性细胞(如肝癌、肾透明细胞癌等)发生铁死亡。细胞对铁死亡的敏感度,由铁的摄入、储存、降解和输出等多个环节共同决定。
细胞外三价铁离子通过转铁蛋白和转铁蛋白受体1(TFRC)被内吞,在酸性细胞器内被STEAP3还原为二价铁,并通过DMT1等转运体释放到细胞质中,形成不稳定的铁池。这个铁池是启动芬顿反应、产生脂质过氧化物、最终导致铁死亡的关键。许多细胞过程通过调控不稳定铁池的含量来改变癌细胞对铁死亡的敏感性。例如,铁调节蛋白1和2(IRP1/2)协同调控多个铁反应基因。铁蛋白的重链和轻链(FTH1/FTL)表达下调会导致铁含量升高,使黑色素瘤细胞对铁死亡更敏感。相反,参与铁硫簇生物合成的CISD1、CISD3和NFS1表达增加,则导致肝细胞癌、非小细胞肺癌等细胞对铁死亡不敏感。
铁的储存和输出同样关键。细胞内铁蛋白的丰度决定了癌细胞对铁死亡的敏感性,铁蛋白水平越高,对铁死亡的抵抗力越强。肝源性肽激素hepcidin通过结合铁输出蛋白铁转运蛋白(FPN1)并触发其内化和降解,来充当全身铁稳态的“看门人”。FPN1下调会减少细胞铁外流,增加细胞内不稳定铁水平,从而促进铁死亡。在乳腺癌、结直肠癌和肝癌等多种癌症中,肿瘤或基质细胞衍生的hepcidin通过将铁保留在肿瘤细胞和肿瘤相关巨噬细胞内,促进了癌症进展。相反,Prominin 2通过促进含铁蛋白的多泡体和外泌体的形成,将铁运出细胞,从而驱动铁死亡抵抗。2+ is released into the cytosol, contributing to the labile iron pool. Free iron is transported from the extracellular medium to the cytosol by divalent metal transporter 1 (DMT1) and is directly added to the labile iron pool. Iron can also be exported from mitochondria and lysosomes into the cytosol. Ferritinophagy is a mechanism leading to Fe2+release via autophagy-dependent ferritin degradation. This free iron is necessary for the Fenton reaction, which promotes lipid peroxidation, leading to lethal ferroptosis. In contrast, iron export from the tumor cell cytosol prevents iron overloading and inhibits ferroptosis. For example, ferritin captured in multivesicular bodies or exosomes can be transferred extracellularly, leading to cellular resistance to ferroptosis. Importantly, several genes, including NRF2, HIF2α and MTF1, are involved in the regulation of intracellular free irons and influence the vulnerability of cancer cells to ferroptosis">
机制认知二:脂质代谢与铁死亡
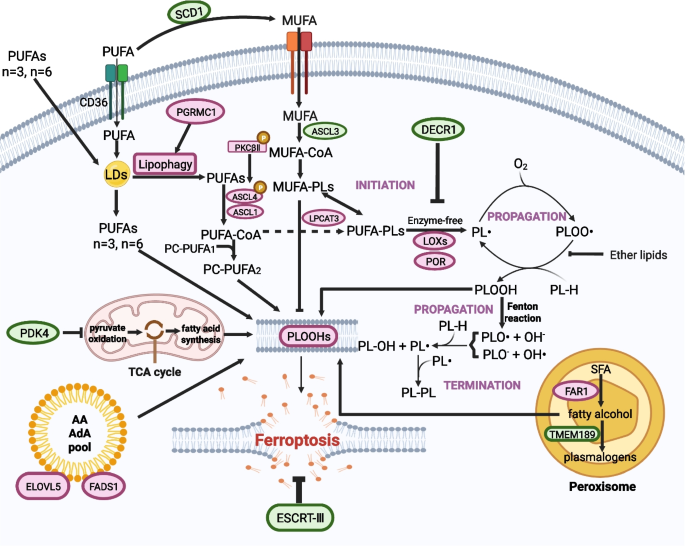
脂质过氧化是铁死亡的标志,它通过破坏细胞膜来驱动铁死亡性细胞死亡。在脂质代谢中,多不饱和脂肪酸(PUFA)的双烯丙基氢原子使其易于发生过氧化,这一过程对铁死亡至关重要。研究表明,只有特定类型的磷脂过氧化物能触发铁死亡,这些游离的PUFA必须被酯化到膜磷脂中才能产生脂质信号。脂质组学分析指出,含有花生四烯酸(AA)或肾上腺酸(AdA)的磷脂酰乙醇胺是铁死亡过程中发生过氧化的关键磷脂。
脂质过氧化可由铁和活性氧/氮物种非酶促驱动,也可由特定的脂质氧化酶酶促驱动。参与酶促过氧化的关键酶包括长链脂肪酰辅酶A连接酶4(ACSL4)、铁依赖性脂氧合酶(LOXs)和细胞色素P450氧化还原酶(POR)。ACSL4是铁死亡的关键驱动因子,它优先连接长链PUFA(如AA和AdA),使其能够被溶血磷脂酰胆碱酰基转移酶(LPCATs)酯化为磷脂。遗传敲除ACSL4会在磷脂中产生单不饱和脂肪酰(MUFA)链,从而在GPX4敲除条件下促使细胞增殖,并保护细胞免受铁死亡。脂氧合酶(LOXs)是另一类关键的脂质氧化酶,它们通过铁不依赖的双加氧作用直接氧化膜中的PUFA,从而促进铁死亡。除了LOXs,细胞色素P450氧化还原酶(POR)和氧化还原酶CYB5R1也被确定为铁死亡的关键介质,它们通过从NAD(P)H向氧气转移电子产生羟基自由基,从而诱导铁死亡。
除了触发脂质过氧化的机制,还有几条保护性通路通过调节脂质代谢来抑制铁死亡。甲羟戊酸途径在细胞内脂质代谢中扮演重要角色,被他汀类药物靶向抑制后可导致铁死亡。另一条脂质代谢通路,环水解酶-1 GCH1-BH4,也通过增加BH4和CoQ10水平来调节脂质过氧化。靶向GCH1-BH4是使癌细胞对铁死亡诱导敏感的有效方法。此外,磷脂酶A2(PLA2)和溶血磷脂酰丝氨酸脂肪酶ABHD12等负调节因子共同作用,将受损的脂肪酰基链排除在癌细胞膜的整合之外。DECR1是PUFA氧化的限速酶,在前列腺肿瘤中通过抑制脂质过氧化而作为铁死亡的负调节因子。
与易于发生脂质过氧化的PUFA相比,MUFA表现出对脂质过氧化的抵抗性。因此,外源性MUFA可被用来替代PUFA。硬脂酰辅酶A去饱和酶(SCD)是MUFA生物合成所必需的。在胃癌中,SCD1的高表达通过抑制铁死亡和改变癌症干性来促进肿瘤生长和迁移。SCD1类似的保护作用在多种癌症中均有观察到,包括KRAS突变肺癌、淋巴转移黑色素瘤和卵巢癌细胞。
机制认知三:抗氧化代谢与铁死亡
谷胱甘肽(GSH)是哺乳动物细胞中最丰富的非蛋白质硫醇,处于细胞氧化还原稳态和铁死亡调节的十字路口。GSH是谷胱甘肽过氧化物酶4(GPX4)的重要辅因子。GPX4利用GSH将有毒的脂质氢过氧化物(LOOH)还原为无害的脂质醇(LOH),从而阻止驱动铁死亡的过氧化链式反应。因此,细胞内GSH池直接决定了细胞对铁死亡的易感性。
癌细胞中的GSH调节是多方面的,涉及生物合成、利用和再循环。GSH的合成关键取决于半胱氨酸的可用性,而半胱氨酸主要通过胱氨酸/谷氨酸逆向转运体系统Xc?(由SLC7A11和SLC3A2组成)导入。在许多癌症中,NRF2等致癌信号通路被持续激活,导致SLC7A11、GCL和其他抗氧化基因的转录上调,从而提高GSH水平和铁死亡抗性。相反,p53等肿瘤抑制因子可以抑制SLC7A11表达或促进促铁死亡代谢转变,使细胞更容易受到脂质过氧化的影响。
新兴的调节因子与信号通路
铁死亡的分子调控机制非常复杂,因为与铁代谢、脂质过氧化、氧化还原稳态和能量代谢相关的分子都可以驱动铁死亡。目前至少已确定了三条经典的信号通路和几条非经典通路来调节癌细胞对铁死亡的敏感性。
Xc?-GSH-GPX4轴
系统Xc?由SLC7A11和SLC3A2组成,作为胱氨酸/谷氨酸逆向转运体发挥着关键作用,它用细胞外的胱氨酸交换谷氨酸,胱氨酸的摄取增强了GSH的形成,进而减弱癌细胞中的氧化应激。在多种人类肿瘤细胞中,发现SLC7A11过表达,并且与患者生存率呈负相关。当肿瘤细胞中SLC7A11表达被敲除后,在几种小鼠模型中肿瘤生长被抑制。由于SLC7A11敲除小鼠健康且可生育,SLC7A11是开发铁死亡诱导剂(如erastin和索拉非尼)的有希望的靶点。
展望:连接机制与临床的桥梁
铁死亡在癌症治疗中的应用前景广阔,特别是在克服耐药性方面。许多具有间质表型、上皮-间质转化或癌症干细胞特性的耐药癌细胞对铁死亡诱导表现出更高的敏感性。放疗、化疗和免疫治疗均可与铁死亡诱导策略联合,产生协同抗肿瘤效应。例如,放疗与免疫治疗相结合可通过协同抑制SLC7A11来促进癌细胞脂质过氧化和铁死亡。纳米医学为铁死亡诱导剂的靶向递送和可控释放提供了创新平台,能够提高疗效并减少脱靶毒性。
然而,铁死亡疗法的临床转化仍面临诸多挑战,包括对铁死亡分子基础的深入理解、如何将铁死亡诱导与常规疗法有效整合、如何平衡基于铁死亡治疗的获益与风险,以及如何克服癌细胞对铁死亡的获得性抵抗。未来的研究需要阐明铁死亡在不同肿瘤背景和器官环境下的特异性调控网络,并开发生物标志物指导的个体化联合治疗方案,从而将这种独特的细胞死亡方式安全、有效地转化为对抗癌症的新武器。



 生物通微信公众号
生物通微信公众号