
-

生物通官微
陪你抓住生命科技
跳动的脉搏
通过编辑玉米黍(Setaria italica)中高表达基因SiPLA的 pollen(花粉),建立一条单倍体诱导系
《Seed Biology》:Establishing a haploid inducer line by edited pollen high expressed gene SiPLA in foxtail millet (Setaria italica)
【字体: 大 中 小 】 时间:2026年04月04日 来源:Seed Biology 3.4
编辑推荐:
狗尾草(Setaria italica)作为C4作物模型,其单倍体诱导研究通过CRISPR/Cas9技术敲除SiPLA基因,发现其单倍体诱导率(HIR)达6.33%,显著高于之前报道的SiMTL基因(2.8%)。该基因在花粉中高表达,且编辑后产生的T1植株种子设置率平均50.1%,T2自交系中检测到10个单倍体。通过母本为野生型Ci846的杂交实验,验证了父本特异性诱导单倍体的可行性,并发现单倍体植株器官显著变小。研究为狗尾草单倍体育种提供了新基因靶点,并指出通过多基因编辑可进一步提升诱导效率。
粟米(Setaria italica)是一种属于禾本科(Poaceae)Setaria属的二倍体植物,是全球最重要的粮食作物之一。与玉米(Zea mays)、甘蔗(Saccharum officinarum)、高粱(Sorghum bicolor)和柳枝稷(Panicum virgatum)等近缘C4谷物作物相比,粟米及其野生种Setaria viridis具有较小的二倍体基因组、较短的生长周期、易于转化以及便于实验室操作的特点。因此,它逐渐成为研究C4光合作用以及谷物作物抗逆性和养分利用效率的理想模型作物[1。双单倍体(DH)技术包括首先生成单倍体植株,然后通过染色体加倍恢复其正常的染色体数目。这种方法通过显著缩短育种周期来加速遗传改良[2。与传统育种方法相比,单倍体诱导和加倍技术可以在一代内使遗传物质达到纯合状态,从而大大提高育种的进展和效率。
在玉米中鉴定出的单倍体诱导基因促进了相关作物物种中的广泛基因组编辑研究。在众多单倍体诱导基因中,PLA(磷脂酶A)是最早在玉米中发现的基因[3。后续研究在多个物种中鉴定并表征了PLA的同源基因[4,结果一致表明这些基因在花粉中的表达量较高。粟米中也存在多种类似植物的磷脂酶同源基因,但尚不清楚具体是哪个基因负责诱导单倍体形成。Cheng等人[5利用CRISPR/Cas9技术结合高效的遗传转化平台编辑了SiMTL基因,成功培育出了单倍体植株。Huang等人[6通过使用蒲公英(Taraxacum officinale)中PARTHENOGENESIS(PAR)基因在卵细胞中的表达,成功实现了单倍体的种子生成,这为将DH技术应用于粟米育种提供了可能。根据我们的初步研究[7,我们筛选了PLA基因,发现SiPLA(Seita.9G114100)在花粉中的表达量远高于SiMTL(Seita.9G376800)(图1a;补充表S1)。我们还在Ci846品种的不同器官上进行了逆转录-定量聚合酶链反应(RT-qPCR)分析,结果显示SiPLA在花粉中的表达量高于其他组织(图1b)。因此,我们使用CRISPR/Cas9编辑系统设计了针对第一个外显子的引导RNA序列(图1c)。引导RNA的表达由OsU3启动子驱动,而Cas9则受玉米Ubiquitin-1启动子的调控。通过农杆菌介导的方法对Ci846品种进行了转化,获得了104株植株。序列分析显示目标位点发生了48次等位基因编辑。我们从8个携带SiPLA移码突变的T0植株中获得了T1植株(图1d;补充图S1),并检测了它们的结实率。这些< />突变体的平均结实率为50.1%,范围在11.63%到77.56%之间(图1e)。单个花粉粒中的淀粉积累情况正常(补充图S2),这与水稻(Oryza sativa)和小麦(Triticum aestivum)的观察结果一致[8,9)。接下来,我们对3个纯合系进行了自交,得到了T2后代,通过流式细胞术鉴定出10株单倍体,平均单倍体诱导率(HIR)为6.33%。为了评估该诱导系在多种母本背景下的单倍体胚胎生成能力,我们使用去雄的野生型Ci846作为母本,并用Line 5的花粉进行授粉(图1g;补充图S3)。对441株杂交植株进行流式细胞术分析,鉴定出26株单倍体;而当野生型Ci846作为父本时,在188株F1植株中未检测到单倍体。单倍体植株的所有器官(包括叶片、穗和雄蕊)的大小均显著减小(图1h)。
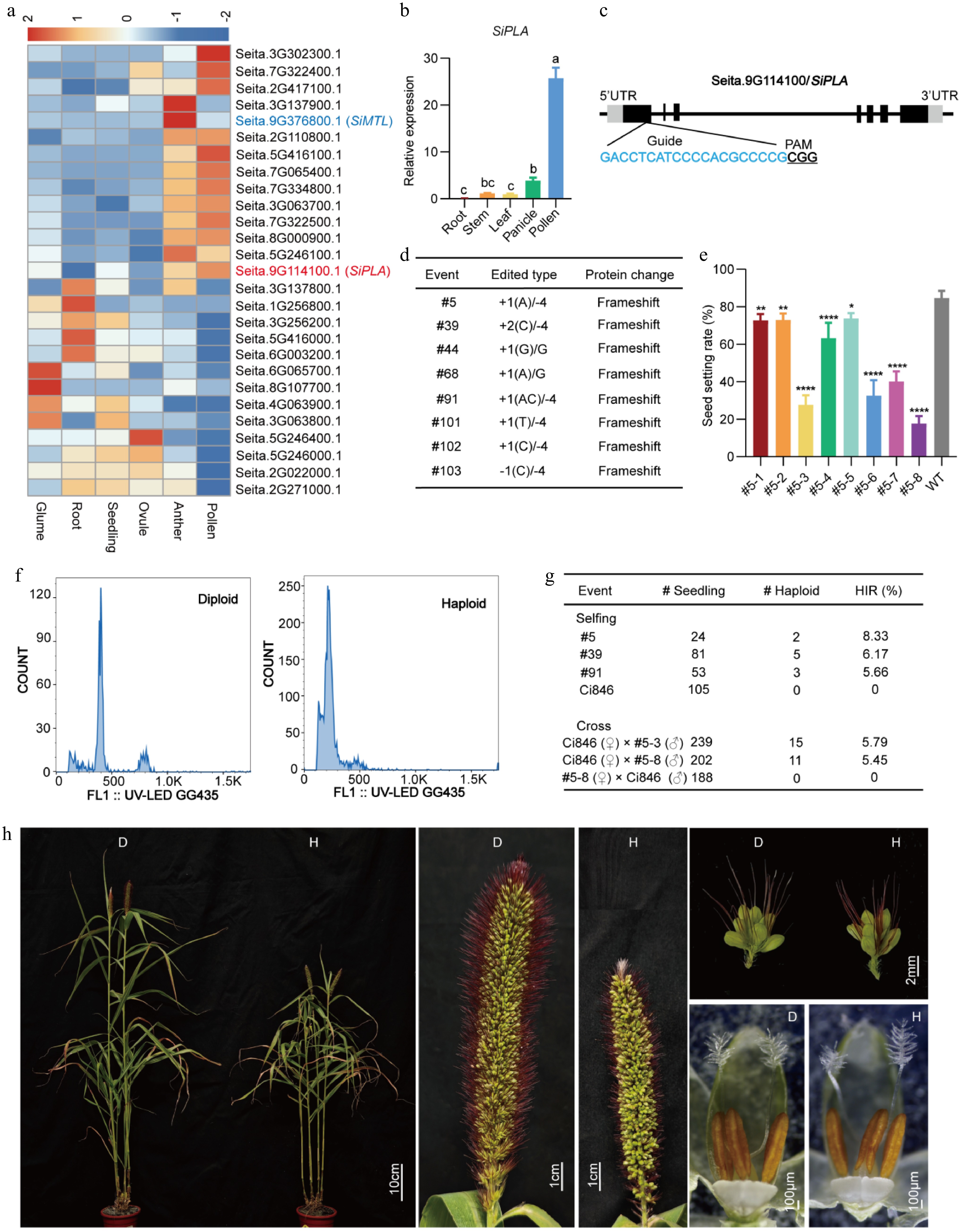
粟米中的单倍体诱导。(a) 从我们的粟米转录组数据中鉴定出的PLA表达热图。彩色框表示log2倍变化值。数字表示每百万 mapped reads 中每个千碱基的转录片段数量(FPKM)的相对表达水平。红色表示上调表达,蓝色表示下调表达。(b) RT-qPCR结果显示花粉中SiPLA的相对表达量较高。使用Tukey方法进行了一元方差分析(ANOVA)以分析显著差异;小写字母表示统计显著性,p < 0.05。(c) SiPLA的基因结构及CRISPR/Cas9靶向位点。PAM部分被下划线标出,引导RNA序列用蓝色突出显示。(d) T0植株中的编辑位点和核酸序列变化。(e) 来自突变体#5的自交T1植株的结实率。每个误差条代表三次生物学重复实验的平均值及其标准差(±SD)(n = 10)。使用单因素方差分析(ANOVA)后进行Tukey多重比较测试(* p < 0.05;** p < 0.01;**** p < 0.0001)。(f) 通过流式细胞术分析验证单倍体植株。x轴表示细胞核信号峰,y轴表示细胞核数量。(g> 通过自交或杂交确定的单倍体诱导效率(HIR)。(h) 单倍体和二倍体植株的表型。"D"表示二倍体对照,"H"表示单倍体。
我们的结果表明,通过敲除SiPLA可以实现粟米中的单倍体诱导。SiPLA是第二个被证实能在粟米中诱导单倍体的同源磷脂酶。其单倍体诱导率(HIR)为6.3%,显著高于先前报道的SiMTL(2.8%),为培育单倍体粟米提供了更有效的候选基因。这一发现为高效诱导粟米无性繁殖提供了理论指导。鉴于不同诱导系在玉米中的诱导率存在差异,我们预计通过使用CRISPR/Cas9技术在粟米中生成具有不同遗传背景的单倍体系,或与其他相关基因的突变结合,可以进一步提高单倍体诱导率[10。
实验使用的是粟米品种Ci846。粟米材料在中国山西农业大学农学院的温室中栽培。温室内的环境条件受到严格控制,温度维持在25°C,光照周期为16小时光照/8小时黑暗。
使用FlaPure Plant Total RNA Extraction Kit(Genesand Biotech,北京)从植物材料中提取RNA,随后使用Union Script First-strand cDNA Synthesis kit(Genesand Biotech,北京)将其逆转录为cDNA。基因表达水平通过特异性引物(补充表S1)和SYBR Green Super Mix(Mei5bio,北京)在Bio-Rad CFX Duet(Bio-Rad CFX Duet,BIORAD,美国)上进行检测。准备20-μL的RT-qPCR反应体系,其中包含2 μL逆转录得到的cDNA作为模板,10 μL的2× Real-time PCR Super Mix(含anti-Taq),以及10 μM的正向和反向引物各0.5 μL,双蒸水调整体积。反应条件为:95°C加热1分钟,随后进行40个循环:95°C 15秒、60°C 15秒、72°C 30秒。使用粟米肌动蛋白基因SiActin(Seita.8G043100)作为内参[11)。目标基因的相对表达水平通过2^(-ΔΔC?)方法计算。
使用CRISPR-GE在线网站(http://skl.scau.edu.cn/home/)设计sgRNA。引物由补充表S1设计,以pcBC-MT1T2为模板进行克隆,并通过BsaI酶连接到< />[12质粒上。质粒被送往中国农业科学院作物科学研究所,Ci846作为遗传转化的受体。
数据分析采用了一元方差分析(ANOVA),随后进行Tukey多重比较测试。显著性水平如下:* p < 0.05,** p < 0.01,*** p < 0.001,**** p < 0.0001;图像采集和处理使用Image J软件。
当栽培材料开始抽穗后,第二天取下穗状花序,将其放入离心管中加水。取一个穗状花序的雄蕊放在载玻片上,加入1-2滴5% I2-KI溶液,用镊子盖住盖玻片并轻轻按压以释放花粉粒,静置2-3分钟。然后在显微镜(Olympus BX51,日本)下观察。
流式细胞术分析由广州瑞益生物科技有限公司完成。
作者对本文的贡献如下:研究设计、手稿撰写:Wang JG, Chu X, Chen DY;实验操作和数据分析:Chen DY, Su M, Sun M, Wang H, Yuan X, Dong S, Li X, Gao L, Yang G。所有作者均审阅了结果并批准了最终版手稿。
本研究生成或分析的所有数据均包含在本文及其补充信息文件中。如需其他格式的原始数据文件,可向通讯作者提出合理请求。
本研究得到了中国国家重点研发计划(2023YFD1202702-6)和国家自然科学基金(32400217和32200222)的支持。
作者声明没有利益冲突。